au sommaire
- À lire aussi
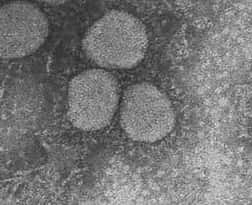
Image en microscopie électronique du nouveau coronavirus causant la pneumonie atypique (SRAS).(crédit : Department of Microbiology, The University of Hong Kong and the Government Virus Unit, Department of Health, Hong Kong SAR China)
L'analyse génétique d'une grande cohorte de sujets hospitalisés pour cette maladie, en Thaïlande, a permis à des chercheurs de l'Institut Pasteur associés à ceux de l'Inserm de mettre en évidence le rôle d'un variant génétique chez les personnes atteintes de formes graves de dengue. Ces travaux, publiés dans Nature Genetics, montrent l'importance de la moléculemolécule DC-SIGN, un co-récepteur du virus de la dengue, dans la pathogenèse de cette maladie. Ils conduisent à revoir les hypothèses actuelles quant au déterminisme des formes graves de dengue et pourraient avoir des conséquences importantes pour le développement de stratégies préventives et thérapeutiques contre cette maladie. Le variant génétique identifié pourrait également être impliqué dans la sensibilité à d'autres infections faisant intervenir la molécule DC-SIGN.
Existe-t-il des facteurs génétiques prédisposant au risque d'infection par les virus de la dengue ou à l'évolution vers les formes graves de la maladie ?
Pour répondre à cette question, l'équipe de Cécile Julier, responsable de l'Unité mixte Institut Pasteur-Inserm « Génétique des Maladies Infectieuses et Autoimmunes » (Institut Pasteur, Unité Inserm 730), a analysé le profil génétiqueprofil génétique d'une cohorte de 600 patients hospitalisés en Thaïlande pour la dengue et de près de 700 individus contrôles. Ce travail a été mené en collaboration avec la Mahidol University à Bangkok, le Centre National de Génotypage à Evry, et l'Unité Interactions FlavivirusFlavivirus-Hôtes de l'Institut Pasteur.
L'étude s'est focalisée sur un gènegène particulier, codant pour DC-SIGN, une molécule qui avait été identifiée en 2003 à l'Institut Pasteur comme un co-récepteur indispensable à l'infection des cellules humaines cibles des virus de la dengue.
Il est reconnu que la majorité des infections par le virus de la dengue (environ 90%) sont asymptomatiques ou résultent en une fièvrefièvre indifférenciée. Parmi les personnes gravement atteintes, deux formes cliniques ont été définies, la fièvre de dengue (FD) et la fièvre hémorragique de dengue (FHD) ; cette dernière, gravissime, est caractérisée cliniquement par une fuite plasmatique, et peut être mortelle.
Un criblage moléculaire du gène codant pour DC-SIGN a permis dans un premier temps d'en définir tous les variants. Les chercheurs ont ensuite montré qu'un des variants génétiques était associé à une forte protection contre la FD : parmi les personnes hospitalisées pour cette maladie, les individus porteurs de ce variant ont en effet un risque 5 fois moins grand de développer une FD que les autres, alors que ce variant n'affecte pas le risque de développer la forme gravissime FHD. Cette étude montre que ces deux formes graves de la dengue répondent à des mécanismes pathophysiologiques au moins en partie distincts.
Les études fonctionnelles menées par les chercheurs sur ce variant de DC-SIGN suggèrent que son rôle protecteur serait lié à une diminution de la quantité du co-récepteur DC-SIGN à la surface des cellules cibles des virus de la dengue (cellules dendritiques). L'absence de protection liée à ce phénomène dans les cas de FHD, laisse penser que dans cette forme de maladie, d'autres mécanismes court-circuiteraient ou minoreraient le rôle du co-récepteur DC-SIGN.
Ces conclusions renforcent l'idée selon laquelle DC-SIGN est une molécule-clé pour la recherche de thérapiesthérapies contre la dengue, dont le rôle différentiel dans les deux formes cliniques de la maladie doit désormais être considéré. Les différences génétiques entre individus aujourd'hui mises en évidence, devraient être prises en compte à l'avenir lors des essais de préventionprévention (par exemple tests vaccinaux) ou de thérapie où cette molécule pourrait intervenir.
Ce gène n'explique pas la totalité des différences inter-individuelles en réponse à l'infection par le virus de la dengue, et l'équipe de Cécile Julier et ses collaborateurs poursuivent leurs recherches d'autres gènes intervenant dans le risque d'infection ou la gravitégravité de la maladie chez les personnes infectées.
Au-delà de la dengue, ces résultats pourraient avoir des implications sur les recherches portant sur d'autres pathologiespathologies. Si DC-SIGN joue en effet un rôle majeur dans les arboviroses (dengue, fièvre à virus West Nile, fièvre jaunefièvre jaune, encéphalite japonaiseencéphalite japonaise), c'est aussi une molécule d'attachement pour divers autres agents infectieux d'intérêt majeur en santé publique: VIHVIH, virus de l'hépatite Chépatite C, cytomégalovirus, virus Ebola, virus du SRASSRAS, bacillebacille de la tuberculosetuberculose et certains parasitesparasites. Le variant qui vient d'être identifié pourrait donc intervenir dans la sensibilité génétique à différentes maladies infectieuses.