au sommaire
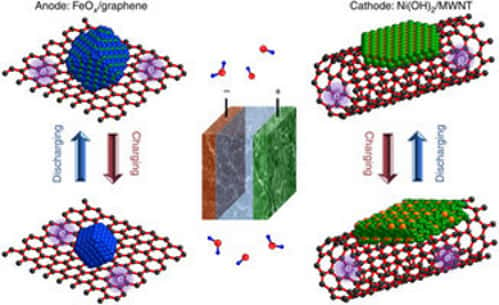
Dans le dispositif expérimental de cette batterie nickel-fer, l'anode (en oxyde de fer, FeOx) est recouverte de graphène, c'est-à-dire d'une couche monoatomique de carbone, et la cathode en nickel (Ni(OH)2/MWNT) est garnie de nanotubes de carbone. Ces surfaces facilitent considérablement le mouvement des charges électriques. © Hailiang Wang et al./Science
La vieille batterie au nickelnickel-ferfer, conçue au tout début du XXe siècle par Thomas EdisonEdison et depuis longtemps passée de mode, vient subitement de prendre un coup de jeune grâce aux nanotechnologies. Une telle batterie pourrait se recharger en 2 minutes et demie et se décharger en moins de 30 secondes, ce qui pourrait vivement intéresser l'industrie automobileautomobile pour de futures voitures électriques.
En 1902, l'inventeur américain et son collègue Waldemar Jungner avaient fabriqué leur batterie à l'aide de deux électrodesélectrodes, l'une en nickel et l'autre en fer, immergées dans une solution alcalinealcaline. Par rapport à la traditionnelle batterie au plombplomb-acideacide, l'accumulateur Ni-Fe a l'avantage d'une plus grande énergieénergie spécifique, 265 Wh/kgkg pour la valeur théorique, contre 170 Wh/kg. Dans la pratique cependant, la différence est moins nette, le couple plomb acide-stagnant entre 30 et 50, le nickel-fer faisant juste un peu mieux, bien en dessous du couple lithium-ion (70 Wh/kg). L'accumulateur Ni-Fe se distingue par sa longue duréedurée de vie et sa résistancerésistance aux décharges profondes et aux surcharges. De plus, le nickel et le fer sont relativement abondants et la solution reste assez inoffensive comparée aux batteries au plomb-acide.
Au chapitre des inconvénients figurent une autodécharge assez grande et, surtout, une décharge lente. La batterie Ni-Fe a du mal à délivrer une forte énergie en peu de temps, ce qu'il faut par exemple quand il s'agit de faire tourner le démarreur d'un moteur thermiquemoteur thermique. Ces caractéristiques ont cantonné ces batteries à des usages restreints. Elles sont par exemple restées une source d'énergie de secours pour les chemins de fer et les mines jusque dans les années 1970. Aujourd'hui, seule une poignée de sociétés fabrique encore ce genre d'accumulateurs, surtout pour stocker les surplus d'électricité générés par les panneaux solaires ou les éoliennes.

En 1910, la voiture électrique équipée de la batterie nickel-fer de Thomas Edison a parcouru un millier de miles, soit 1.600 km, pour démontrer la fiabilité du concept. Mais le moteur thermique l'a emporté... © Stanford University
La batterie nickel-fer, le « turbo » de la voiture électrique ?
Les choses pourraient changer avec l'innovation apportée par Hongjie Dai, chimiste à la Stanford University (États-Unis), et son équipe. Les chercheurs ont conservé le même principe nickel-fer qu'Edison pour les électrodes. Mais ils les ont couplées à des nanotubes de carbonenanotubes de carbone et à du graphènegraphène, un matériaumatériau constitué d'une couche de carbone épaisse de seulement un atomeatome. « Cela permet aux charges électriques de se déplacer rapidement entre les électrodes et dans le circuit extérieur. Le résultat est une version ultrarapide de la batterie nickel-fer », a expliqué Hongjie Dai dans un communiqué de la Stanford University.
On obtient donc une batterie à vitessevitesse de charge élevée, mais avec une vitesse maximale de décharge très grande elle aussi. Le modèle à nanotubes et graphène de la Stanford University devient ainsi plus efficace sur ce plan que les batteries au plomb et au lithiumlithium.
L'innovation en reste pour l'instant à l'échelle du laboratoire. Seul un petit prototype d'un voltvolt capable d'alimenter une lampe-torche a été fabriqué. Mais à taille comparable, l'engin affiche une densité énergétique mille fois supérieure à son ancêtre du début du XXe siècle. « Notre batterie ne sera probablement pas capable à elle seule de propulser une voiture électrique car sa densité énergétique n'est pas idéale. Mais elle pourrait venir en appoint des batteries lithium-ionbatteries lithium-ion en leur donnant un réel surcroît de puissance en cas d'accélération », estime l'un des scientifiques du projet, Hailiang Wang. Après avoir fourni ce coup de pouce au moteur principal, la batterie nickel-fer se rechargerait rapidement grâce à l'énergie récupérée lors du freinage de la voiture.