En chimie, la puissance d’un acide est mesurée par sa capacité à céder un proton, et donc à faire baisser le pH de l’eau. Les acides les plus forts sont aussi généralement les plus corrosifs.
au sommaire
Un acide, en chimie, est une substance capable de libérer des hydrons (ions H+) dans l'eau. Quand on verse un acide dans l'eau, le ratio d'ions H+ va ainsi augmenter, ce qui fait baisser le pH de la solution qui devient alors acide. Plus l'acide cède facilement des protons, plus il est considéré comme puissant. Certains acides sont même si puissants qu'ils « forcent » les autres molécules à leur arracher un hydron. Cette puissance est mesurée par la constante d'acidité, notée Ka : plus le Ka est élevé, plus l'acide est fort -- attention, car cette valeur dépend non seulement de l'acide concerné, mais aussi du solvantsolvant et de la température.
L’acide carborane, 100 milliards de fois plus acide que l’eau
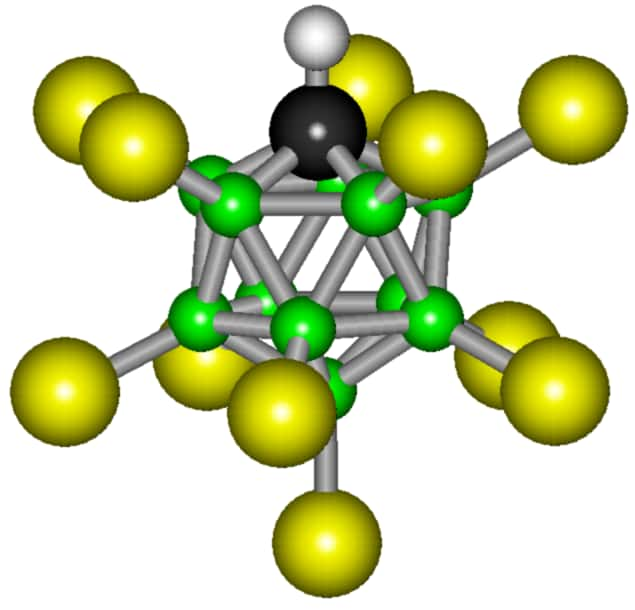
Selon cette définition, c'est l'acide carborane H(CHB11Cl11) qui est l'acide le plus puisant : cette molécule, synthétisée en 2004, est 100 milliards de fois plus acide que l'eau et un million de fois plus réactive que l'acide sulfuriqueacide sulfurique concentré. Cet acide doit ses propriétés à sa structure moléculaire, où les charges négatives sont regroupées au centre sous une couche d'atomesatomes de chlorechlore, ce qui rend les liaisons avec les protons particulièrement fragiles.
Acidité et corrosion : deux propriétés généralement liées
Les acides les puissants sont aussi généralement les plus corrosifs, car une fois débarrassés de leur hydron, ils deviennent très réactifsréactifs et détruisent facilement les liaisons à l'intérieur des autres molécules. Sur ce point, c'est l'acide fluoroantimonique HF·SbF5 qui est le plus puissant, capable de protoner à peu près n'importe quel matériaumatériau (verre, plastiqueplastique, or, airair, eau...). Il est tellement corrosif qu'il doit être conservé dans une bouteille en Téflon, le seul matériau qui lui résiste.
L'acide carborane, lui, fait exception à la règle : il est au contraire remarquablement stable, car la structure négative qui résulte de la perte du proton reste quasiment inerte. Une propriété qui le rend particulièrement intéressant pour une exploitation commerciale, comme la fabrication de vitaminesvitamines qui sont acidifiées, le raffinageraffinage de pétrolepétrole ou la fabrication de polymèrespolymères thermorésistants.