au sommaire
- À lire aussi
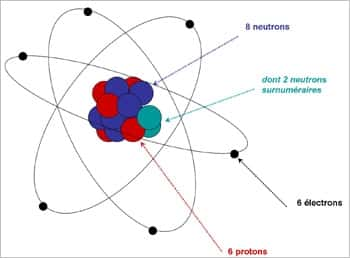
Un atome de carbone 14. Les 6 électrons tournent autour d'un noyau comprenant 6 protons (en rouge) et 8 neutrons (en bleu). C'est deux neutrons de trop : le noyau est instable et les 2 neutrons surnuméraires (en bleu ciel) sont facilement éjectés. L'atome devient alors un carbone 12, stable. © DR
Un radionucléide, ou radioisotope, est un isotope radioactif d'un élément. Il peut en exister des isotopes stables. Exemple : le carbonecarbone 14 (14C) est un radioisotope de l'élément carbone, dont l'isotope le plus commun (12C) est stable.