au sommaire
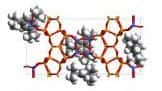
Alumino-silicatesilicate hydraté. La zéolithe (en grec, « pierre qui bout »), ou zéolite, est formée de structures cristallines dans lesquelles quatre atomes d'oxygène enferment un atome de silicium ou d'aluminium.
Formées naturellement dans des eaux alcalinesalcalines ou dans les sédimentssédiments, les zéolithes ont la propriété de gonfler sous l'effet de la chaleur. Chimiquement, elles s'hydratent et se déshydratent de façon réversibleréversible.
On connaît 48 zéolithes naturelles mais les chimistes ont créé près de 200 formes de synthèses. Elles sont utilisées pour filtrer (on les a qualifiées de tamis moléculaire), dans les adoucisseurs d'eau, les colonnes échangeuses d'ionsions, dans les systèmes de production d'oxygène ou encore dans la séparationséparation des produits pétroliers ou lors de l'extraction du gaz naturelgaz naturel. Elles sont aussi utilisées comme catalyseurscatalyseurs dans de nombreux types de réactions chimiquesréactions chimiques. Comme transporteur de potassiumpotassium, certaines font office d'engrais pour l'agricultureagriculture.