au sommaire
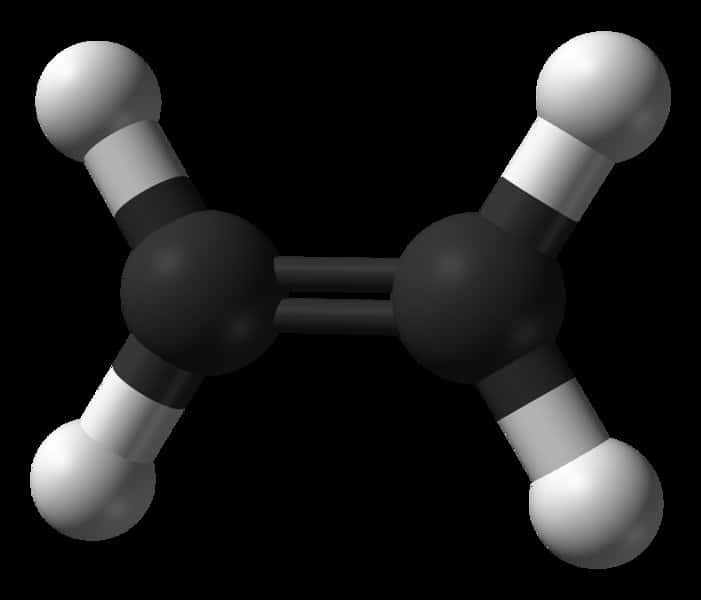
Une représentation de la molécule d'éthylène. On remarque les deux atomes de carbone (en noir), maintenus par leur double liaison, et les quatre atomes d'hydrogène (en blanc). La double liaison peut laisser place à une simple liaison, chaque atome de carbone pouvant alors se lier à un autre atome ou une autre molécule. C'est ainsi que l'on peut polymériser l'éthylène en accrochant les molécules les unes aux autres. © Domaine public
Le processus de production de l'éthylène est majoritairement réalisé par le craquage thermique, aussi connu sous le terme de steamsteam cracking, de naphtha ou de gaz d'hydrocarbures légers. Ce processus implique une décomposition thermique des hydrocarbures à des températures comprises entre 750 et 950°C en présence de vapeur. Cette opération est fondamentale pour briser les liaisons chimiques et libérer l'éthylène ainsi que d'autres hydrocarbures. Le produit ainsi obtenu est ensuite purifié à travers diverses étapes qui incluent la compression, la réfrigération et la distillation pour isoler l'éthylène pur.
Applications de l'éthylène dans divers secteurs
L'éthylène est essentiel dans de nombreuses applications industrielles, notamment dans la production de polymèrespolymères et plastiquesplastiques comme le polyéthylènepolyéthylène, le polychlorure de vinylepolychlorure de vinyle (PVC) et le polystyrènepolystyrène. Le polyéthylène, notamment, est utilisé pour fabriquer une multitude de produits allant des emballages souples aux bouteilles en plastique, en passant par les tubes et les jouets. L'éthylène est également crucial dans la fabrication de l'alcoolalcool éthylique (éthanol) par hydratationhydratation et est un agent clé dans la production de nombreux solvantssolvants industriels, antigel et pesticidespesticides.
Utilisation de l'éthylène en agriculture
L'éthylène joue également un rôle significatif dans l'agricultureagriculture. En tant qu'hormone végétalehormone végétale, il régule diverses fonctions physiologiques chez les plantes, comme la maturation des fruits, la floraison et l'ouverture des fleurs. L'utilisation contrôlée d'éthylène peut accélérer la maturation de certains fruits pour rendre leur récolte et leur commercialisation plus efficaces. Cependant, une gestion prudente est nécessaire pour éviter des maturations prématurées ou inégales.
Challenges et innovations environnementales dans la production d'éthylène
La production d'éthylène est énergivore et associée à d'importantes émissionsémissions de dioxyde de carbonedioxyde de carbone. Face à cela, l'industrie chimique explore des méthodes plus durables pour produire de l'éthylène, y compris à partir de sources biosourcées comme la biomassebiomasse. Les innovations technologiques cherchant à améliorer l'efficacité énergétique du processus de craquage thermique sont également à l'étude. Cela comprend l'utilisation de techniques avancées de capture et de stockage du carbone pour réduire l'impact environnemental associé à la production d'éthylène.
Éthylène et recherche scientifique
La recherche continue d'élargir notre compréhension et notre utilisation de l'éthylène. Des études récentes, accessibles sur des plateformes de prépublication comme recherche sur l'éthylène à arXiv, explorent de nouvelles applications de l'éthylène et de ses dérivés dans des domaines comme les matériaux avancés, la médecine et l'énergie renouvelableénergie renouvelable. Ces efforts de recherche visent non seulement à améliorer les applications existantes mais aussi à révolutionner la manière dont nous utilisons ce gaz vital.