au sommaire
Un acide de Lewis, tel que défini en 1923 par le chimiste américain Gilbert Newton Lewis, est un composé susceptible d'accepter un doublet d'électrons et qui possède une lacune électronique sur sa couche de valence (couche périphérique). Dans la moléculemolécule de triofluorure de borebore, par exemple, la couche de valence du bore comporte trois électrons, liés chacun à un atomeatome d'hydrogènehydrogène. Il reste donc une place libre pour un doublet supplémentaire. Un acide de Lewis peut être un ionion (H+, Li+, Al3+...) ou une molécule neutre (BF3, Br2, AlCl3...).
La définition d’acide de Lewis est plus inclusive que celle de l'acide de Brønsted, qui qualifie un composé susceptible de libérer un ion H+. La définition de Lewis explique donc le comportement acide de certaines substances non considérées comme acides au sens de Brønsted. Les deux acides ont cependant en commun la capacité à abaisser le niveau de pH d'une solution aqueusesolution aqueuse.
Exemples d’acides de Lewis :
- triofluorure de bore (BF3) ;
- borane (BH3) ;
- chlorure d'aluminiumaluminium (AlCl3) ;
- fluorure d'aluminium (AlF3) ;
- chlorure de zinczinc (ZnCl2) ;
- dibrome (Br2).
Rôle des acides de Lewis en chimie organique
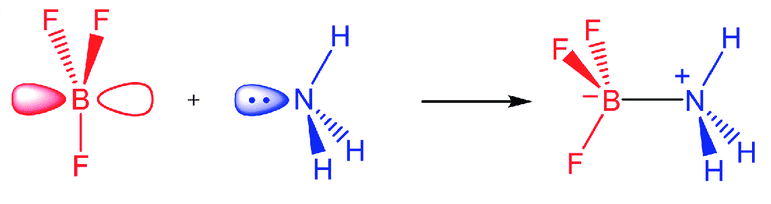
Un acide de Lewis s'associe avec une base de Lewisbase de Lewis par une liaison covalenteliaison covalente (partage de deux électrons entre deux atomes). La réaction entre un acide et une base de Lewis produit un composé appelé adduitadduit de Lewis. Cette réaction est nommée réaction de complexationréaction de complexation.
Les acides de Lewis sont des catalyseurscatalyseurs très puissants dans les réactions organiques. Ils sont par exemple utilisés en grande quantité dans les réactions d'acylation ou d'alkylation de Friedel-Crafts.