au sommaire

De gauche à droite, les physiciens et chimistes britanniques William Henry Bragg (1862-1942) et son fils William Lawrence Bragg (1890-1971). Ils ont reçu le prix Nobel de physique en 1915. William Lawrence Bragg, le plus jeune prix Nobel de physique, a découvert une relation (la loi de Bragg) qui, à partir d’un diagramme de diffraction de rayons X, permet de connaître les distances entre plans atomiques à l’intérieur d’un cristal. © Nobel Media AB 2014
Vingt-huit prix Nobel ont été décernés pour des travaux en rapport avec la cristallographiecristallographie. Les premières récompenses furent décernées aux pionniers du domaine : le physicienphysicien allemand Max von Laue en 1914 (il avait montré en 1912 que les cristaux pouvaient diffracter des rayons X) et, en 1915, les Bragg père et fils, lesquels ont montré comment utiliser les travaux de leur prédécesseur pour déterminer la structure du diamant et du chlorure de sodium.
Ces réussites ont ouvert de nouvelles voies qui ont conduit à bien des découvertes, comme celles des structures d'enzymes et de l'ADNADN. Il n'est donc pas surprenant que les Nations unies aient décrété 2014 Année internationale de la cristallographie.
Une introduction à la cristallographie aux rayons X. © The Royal Institution, YouTube
La diffraction des rayons X reste limitée aux cristaux
Des physiciens, biologistes et chimistes, parmi lesquels on peut citer John Bernal, Linus PaulingLinus Pauling, Max Perutz, Dorothy Hodgkin et Aaron Klug, vont s'intéresser dès les années 1930 à la détermination de la structure de certaines molécules organiques, notamment des protéinesprotéines et des vitaminesvitamines, à l'aide des techniques de diffractiondiffraction des rayons X. Ces travaux vont culminer en 1953 avec la découverte de la structure de l'hémoglobine, pour laquelle Max Perutz et John Kendrew décrocheront le prix Nobel de chimiechimie en 1962, et avec celle de l'ADN par Crick et Watson, grâce à un cliché de diffraction obtenu par la biologiste britannique Rosalind Franklin.
De nos jours, la détermination de la structure des molécules biologiques par diffraction de rayons X reste un domaine très actif, car il permet la mise au point de médicaments de toute sorte. L'une des stratégies utilisées pour comprendre notamment la structure des protéines est de les étudier sous forme cristallisée. Mais cette étude s'effectuant in vitroin vitro, on ne peut pas être sûr de la structure réelle de ces protéines quand elles sont encore à l'intérieur de cellules vivantes, prêtes à participer à des réactions biochimiques.
Pour éliminer ce biais, les chercheurs ont donc cherché à mettre au point une technique de diffraction des rayons X qui permettrait de faire des mesures in vivoin vivo. Dans ce but, ils se sont tournés vers les laserslasers à rayons X en développement depuis un certain nombre d'années. Un article publié dans Pnas fait état d'une première réussite en ce sens avec le laser de la Linac Coherent Light Source du célèbre SLACSLAC en Californie.
Un panorama des applications de la cristallographie aux rayons X. Elles vont de la résistance des alliages aux médicaments. © Unesco TV (français), YouTube
Une protéine épiée aux rayons X dans une bactérie
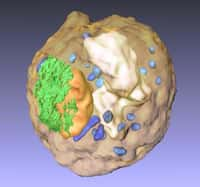
L'équipe internationale de chercheurs qui a utilisé le laser du LCLS s'est intéressée à une bactériebactérie très connue du nom de Bacillus thuringiensisBacillus thuringiensis (Bt), vivant un peu partout dans les sols et l'eau. Elle a la particularité de synthétiser et d'excréter une protéine sous forme cristallisée qui est toxique pour les insectesinsectes. Des cristaux protéiques sont présents dans la bactérie elle-même. Des expériences ont donc été réalisées pour déterminer la structure de ces cristaux à l'intérieur des cellules. Pour cela, une solution contenant des bactéries Bt a été soumise à des impulsions laser et plus de 30.000 figures de diffraction des rayons X ont été obtenues. Elles ont été traitées par ordinateurordinateur avec les outils mathématiques de l'analyse de Fourier, ce qui a permis de reconstituer la structure des protéines en 3D.
Stratégie victorieuse avec à la clé la première détermination de la structure d'une protéine in vivo. Les résultats de l'expérience ont montré qu'au moins dans ce cas précis, il n'y avait pas de différence entre la structure de la protéine in vivo et in vitro. Il semble donc que l'on soit bel et bien parvenu à construire un nouvel outil pour comprendre ce qui se passe à l'intérieur des cellules vivantes.