au sommaire
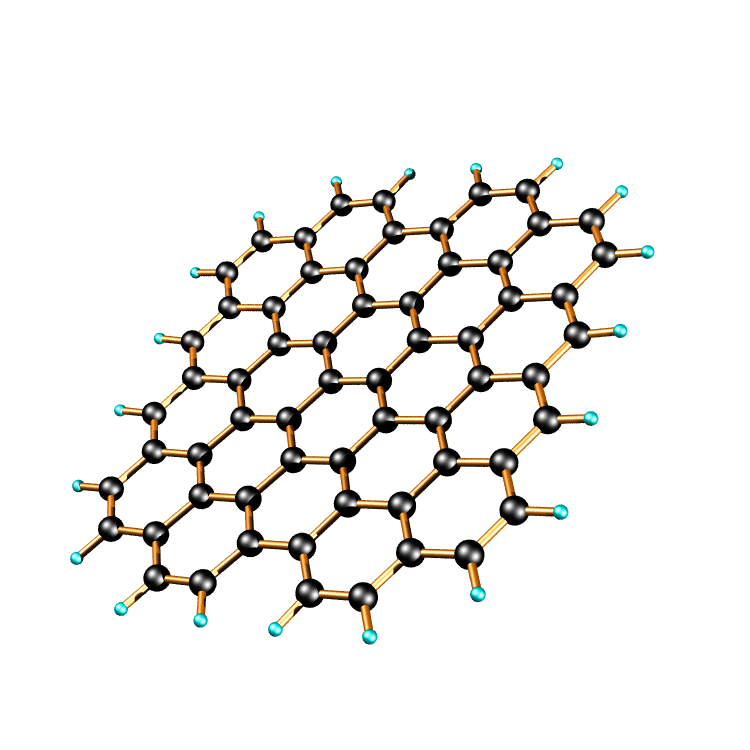
La structure d'un feuillet de graphène avec ses atomes de carbone. Crédit : Chris Ewels
L'arrivée du graphènegraphène sur la scène de la nanotechnologienanotechnologie est récente et ses nombreuses propriétés physiques sont si prometteuses qu'il fait l'objet de nombreuses recherches dans le monde. Ce n'est pourtant qu'une simple couche d'épaisseur atomique dont les empilements constituent le graphite de nos mines de crayon. Les applications qu'on lui prête sont variées, de la nanoélectronique à la la réalisation de cellules solaires plus efficaces en passant par l'augmentation de la résistancerésistance des matériaux. Ses propriétés, souvent, surprennent, comme un effet Hall quantique à température ambiante. On parle même de futurs ordinateurs qui utiliseraient le graphène.
Malheureusement, sa production ne peut être réalisée qu'à des coûts exorbitants. En 2008, il aurait fallu dépenser près de cent millions d'euros pour en obtenir un seul centimètre carré ! Le prix a depuis été divisé par 100.000 mais, clairement, du chemin reste à faire.
Depuis quelque temps, les chercheurs se penchant sur le problème de la production du graphène étudient l'oxyde de graphite. Sa structure en couche est identique à celle du graphite mais avec des distances plus grandes entre les couches. Voilà environ 150 ans que les chimistes et les physiciensphysiciens étudient ce matériau, mais il est encore loin d'avoir livré tous ses secrets.
On sait par exemple qu'il peut incorporer différents solvants entre ses couches mais, lors des études avec insertion de moléculesmolécules d'eau à hautes pressionspressions, on a découvert avec étonnement que l'oxyde de graphite ainsi modifié se dilatait avec l'augmentation de la pression !
Curieux mécanismes à l'échelle moléculaire
Le même phénomène vient d'être constaté par des chercheurs de l'Université Umelå en Suède à l'aide d'une enclume de diamantsdiamants après l'ajout d'alcoolsalcools, comme l'éthanol et le méthanol.
Alors que les molécules d'eau s'insérent de façon graduelle, les alcools, eux, le font en une seule étape. De façon étonnante, avec un mélange d'alcool et d'eau, cette dernière reste même liquideliquide entre les couches de l'oxyde de graphite, comme l'a montré la diffraction des rayons X.
Ce genre d'étude devrait permettre de mieux comprendre la structure de l'oxyde de graphite et par quels mécanismes il se convertit en feuillets de graphène lorsqu'on le chauffe modérément, lors de sa dispersion en solution et même sous l'action de la lumièrelumière d'un simple flashflash d'appareil photographique.