Selon le Comité scientifique des Nations unies sur les effets des radiations atomiques (UNSCEAR), les rayonnements naturels du Soleil et de la Terre transmettent à chaque individu environ 2,4 milli-Siever (mSv) par an. Les activités humaines nous exposent à une dose supplémentaire de radiations, en particulier les techniques de pointe de diagnosticdiagnostic médical non invasifinvasif (radiographieradiographie, CT-scanner) de plus en plus répandues dans les pays industrialisés. L'UNSCEAR estime à environ 1,2 mSv/an la dose individuelle moyenne reçue dans ce cadre.

Deux techniques médicales de pointe soumettant les patients à des radiations à faible dose. La fluorescence par hybridation in situ permet l'observation de chromosomes et est notamment utilisée pour étudier l'instabilité chromosomique lors de diagnostics prénatals © Vigouroux/CEA
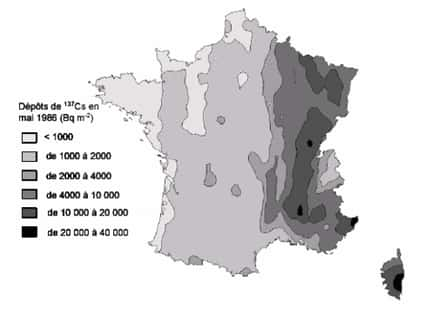
Quant aux impacts actuels de Tchernobyl, des essais nucléaires atmosphériques et de la production d'électricité par les centrales nucléairescentrales nucléaires, ils ne représentent plus que des proportions infimes, respectivement de 0,002, 0,005 et 0,0002 mSv. Toutes ces radiations sont donc peu élevées par rapport au seuil d'environ 100 mSv en deçà duquel elles n'ont pas d'effets cancérogènescancérogènes établis.
Environnement, activité, héritage…

Et la caméra TEP permet de reconstituer une image 3D de l'organe étudié. Cette technique est utilisée pour pratiquer des examens neurologiques, cardiaques et oncologiques.© L.Medard/CEA
Les effets biologiques des multiples expositions à faibles doses représentent cependant un no man's land car il n'est pas possible d'en connaître les conséquences directes sur la santé. Ceux-ci sont trop faibles pour être dégagés du bruit de fond constitué par le pourcentage important de cancerscancers. En revanche, certaines populations sont plus exposées que d'autres selon leur lieu d'habitation (divers terrains de type granitique ont une concentration naturelle en substances radioactives jusqu'à 100 fois supérieure à la moyenne) ou selon leur activité professionnelle. Les travailleurs du nucléaire, les chercheurs en laboratoire, le personnel navigant des compagnies aériennes, à plus forte raison les astronautes, les professions médicales et d'autres métiers reçoivent des doses de radiations plus élevées. Les scientifiques ont également constaté que la sensibilité de l'organisme face aux radiations diffère selon les individus, au même titre que la sensibilité aux UVUV solaires. Ces différences pourraient provenir d'une configuration particulière de certains gènesgènes prédisposant au développement de cancers radio-induits.
a

C'est dans cette installation prototype qu'a été mis au point le procédé de retraitement des combustibles usés par colonnes pulsées encore en cours à La Hague (FR). On assiste ici au contrôle radiologique de l'extérieur de ces colonnes, après assainissement et avant démontage.
© L.Medard/CEA
Les hypothèses formulées par les scientifiques se heurtent à un obstacle : on comprend mal les liens entre les effets précoces des radiations - provoquant des dommages sur les brins d'ADNADN - et les effets à long terme - le développement de cancers, qui est un processus complexe et long. Ce chaînon manquantchaînon manquant de connaissance est l'objet des recherches du projet intégré européen Risc-Rad.
Selon Laure Sabatier, coordinatrice du projet, "il est nécessaire de comprendre en profondeur les mécanismes de la cancérogenèsecancérogenèse radio-induite pour arriver à faire la part de la variation individuelle dans la réponse de l'organisme aux radiations."
Si cette variation joue un rôle marginal dans le cas d'irradiation forte, elle pourrait être déterminante dans la réponse liée aux faibles doses et doit être prise en compte pour quantifier le risque associé. Cette approche pourrait, à terme, suppléer aux limites des études épidémiologiques sur lesquelles sont basées les normes de radioprotection actuelles.
Margot Tirmarche, de l'Institut de radioprotection et de sûreté nucléaire français, a participé, quant à elle, à une vaste étude épidémiologique menée par le Centre international sur le cancer auprès des travailleurs du nucléaire, publiée en juin dernier dans le British Medical Journal. Elle explique que "les résultats de cette étude, menée sur une population dont on connaît avec précision les doses reçues, montrent une relation de proportionnalité entre le cumul de doses et l'augmentation du risque. Des facteurs génétiquesgénétiques sont certes pris en compte quand on étudie la courbe de distribution dose/effet dans une étude épidémiologique, mais ils sont mêlés à l'exposition à d'autres agents toxiques. Les spécialistes de la biologie moléculairebiologie moléculaire ne sont pas, à l'heure actuelle, en mesure de nous dire quels facteurs génétiques il faut isoler."
Le challenge de Risc-Rad est de combler ce manque et d'identifier les gènes candidats jouant un rôle dans la susceptibilité à développer un cancer radio-induit et de tester leur validité sur des modèles animaux. "Une fois qu'on aura trouvé ces gènes, on pourra chercher, dans la population, les polymorphismes correspondants, c'est-à-dire les différentes variantes de ces gènes",
précise Laure Sabatier.
Melting-pot disciplinaire
Cet objectif ambitieux nécessite de faire travailler ensemble des scientifiques de spécialités et de cultures différentes : des radiobiologistes espagnols, des cancérologuescancérologues italiens, des modélisateurs allemands, etc. La qualité du pilotage du projet devient une question cruciale pour sa réussite, au même titre que la qualité scientifique des équipes. "En tant que projet intégré, Risc-Rad se particularise par sa taille et la diversité des sujets qui sont étudiés. Il comprend également une part de flexibilité. Ses objectifs et sa stratégie sont discutés tous les ans lors de la définition du nouveau plan de mise en oeuvr