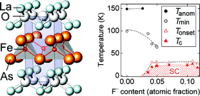
au sommaire
« Nous avons atteint le graal de la physique des hautes pressions. Nous avons produit un matériau qui n'avait encore jamais été produit sur Terre auparavant : de l'hydrogène métallique ! » C'est ce qu'annonce Isaac Silvera, professeur à Harvard, dans une vidéo publiée récemment sur le site de l'université américaine. Cette annonce repose sur une étude parue dans le très sérieux magazine Science, mais, déjà, quelques spécialistes émettent des doutes quant aux résultats affichés.
L'hydrogène n'est pas un élément exotiqueexotique. Loin de là. Il est à la fois l'élément le plus simple et le plus abondant de notre univers. Habituellement -- dans des conditions normales de température et de pressionconditions normales de température et de pression, diront les physiciensphysiciens --, nous le rencontrons sous sa forme gazeuse. Toutefois, comme tous les éléments, il peut subir des transitions de phase. Ainsi, refroidissez l'hydrogène à quelque 20 K (soit environ -250 °C) et voilà qu'il devient liquideliquide ; juste en dessous de 14 K (-259 °C), il se solidifie.
Rappelons par ailleurs que l'hydrogène se rencontre classiquement sous une forme moléculaire, le dihydrogène (H2). Pourtant, en 1935, des physiciens prédisent que, soumises à de fortes pressions, les moléculesmolécules de dihydrogène pourraient être amenées à se dissocier pour former de l'hydrogène atomique présentant les propriétés d’un métal. Toutefois, jusqu'à l'annonce du professeur Isaac Silvera, on pensait ces pressions hors d'atteinte. Du moins en laboratoire.
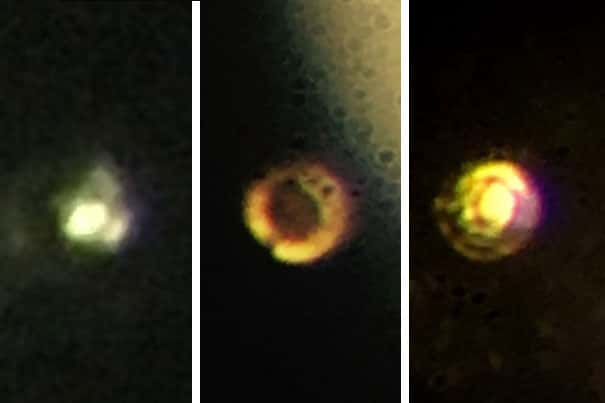
Ici, trois stades de la formation de l’hydrogène métallique. À gauche, un hydrogène moléculaire transparent et isolant, à une pression de 200 gigapascals (GPa). Au centre, un hydrogène moléculaire noir et semi-conducteur. Enfin, à droite, un hydrogène métallique atomique supraconducteur à une pression de 495 GPa. © Isaac Silvera, Harvard
Une expérience sujette à polémiques
L'équipe de Harvard serait donc parvenue à faire peser sur un minuscule échantillon d'hydrogène, une pression de quelque 495 gigapascals. Une pression supérieure à celle régnant au centre de la Terre, qui avoisine les 350 gigapascals. Comment ? À l'aide d'un dispositif baptisé « cellule à enclumes de diamantdiamant » (ou « presse à enclumes de diamant »). Ce dispositif a été inventé à la fin des années 1950. Toutefois, ici, les diamants utilisés étaient des diamants synthétiques polis à la poudre de diamant et cinq petits micronsmicrons de leur surface ont ensuite été rasés par gravuregravure ionique réactive de manière à les rendre encore plus résistants, une condition indispensable à l'obtention de pressions aussi élevées que celles annoncées. Enfin, ils ont été recouverts d'une fine couche d'aluminealumine. De quoi éviter, en principe, la diffusiondiffusion de l'hydrogène dans la structure cristalline des diamants.
Cependant, quelques heures seulement après l'annonce d'Isaac Silvera, des experts de divers pays (du CEA en France, de l'Institut Max PlanckMax Planck en Allemagne, de l'université de Washington aux États-Unis, de l'université d'Édimbourg en Écosse, etc.) ont remis en cause les résultats publiés. Selon eux, la pression atteinte aurait pu être surestimée -- par des mesures peu précises ou des extrapolations mal justifiées --, remettant en cause la possibilité de créer de l'hydrogène métallique. De plus, les observations visuelles d'un matériau brillant -- qui correspondrait au fameux hydrogène métallique -- pourraient n'être que celles du revêtement d'alumine qui se serait transformé sous la pression.

L’hydrogène métallique pourrait être utilisé comme carburant très efficace de propulseurs plus puissants qu’à ce jour. Il jouerait alors un rôle clé dans l’exploration de l’espace lointain. © Nasa-Imagery, Pixabay, DP
Des applications extraordinaires
Pourquoi y a-t-il tant de réactions autour de cet hydrogène métallique ? Parce que ces travaux -- s'ils peuvent être reproduits -- revêtent une importance particulière en matièrematière de physique fondamentale. Isaac Silvera leur promet également une foule d'applicationsapplications très pratiques, qui pourraient, entre autres, révolutionner notre système énergétique.
L'hydrogène métallique, en effet, est réputé pour être « métastablemétastable ». Afin de bien comprendre ce terme, prenons l'image du diamant. Celui-ci se forme à partir de graphitegraphite soumis à des températures et des pressions extrêmes. Lorsque les conditions se relâchent, le diamant ne revient pas à l'état de graphite. Il demeure dans cet état, qualifié alors de métastable. Dans la théorie, il en irait de même pour l'hydrogène métallique. Sachant que la théorie l'annonce supraconducteursupraconducteur, nous tiendrions enfin là un supraconducteur à température ambiante !