Certains physiciensphysiciens se passionnent pour les mystères des particules élémentaires ou de l'espace-temps, d'autres pour la physique des fluides et des plasmas et d'autres encore, comme le regretté Pierre-Gilles de Gennes, pour la physique des solides ou de la « matière molle » comme le prix Nobel aimait à l'appeler. Dans ce domaine, les superfluidessuperfluides et les supraconducteurssupraconducteurs font rêver mais la physique de l'eau et de la glace peut elle aussi se révéler étonnante, comme le prouvent par exemple les travaux récents montrant qu'à température et pressionpression ambiante, l'eau est en fait composée de deux liquides.
L'aventure continue : dans un article de la revue The Journal of Chemical Physics, un groupe de chercheurs japonais prédit l'existence d'une nouvelle phase de glace pouvant être ultralégère. Il ne s'agit pour le moment que de travaux théoriques basés sur des méthodes de dynamique moléculaire pour des simulations sur ordinateurordinateur. Elles permettent d'explorer les propriétés d'un solide dans des conditions physiques extrêmes et inatteignables en laboratoire à partir des forces liantliant les atomesatomes ou les moléculesmolécules.
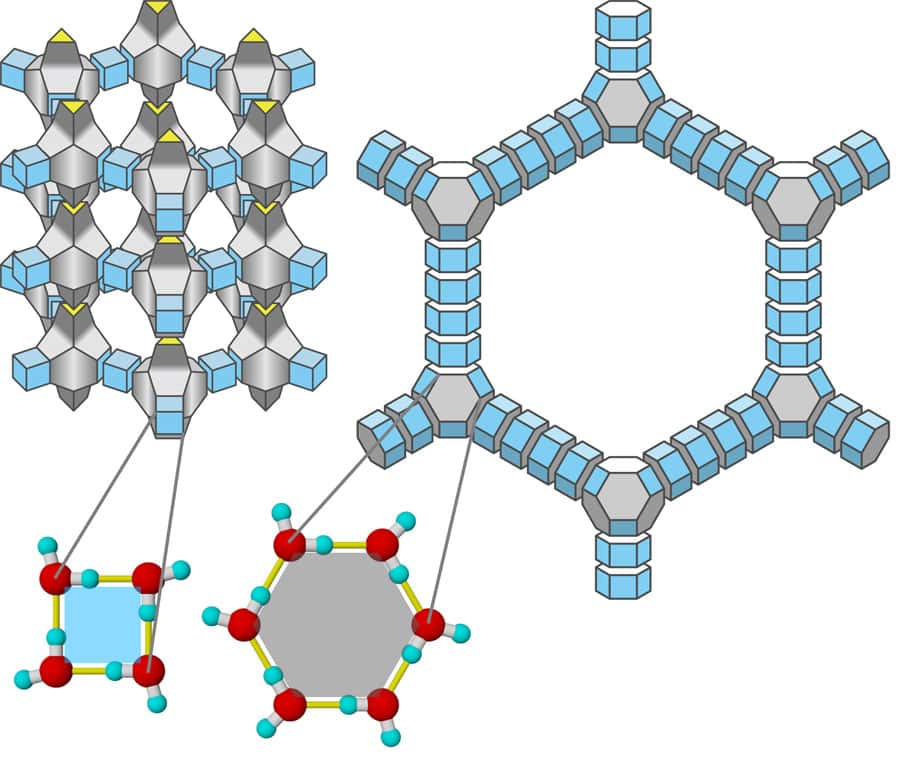
Sur ce schéma, les molécules d'eau (en rouge les atomes d'oxygène, en bleu l'hydrogène) forment une structure de type zéolite. © Masakazu Matsumoto, CC BY 2.0
Dans le cas présent, les chercheurs se sont intéressés aux phases de la glace pour lesquelles tout se passe comme si elle était soumise à des pressions négatives, donc, en quelque sorte, à des forces qui la dilateraient de l'extérieur. De telles pressions négatives sont possibles au sein des liquidesliquides et des solides, mais pas des gazgaz. Elles sont réalisées en étirant le matériaumatériau, qui devient métastablemétastable par rapport au passage à l'état de vapeur, la nucléationnucléation des bulles de gaz nécessitant de l'énergieénergie pour franchir une barrière d'activation. Le matériau à pression négative peut donc rester intact durant de longues périodes jusqu'à ce que cette barrière d'activation soit surmontée.
Les aéroglaces, des sources d'inspiration pour la nanotechnologie
Actuellement, 17 phases de glace sont connues et seulement deux sont plus légères que la glace dans les conditions standards, à savoir les glaces XVI et XVII qui ont été synthétisées ces dernières années. Elles résultent de la formation d'une structure cristalline en trois dimensions qui est celle de la zéolitezéolite, un minéralminéral cristallisé formé d'un squelette microporeuxmicroporeux d'aluminosilicate, dont les espaces vides connexesconnexes sont initialement occupés par des cationscations et des molécules d'eau.
Au départ, les physiciens ont cherché à obtenir une nouvelle glace en s'inspirant de la zéolite car on connaît des centaines de zéolites construites à partir d'assemblages de SiO2. Environ 300 structures de ce type ont été explorées sur ordinateur, dans lesquelles un siliciumsilicium est remplacé par un atome d'oxygèneoxygène, et ceux d'oxygène par des atomes d'hydrogènehydrogène. L'ordinateur a découvert l'existence de plusieurs glaces nouvelles dont les densités sont comprises entre 0 et 0,5 g/cm3.
Ces glaces ultralégères ont reçu le nom d'aéroglace, par analogieanalogie avec les aérogels qui sont aussi remarquablement peu denses. Selon les chercheurs, cette découverte devrait permettre de mieux comprendre les propriétés fondamentales et le comportement de l'eau dans les nanotubes.
Ce qu’il faut
retenir
- Charbon et diamant sont tous deux faits d'atomes de carbone mais forment pourtant des phases différant par l'organisation dans l'espace des atomes et de leurs liaisons. De même, plusieurs phases de glace sont possibles selon la pression et la température.
- On peut modéliser des phases de glace dans des conditions extrêmes, par exemple avec des pressions négatives. Ces modélisations prédisent l'existence de glaces dont les densités sont comprises entre 0 et 0,5 g/cm3. Elles sont baptisées aéroglaces par analogie avec les aérogels.