au sommaire
Lorsque la conquête spatiale a vraiment commencé après la seconde guerre mondiale, on s'attendait à trouver des molécules organiques à la surface des planètes comme Mars, ou des satellites comme la Lune, mais certainement pas dans l'environnement froid et hostile du milieu interstellaire. On savait de plus qu'il est parcouru par des rayons cosmiques très énergétiques, dont certains sont même des particules d'antimatière. La chimie du milieu interstellaire se devait d'être pauvre, et des molécules organiques ne devaient pas y survivre longtemps.
Et pourtant, dès 1941, on a commencé à détecter des molécules organiques dans le milieu interstellaire : HC, HC+ et CN. Ces molécules y ont été découvertes grâce à leurs raies (observées en absorptionabsorption dans le domaine visible) dans le spectrespectre de l'étoileétoile Zeta Ophiuchi. Rapidement, l'ouverture de la fenêtrefenêtre des ondes centimétriques et décimétriques en radioastronomie permettra la découverte du radical hydroxyle HO (en 1963) et des premières molécules polyatomiques : l'ammoniacammoniac NH3 (en 1968), l'eau H2O et le formaldéhydeformaldéhyde H2CO (en 1969). Mais c'est l'accès à la fenêtre observationnelle des ondes millimétriques et submillimétriques, à partir des années 1970, qui a permis de découvrir la plupart des molécules interstellaires. Plus de 150 sont connues à ce jour.
Molécules synthétisées dans la glace cosmique
De prime abord, l'existence de ces molécules était paradoxale, car on les trouvait dans des nuagesnuages à de très basses températures et dans des conditions de vide très poussé. Dans de telles conditions, les réactions chimiques sont en principe très lentes, voire impossibles. On a fini par comprendre qu'elles peuvent tout de même avoir lieu en phase gazeuse dans un ultravide et à des températures de l'ordre de 10 K, soit environ -263 °C. Autre découverte, elles peuvent se dérouler dans le manteaumanteau de glace amorpheamorphe recouvrant les poussières interstellairespoussières interstellaires présentes dans les nuages moléculaires.
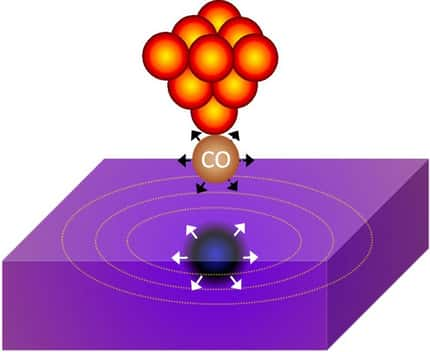
Or, depuis quelque temps, les astrochimistes détectaient dans les nuages moléculaires un cousin du radical hydroxyleradical hydroxyle HO, le radical méthoxyle CH3O. C'est une entité chimique très réactive, mais on avait bien du mal à comprendre comment elle pouvait se former dans le milieu interstellaire. L'hypothèse la plus simple voulait que comme bien d'autres molécules organiques dans l'espace, elle se forme à partir du méthanol dans la gangue de glace des poussières silicatées ou carbonées présentes dans les nuages entourant de jeunes étoiles. Les photonsphotons du rayonnement UVUV de ces étoiles peuvent en effet faire des miracles quand ils frappent des molécules carbonées simples dans cette gangue de glace que l'on appelle de la glace cosmique.
Malheureusement, les expériences conduites en laboratoire avec cette glace cosmique ne permettaient pas d'observer la formation de ces radicaux sous l'action des rayons UV. Et ce bien que l'on ait reproduit les conditions du milieu interstellaire.

Le physicien George Gamow a été le premier à comprendre que les ondes de matière quantique pouvaient traverser des barrières d'énergie interdisant classiquement des réactions nucléaires et chimiques. Il a ainsi découvert l'effet tunnel. © AIP, Emilio Segre, Visual Archives
Accélération quantique foudroyante des réactions chimiques
Des chercheurs de l'université de Leeds viennent toutefois de trouver la clé de l'énigme. Comme ils l'expliquent dans un article publié dans Nature Chemistry, cette clé n'est autre que l'effet tunneleffet tunnel. Rappelons que l'effet tunnel a tout d'abord été découvert théoriquement par George GamowGeorge Gamow en 1928 lors de ses recherches sur la physiquephysique nucléaire. Le génial futur père de la théorie du Big Bang, avec Georges LemaîtreGeorges Lemaître, s'était servi de la toute jeune mécanique ondulatoiremécanique ondulatoire de Schrödinger pour montrer qu'une particule alpha ne pouvait pas rester confinée dans un noyau, mais avait une chance non négligeable de s'en échapper. Ses calculs permirent d'expliquer quantitativement plusieurs aspects de la radioactivitéradioactivité alpha. Plus tard, on s'est rendu compte que cet effet intervenait dans nombre de phénomènes en chimie quantique et en physique du solidesolide.
Dans le cas présent, les chercheurs avaient supposé que pour un mélange gazeux très froid et très dilué de méthanol et de radical hydroxyle HO, ce que l'on appelle un intermédiaire réactionnel pouvait exister relativement longtemps dans l'espace. Ce faisant, une barrière d'énergieénergie (interdisant normalement, ou pour le moins défavorisant nettement, une réaction entre ces deux entités pour donner un radical méthoxyle) pouvait tout de même être franchie par effet tunnel.
Les astrochimistes ont reproduit ce mélange dans les conditions régnant dans des nuages moléculaires à environ 63 K. Le résultat a été spectaculaire. Non seulement le radical se formait bien, mais la vitessevitesse de la réaction était 50 fois plus élevée qu'à température ambiante. Pour les chercheurs, cela implique que tout un pan de la chimie interstellaire faisant intervenir des alcoolsalcools reste à découvrir, et que l'on a sévèrement sous-estimé la vitesse des réactions à basse température dans les nuages moléculaires.