au sommaire
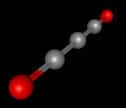
La molécule C3O2 est de forme linéaire et les cinq atomes rangés dans l'ordre OCCCO, sont reliés par des doubles liaisons.Crédit : http://www.chem.ox.ac.uk
Par ailleurs, à l'aide de leur méthode basée sur la mesure de la dispersion de rayons X par une solution, ils ont montré que le polymère contient environ 40 monomèresmonomères de sous-oxyde de carbone. L'énigme qui planait sur la structure et la taille de ce polymère est enfin levée.
A coté des bien connus monoxyde et dioxyde de carbonedioxyde de carbone, l'oxygène et le carbone peuvent former d'autres moléculesmolécules, dont le sous-oxyde C3O2 est l'une des plus stables. Cette molécule, qui constitue une substance gazeuse, a été découverte en 1906. Elle est de forme linéaire et les cinq atomesatomes rangés dans l'ordre OCCCO, sont reliés par des doubles liaisons. Le sous-oxyde de carbone réagit spontanément et se transforme en un polymère solidesolide, une molécule géante, composée d'un grand nombre de monomères C3O2. Combien est-ce qu'une molécule de polymère contient-elle d'unité de C3O2, et de quelle manière sont-elles agencées entre-elles, restaient des questions sans réponse à ce jour.