La découverte en 1985 de la célèbre molécule en forme de ballon de football appelée buckminsterfullerène (ce nom lui a été donné en hommage à l'architectearchitecte états-unien pionnier des dômes géodésiques Richard Buckminster Fuller) peut rétrospectivement être vue comme la pointe émergée d'une révolution à venir, celle des feuillets de graphène et des nanotubes de carbone. En sera-t-il de même avec la variante de la mythique molécule de C60 qu'un groupe de chercheurs états-uniens et chinois annoncent avoir découvert dans un article de la revue Nature Chemistry ?
Difficile de le dire. Il s'agit en tout cas d'une sorte de cage moléculaire formée de 40 atomes de bore. Les physiciensphysiciens suspectaient son existence depuis un certain temps et, en fait, l'avaient même prédit théoriquement. Lai-Sheng Wang, professeur de chimiechimie à l'université de Brown, et ses collègues sont des spécialistes de la chimie du bore. Il se trouve que celui-ci fait partie de la même période que le carbone dans le tableau de Mendeleïev. Le bore présente donc le même nombre de couches électroniquescouches électroniques que l'atome de carbone mais il possède un électronélectron de moins. Les chimistes en avaient déduit qu'en raison de cette proximité avec les atomes de carbone, il existait peut-être des analogues des feuillets de graphènegraphène et donc, aussi des fullerènesfullerènes. Des simulations sur ordinateursordinateurs avaient convaincue Lai-Sheng Wang et ses collègues que cela devait être le cas. Le borophène était probablement à portée de mains si l'on s'y prenait convenablement...

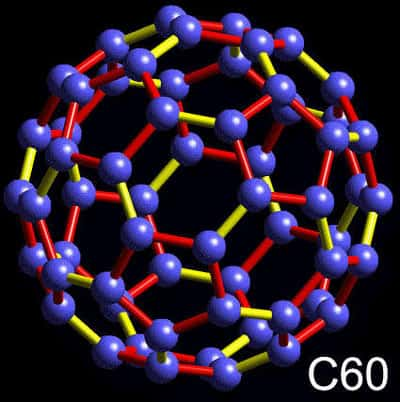
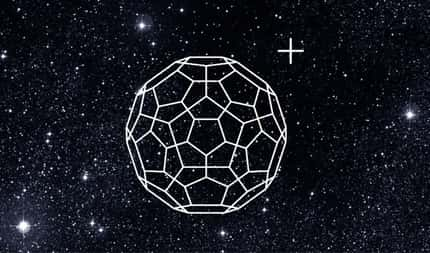
Le borosphèrène est constitué de nombreux triangles. Bien que sa forme soit approximativement sphérique il n'est pas aussi lisse que son cousin en carbone le buckminsterfullerène. © Brown University
Des molécules pour stocker de l’hydrogène ?
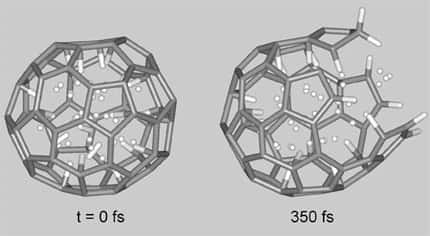
Des résultats encourageants ont bel et bien été obtenus avec la synthèse de disques contenant 36 atomes de bore. Mais en continuant à explorer sur ordinateur le monde des molécules formées uniquement de bore à l'aide des équationséquations de la chimie quantique, les chercheurs se sont aperçus qu'il existait théoriquement des constructionsconstructions particulièrement stables formées de 40 atomes. En examinant environ 10.000 configurations atomiques différentes, l'ordinateur a fini par livrer l'existence de deux structures. L'une quasiplane et l'autre de forme sphérique. Mieux, il pouvait prédire aussi les niveaux d'énergiesénergies des électrons de ces molécules, et donc leurs spectresspectres.
Ne restait plus qu'à vérifier ses prédictions en laboratoire. D'abord, il a fallu synthétiser des molécules en refroidissant, à l'aide de faisceaux d'héliumhélium, un gazgaz d'atomes de bore. Les composés moléculaires obtenus furent ensuite triés en fonction de leurs massesmasses, de sorte que l'on a pu isoler ceux qui contiennent 40 atomes. Il ne restait plus qu'à employer la technique de la spectroscopie de photoémission pour mesurer l'énergie de liaison des électrons. Elle a consisté, dans le cas présent, à mesurer l'énergie des électrons émis par effet photoélectriquephotoélectrique sous l'action d'un laserlaser.
Les résultats expérimentaux se sont révélés en très bon accord avec les prédictions numériquesnumériques tirées de la chimie quantique. Le borosphèrène, ainsi l'ont baptisé les chercheurs, existe bel et bien. Toutefois, on ne sait pas encore quelles applicationsapplications sont possibles avec ce cousin du buckminsterfullerène. Comme lui, le nouveau venu pourrait servir à stocker de l'hydrogènehydrogène pour alimenter les piles à combustible du futur.