au sommaire
- À lire aussi

Le prion, sept ans après
La maladie de la vachevache folle n'apparaît plus aujourd'hui que comme un mauvais souvenir. Mais les questions scientifiques fondamentales posées par le prionprion restent entières. Quels sont, par exemple, les mécanismes qui lui permettent de franchir la barrière d'espèceespèce ? Des études chez le mouton et le poissonpoisson se proposent d'y répondre.
20 mars 1996. Le gouvernement britannique annonce que plusieurs cas d'une nouvelle variante de la maladie de Creutzfeldt-Jakobmaladie de Creutzfeldt-Jakob sont peut-être dus au passage à l'homme de l'encéphalopathie spongiforme bovineencéphalopathie spongiforme bovine (ESB). L'agent infectieux responsable, le prion, fut assez rapidement identifié. Mais la "déviance" maligne permettant à ce mystérieux composant cellulaire - ni virus ni bactériebactérie - de s'attaquer au système nerveux centralsystème nerveux central demeurait une énigme. Par quels mécanismes agissait-il ? Comment avait-il pu se transmettre à l'homme ? Pouvait-il infecter d'autres espèces ? La Commission réunit alors un Groupe européen pour la recherche sur l'ESB, présidé par le biologiste suisse Charles Weissmann, aujourd'hui membre de l'Imperial College de Londres (UK). Un vaste plan d'action fut lancé. Depuis 1996, quatre appels d'offres successifs, s'ajoutant aux programmes généraux, ont permis d'injecter plus de 100 millions d'euros dans ces recherches.

Sept ans après ce coup de tonnerretonnerre, où en est-on ? Suite aux mesures drastiques prises pendant plusieurs années sur le plan agricole et sanitaire, la situation s'est considérablement améliorée. L'épidémieépidémie d'ESB est sous contrôle, et la hantise d'une "épidémie" de nouveaux cas de la nouvelle variante de la maladie de Creutzfeldt-Jakob ne s'est pas confirmée.
- La question de la "barrière"
Sur le plan scientifique, la mobilisation initiée par la Commission s'est articulée autour de cinq priorités : les recherches cliniques et épidémiologiques sur les différentes encéphalopathies spongiformes transmissiblesencéphalopathies spongiformes transmissibles (EST), ou maladies à prion; l'étude de l'agent infectieux et de sa transmission; les méthodes de détection et de diagnosticdiagnostic (appuyées, notamment, par les travaux de validation menés par le Centre Commun de Recherche - voir encadré); l'évaluation des risques et, enfin, le traitement et la préventionprévention de ces maladies. Sur quelque 95 projets de recherche (de la biologie moléculairebiologie moléculaire la plus pointue à la recherche clinique appliquée), certains s'intéressent à une question biologique fort ancienne : celle de la barrière d'espèce.
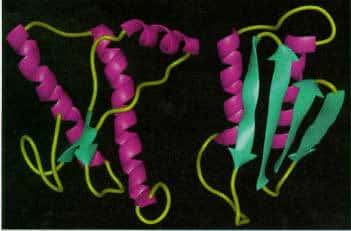
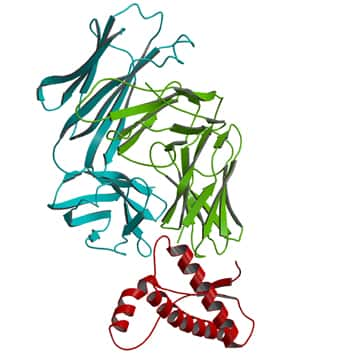
Si le prion défie les biologistes, c'est, en effet, à cause de son étonnante propriété de passer d'une espèce à l'autre. Rappelons qu'une protéineprotéine prion (PrP) existe chez tous les mammifèresmammifères sains, sous des séquences légèrement différentes d'une espèce à l'autre. Pour des raisons mal comprises, la PrP peut changer de conformationconformation et devenir résistante aux enzymes qui la dégradent, d'où son nom de PrPres.
Selon la théorie la plus largement admise, la PrPres est l'agent pathogènepathogène des EST. Injectée dans le cerveaucerveau d'un animal, elle déclenche la maladie et transformerait les PrP en PrPres. Les travaux de Charles Weissmann ont ainsi montré qu'une souris de laboratoiresouris de laboratoire devient résistante à l'injection de PrPres si on la modifie génétiquement pour lui enlever le gènegène codant pour la PrP. Si le gène est rétabli, la PrPres redevient infectieuse.
- Le modèle de la "tremblante"
Et dans la nature ? Que se passe-t-il lorsqu'une protéine prion pathogène entre en contact avec un nouvel hôte, exprimant naturellement une forme différente de la protéine ? La "tremblante du moutontremblante du mouton" - scrapie en anglais -, première EST à avoir été identifiée dès 1938, offre un bon modèle pour répondre à cette question.
Il existerait, en effet, plusieurs souches du prion responsable de cette maladie. De plus, contrairement à ce qui se passe chez les bovins avec l'ESB, la résistancerésistance naturelle des moutons varie et dépend de leur patrimoine héréditaire : certains génotypesgénotypes sont sensibles, d'autres pas. Cette propriété est exploitée par le projet Scrapie free sheep pour sélectionner des troupeaux résistants à la tremblante. Cette double variabilité (souches de prion et résistance de l'hôte) fait de la scrapie un modèle de choix pour l'étude des relations "cause à effet."
Que se passe-t-il, par exemple, si des moutons sont infectés par le prion responsable de l'ESB ? Sera-t-on capable de distinguer les symptômessymptômes de ceux de la tremblante classique ? Les animaux infectés pourront-ils à leur tour transmettre la maladie à leurs congénères ? Les moutons génétiquement résistants à la tremblante seront-ils aussi résistants à l'ESB ? C'est à ces questions (aux importantes répercussions économiques) qu'entend répondre le projet BSE in sheep coordonné par OlivierOlivier Andreoletti de l'Ecole nationale vétérinairevétérinaire de Toulouse (France). "Il s'agit d'être prêt à réagir si on détectait un jour un passage de l'agent de l'ESB au mouton. Nos recherches serviront à nourrir une politique scientifique européenne de gestion de ces risques", explique-t-il.
- Un souci piscicole
Le problème du passage de la barrière d'espèce constitue, en effet, une épée de Damoclès pour nombre de secteurs agronomiques. Exemple : la pisciculturepisciculture. "Tous les poissons d'élevage reçoivent une alimentation qui contient entre 40 et 55 % de protéines. Des protéines animales peuvent être présentes, et donc, potentiellement, des protéines prion pathogènes", fait remarquer Theodoros Sklaviadis de l'Université de Thessalonique (GR).

Les poissons d'élevage reçoivent une alimentation qui peut être composée de protéines animales. Risque d'EST? Des recherches sur le prion sont menées à l'Université de Thessalonique (GR).
En 1997, Carla Bolis, chercheuse à l'Université de MilanMilan (IT) avait, de fait, décelé une protéine prion normale dans le cerveau des saumonssaumons, alors qu'on croyait que celle-ci ne se trouvait que chez les mammifères. D'où l'importance de cerner ce risque d'EST chez les poissons, comme s'emploie à le faire le programme coordonné par le professeur Sklaviadis. Ces travaux se centrent sur deux axes : rechercher systématiquement dans le génomegénome de la truitetruite, du loup de mer et de la brème, les séquences codant pour la protéine prion afin d'analyser ensuite leurs homologieshomologies avec les gènes de mammifères; nourrir ces poissons avec des farines contenant des prions de l'ESB et de la tremblante, pour voir s'il est possible de déclencher ainsi une infection. "Les résultats ne seront pas disponibles avant plusieurs années à cause de la durée d'incubation de la maladie", prévient Theodoros Sklaviadis. La patience est nécessaire, si l'on veut éviter que la pisciculture européenne ne se trouve un jour confrontée à de sérieux problèmes.