au sommaire
Objectifs de l'étude
Un des sujets de recherche du laboratoire concerne l'évaluation et la possibilité d'inhiber l'action oxydante provoquée par la flambée respiratoire chez le granulocytegranulocyte neutrophileneutrophile. Pour cela, diverses molécules à intérêt thérapeutique et ayant une activité antioxydante sont testées pour mesurer la production des espècesespèces réactives de l'oxygène.
Nous nous intéresserons au rôle tenu par la protéineprotéine kinasekinase C lors du stress oxydatifstress oxydatif. Pour cela nous avons mis au point un modèle qui permettra d'évaluer le pouvoir antioxydantantioxydant de molécules inhibitrices de la PKC. Par la suite nous avons testé sur ce modèle des molécules inhibitrices de Rho kinase : le HA-1077 et le Y-32885, puis nous avons évalué le potentiel inhibiteur de molécules originales.
1.5.1. ELABORATION DU MODELE

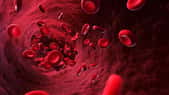
fig. 21 : Un activateur de la protéine kinase C : le phorbol-12-myristate-13-acétate ou PMA.
Dans un premier temps, il faudra mettre en évidence l'activité antioxydante de la molécule testée. Ceci sera fait en pratiquant un dosagedosage de l'anion superoxyde sur des granulocytes neutrophiles préalablement stimulés par un ester de phorbol, le phorbol-12-myristate-13-acétate (fig. 21), ou un stimulant plus physiologique, le fMLP ou N-formyl-méthionyl-leucyl-phénylalaninephénylalanine (fig.22). En effet, le phorbol-12-myristate-13-acétate est un stimulant d'origine chimique qui peut activer la protéine kinase C de façon spécifique en se fixant sur le site de reconnaissance du diacylglycérol ; il déclenche alors une flambée respiratoire importante et durable chez le granulocyte neutrophile (Gschwendt M. et al., 1991).
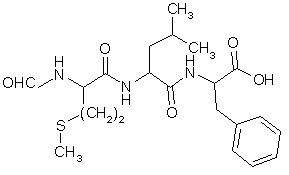
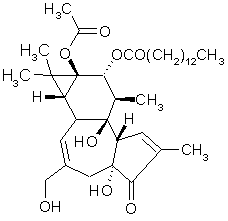
fig. 22 : Le N-formyl-méthionyl-leucyl-phénylalanine ou fMLP
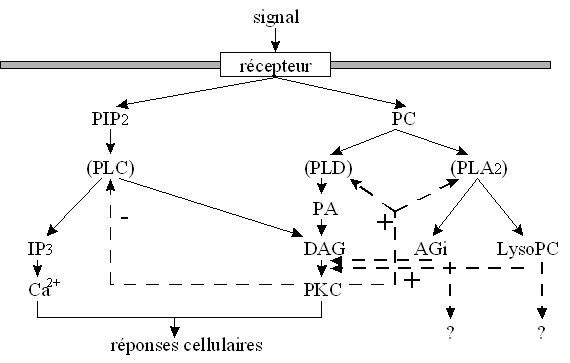
Le fMLP est un peptide bactérien N-formylé mimant un ligand naturel sur certains récepteurs membranaires. La PKC peut être activée par l'intermédiaire de la phospholipase C, mais d'autres enzymesenzymes peuvent être stimulées. Parmi celles-ci, il est possible de noter la protéine kinase A ou les tyrosinestyrosines kinases, la plupart de ces enzymes sont capables de réguler de façon plus ou moins directe l'activité de la NADPH oxydaseoxydase. On peut obtenir le déclenchement de la flambée respiratoire de façon rapide et intense (Uings J.J. et al., 1992).
Afin de confirmer que la molécule testée agit bien sur la PKC, une étude de liaison sera effectuée en utilisant un ligand radiomarqué : le phorbol-12, 13-dibutyrate ou PDB. Cette molécule est un ester de phorbol qui possède le même site de fixation que le PMAPMA. Cette étape est précédée d'une purification de la PKC par chromatographiechromatographie échangeuse d'ionsions.
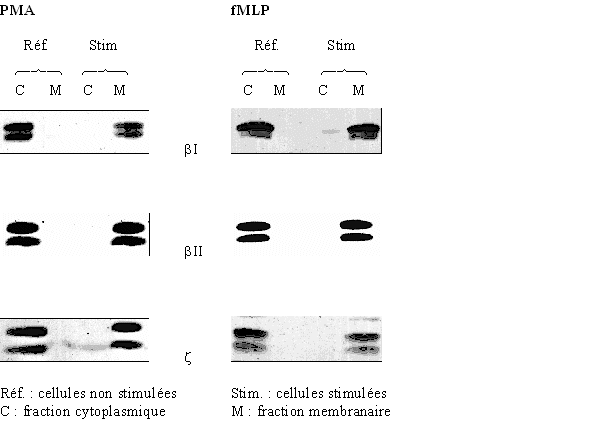
Nous avons vu que lors de son activation, la protéine kinase C est transloquée vers la membrane plasmiquemembrane plasmique. Pour visualiser ce phénomène, une technique de western blotwestern blot est employée. Ceci permettra de confirmer que c'est bien la protéine kinase C qui est impliquée dans les processus étudiés. En outre, nous pourrons également voir si une molécule testée possède une sélectivité vis à vis d'une isoforme de la PKC.
Afin de mettre au point ce modèle, nous avons utilisé un inhibiteur connu : le chlorure de chélérythrine (fig. 23). Cet alcaloïdealcaloïde de benzophénanthridine a été décrit comme inhibiteur naturellement spécifique de la protéine kinase C par rapport aux autres kinases régulièrement décrites. Il se fixe sur le domaine catalytique et plus particulièrement sur le site de liaison du substratsubstrat. Il faut une concentration 200 fois supérieure pour agir sur une autre protéine kinase. La chélérythrine ainsi que d'autres molécules de la même famille (sanguirine, nitidine) ont été utilisées régulièrement pour étudier certains mécanismes liés à la toxicitétoxicité cellulaire. Le couplage de la PKC avec les esters de phorbol est affecté lorsque l'enzyme est incubée avec une concentration en inhibiteur de 20 µM. Cette modification de la reconnaissance pour l'enzyme est due aux modifications conformationnelles provoquées par le chlorure de chélérythrine sur la structure tridimentionnelle de la protéine.
Sur des cellules intactes, la chélérythrine provoque une inactivation irréversible de l'enzyme en méthylant les groupements thiols restés libres des cystéinescystéines. Cela nécessite une incubation d'une heure avec une concentration de 10 à 30 µM, on bloquera alors 70 à 90 % de la réponse cellulaire (Gopalakrishna R. et al., 1995).
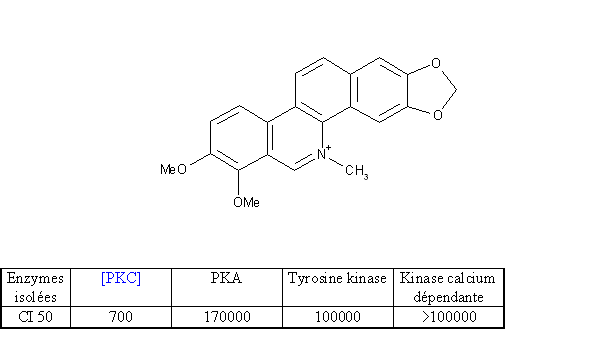
fig. 23 : Un inhibiteur de la protéine kinase C : le chlorure de chélérythrine (CI 50 en µM) (Herbert J.M et al., 1990).
1.5.2. TESTS D'INHIBITEURS POTENTIELS DE LA PROTEINE KINASE C
La famille des kinases est régulièrement étudiée car elle est impliquée dans de nombreux processus cellulaires et voies de transductiontransduction. Un des aspects de ces recherches consiste à trouver des molécules qui pourraient servir soit d'outils pharmacologiques afin de mieux connaître les mécanismes qui régissent ces enzymes, soit des chefs de file comme candidats médicaments. Nous avons testé deux composés qui sont étudiés dans le cadre de recherches sur une Rho kinase.
1.5.2.1. Molécules de références
Le fasudil ou HA-1077 (1-5-(isoquinoline sulfonyl)-homopipérazine HCl) (fig. 24) est un vasodilatateurvasodilatateur au niveau cérébral, en agissant sur la contraction des muscles lissesmuscles lisses sensibles au calciumcalcium. Il a le pouvoir d'inhiber différentes kinases comme la Rho kinase, la protéine kinase A, C, G ou la kinase à chaîne légère de myosine.
Les mécanismes permettant la vasodilatationvasodilatation ne sont pas établis car il semblerait que différentes kinases interviennent dans la régulation de la pressionpression sanguine cérébrale; comme le HA-1077 est capable d'agir sur l'ensemble des kinases, cela rend plus complexe l'interprétation des résultats obtenus (Hara M. et al., 2000, Asano TT. et al., 1987).
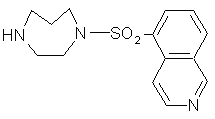
fig. 24 : Structure d'un inhibiteur potentiel de la protéine kinase C : le HA-1077.
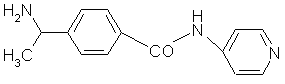
fig. 25 : Structure d'un inhibiteur potentiel de la protéine kinase C : le Y-32885.
Le Y-32885 ou (R)-(+)-N-(4-pyridyl)-4-(-1-aminoéthyl)-benzamide (fig. 25) est également un vasodilatateur, son mode d'action se caractérise par une inhibitioninhibition de la contraction des muscles lisses, ce sont les myofilaments sensibles au calcium qui sont sélectivement atteints. Il inhibe la kinase à chaîne légère de myosine, la Rho kinase, la protéine kinase N et C. (Uehata M. et al., 1997, Amano T. et al., 2000).
1.5.2.2. Molécules originales
Dans le cadre de recherches sur les inhibiteurs de Rho kinase, l'équipe du professeur Daniel Lesieur de l'Institut de ChimieChimie Pharmaceutique Albert Lespagnol (ICPAL) synthétise des molécules pouvant avoir une action sur cette enzyme afin de trouver de nouveaux vasodilatateurs. Nous avons pu tester certains de ces composés sur notre modèle concernant la protéine kinase C. Les formules de ces composés anisi que les structures correspondantes ne pourront pas être données dans ce mémoire pour des raisons de confidentialitéconfidentialité et de secrets industriels. Toutefois, il nous est possible de donner une idée générale des molécules afin de mieux comprendre les conclusions tirées de ces travaux.
Le CED 28 possède sur une extrémité une fonction amine fixée sur un cycle aromatiquearomatique, sur ce cycle est également lié un espaceur qui permet la liaison avec un autre cycle aromatique possédant un atomeatome d'azoteazote.
Le CED 32 a sur une extrémité un cycle non aromatique sur lequel est greffé un groupement aminé d'une part, et d'autre part, un cycle aromatique séparé du premier cycle par un espaceur de même taille que pour le CED 28.
Le CED 33 possède un cycle aromatique sur lequel est fixé un groupement aminé et un espaceur de même longueur que pour les molécules précédentes pour effectuer une liaison avec un autre cycle aromatique.
Le CED 39 possède sur une extrémité un cycle contenant deux atomes d'azote et sur l'autre extrémité un bicycle aromatique possédant un atome d'azote. Il est à noter que la distance entre les deux cycles est plus petite que dans les autres molécules.