au sommaire
Diagnostic et traitement des cancers : l'aide de la génétique
Les cancerscancers sont uniques dans le sens où chaque tumeurtumeur a ses particularités. Déconcertant au premier abord, cela est au contraire bénéfique pour le patient puisque cela permet de personnaliser les traitements afin de cibler encore mieux leur propre tumeur.

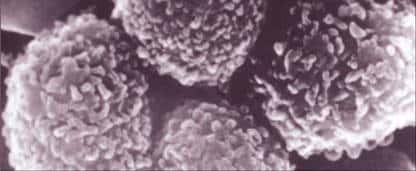
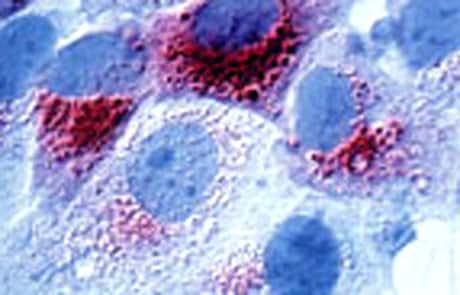
Étude de marqueurs tumoraux dans le pronostic du cancer du sein. Marquage immunohistochimique de la Cathepsine D hyperexprimée dans des cellules de lignée humaine de carcinomes mammaires MCF 7 (Métastase cellulaire facteur 7). La Cathepsine D est une enzyme lysosomiale acide qui favoriserait le potentiel métastatique des cellules tumorales. © H. Rochefort/Inserm - Reproduction et utilisation interdites
L'aide de la génétique
Chaque cancer est unique. Pour le patient, confronté à l'expérience douloureuse de la maladie, ce sentiment va de soi. Mais, avec les progrès de la génomiquegénomique, l'idée a aussi trouvé une illustration concrète, à la source d'un des progrès les plus marquants de cette dernière décennie en matière de cancérologiecancérologie. Plusieurs recherches européennes travaillent ainsi sur le typage de diverses expressions moléculaires des cancers. Cette approche innovante, particulièrement appliquée dans les tumeurs liées au genre, offre de nouvelles perspectives tant sur le plan du diagnosticdiagnostic que du traitement.
À l'origine de ce progrès, un outil : la puce à ADNADN. De quoi s'agit-il ? Schématiquement, d'une méthode de laboratoire permettant de reconnaître rapidement les gènesgènes exprimés dans un tissu vivant - et donc d'établir le profil génétiqueprofil génétique d'une personne, que ce soit au niveau de son patrimoine (on étudie alors l'ADN de ses chromosomeschromosomes) ou de la manière dont il s'exprime dans une cellule donnée, notamment tumorale (on étudie alors les ARNARN produits par les seuls gènes qui sont exprimés). Le grand intérêt de cette technologie est de pouvoir analyser simultanément des milliers de gènes en quelques heures, là où l'étude d'une poignée d'entre eux nécessitait, il y a encore quinze ans, des années de travail. Une des toutes premières puces à ADN a ainsi été appliquée au typage moléculaire de tumeurs du sein. L'innovation avait, en son temps, eu les honneurs de la couverture de Nature. Décrire, sur le plan moléculaire, ce qui fait l'unicité de chaque cancer est, en effet, porteur d'immenses espoirs aussi bien au niveau des diagnostics que des traitements.
Nouvelles signatures pour les diagnostics
Le diagnostic tout d'abord. Lorsque le cancer est détecté, il est souvent trop tard car des métastasesmétastases se sont formées. Le danger est particulièrement prégnant avec le cancer de l'ovaire, ce « tueur silencieux » comme l'appelle Robert Zeillinger, de l'université de médecine de Vienne, coordinateur du projet OVCAD. La tumeur de l'ovaireovaire croît longtemps sans déclencher de symptômessymptômes, à tel point que trois quarts des décès sont attribuables à une découverte trop tardive.
De même, dans le cancer de la prostate, les traitements qui parviennent à venir à bout de la tumeur initiale laissent souvent subsister des résidus indétectables, susceptibles de former de redoutables métastases osseuses. Chris Bangma, de l'université médicale Erasme (Rotterdam - NL), explique l'enjeu médical: « Pour diagnostiquer la maladie, on utilise actuellement le dosagedosage d'un marqueur appelé PSAPSA (ProstateProstate Specific Antigen), dont la concentration augmente en cas de cancer. Mais le problème est que ce dosage n'est pas assez spécifique. Il peut donner des faux positifs pour les personnes en bonne santé ou ayant des tumeurs non malignes. A l'inverse, il peut être négatif en cas de très petites tumeurs. » Chris Bangma coordonne le projet P-Mark qui vise à explorer l'utilisation d'autres marqueurs du cancer de la prostatecancer de la prostate comme tests diagnostiques.
L'espoir des chercheurs d'OVCAD et de P-Mark, ainsi que les équipes de Promet travaillant également sur la prostate, est donc de trouver des signatures moléculaires de la transformation cancéreuse, détectables dès que celle-ci survient. Ces signatures peuvent être des protéinesprotéines exprimées à la surface des cellules tumorales, des niveaux d'hormoneshormones, des messages intra ou intercellulaires, ou encore une altération de l'expression génétique. Explorant une voie nouvelle, le projet Epitron cherche pour sa part du côté des mécanismes épigénétiques (1), c'est-à-dire portant non sur la séquence d'ADN mais sur l'organisation de la double hélice d'ADN en chromatinechromatine des noyaux cellulaires, en particulier dans les cancers du seincancers du sein.
Le temps d'un traitement
Le traitement, ensuite. Tous les cancérologuescancérologues sont, en effet, confrontés à un dilemme : lorsqu'un cancer a été pris en charge précocement et semble guéri, faut-il poursuivre un traitement pour prévenir le risque de récidiverécidive ? À l'interrompre trop tôt, on risque de laisser subsister des cellules cancéreuses indétectables, qui n'ont pas encore formé de tumeurs, comme c'est souvent le cas dans le cancer de la prostate. À trop le prolonger, on risque d'épuiser l'organisme du patient par des traitements souvent lourds et parfois douloureux, en particulier dans le cancer de l'ovairecancer de l'ovaire où, comme le reconnaît Robert Zeillinger, « des chimiothérapieschimiothérapies sont souvent prescrites, après résectionrésection chirurgicale de la tumeur, sans aucune certitude quant à leur utilité ». Ce problème existe aussi dans le cas de cancer du sein. Selon les coordonnateurs du réseau Transbig (sorte de réseau des réseaux qui unifie à l'échelle européenne les centres de recherche sur la maladie), entre 10 et 20 % des femmes ayant souffert de ce type de tumeur sont « surtraitées », avec toutes les conséquences néfastes que cela implique tant sur le plan médical (effets secondaires, dégradation de la qualité de vie) que pour l'équilibre financier des systèmes de santé publique.
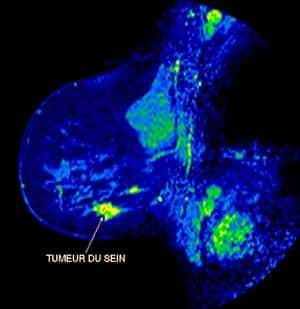
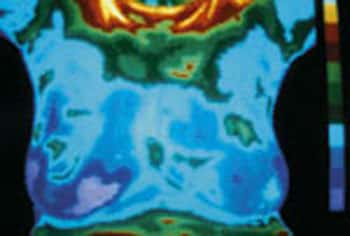
Image en couleur d'un cancer du sein.
© perso.wanadoo.fr/association.afrha/icono.htm
Grâce aux techniques de génomique, il devient possible de définir de véritables cartes d'identités moléculaires de chaque tumeur, qui permettront d'en prédire les propriétés et l'évolution, de personnaliser les traitements appliqués. Tel est le but du projet Transfog, qui commence à explorer tous les gènes impliqués, à un titre ou à un autre, dans le cancer du sein, mais aussi du poumonpoumon et du colon. À terme, il s'agit d'aboutir à une véritable prise en charge individualisée de chaque cancer. La médecine aura alors rejoint le « ressenti » du patient.
(1) Ce terme désigne le grand nombre de modifications de l'expression des gènes dont l'origine peut être, en particulier, des causes environnementales.