au sommaire

Bactéries et industrie
1 - La biolixiviation des minerais aurifères
Pour découvrir ce procédé, lire : L'or, la magie des alchimistes
On applique un procédé du même genre aux mineraisminerais cobaltifères.
2 - Biominéralisation du calcaire
A lire : Cristallographie, chimie de la calcite et en particulier les paragraphes sur les faluns et les tuffeaux.
Certaines bactériesbactéries fabriquent du carbonate de calciumcarbonate de calcium , ce processus est appelé carbonatogenèse. La première précipitation dite passive utilise les voies métaboliques : ammonification des acides aminésacides aminés, réductions diverses- nitrates, sulfates. On obtient du carbonate dissous dans la cellule puis intervient le phénomène de précipitation dite active qui sembe mettre en jeu des processus essentiellement membranaires. En étudiant ceci à des fins précises de restauration les chercheurs ont mis au point un traitement de la pierre qui consiste à favoriser le développement d'une mince couche de biocalcaire protecteur. A partir de 1990, tout un programme d'études visant à optimiser et à industrialiser le procédé a été mis en place. En effet, si le pouvoir calcifiant de certaines bactéries avait été clairement établi en laboratoire, il restait à démontrer la viabilité de celles-ci et le maintien de leurs performances, en situation réelle, extérieure mais également leur adaptation à une utilisation industrielle. Pour finir, c'est Bacillus cereus qui a été retenue comme la bactérie la plus performante et la plus apte à être utilisée de manière industrielle.

Tuffeau de l'église de Thouars
On nettoie la pierre et on y vaporise des bactéries qui vont faire la synthèse du calcairecalcaire dans les microcavités de la pierre, restaurant ainsi une surface (en une semaine, un voile de carbonate de calcium, appelé biocalcin, de quelques microns d'épaisseur (4 à 5 µm) occupe la surface du matériau) qui durcit dans les semaines suivantes par déshydratationdéshydratation. Pour le moment le procédé a déjà été utilisé en France à Thouars, voir bibliographie, et on suit attentivement les résultats depuis maintenant 10 ans.
Il est évident qu'un tel traitement est bien meilleur marché que le remplacement des pierres, beaucoup moins pénible et surtout il permet de maintenir les édifices en pierres fragiles comme le tuffeautuffeau par exemple qui est facilement attaqué et subit une desquamation dangereuse
3 - Lactobacillus et yaourt
A lire : Découvrir la fabrication du yaourt :
Le décret n°88-1203 du 30 décembre 1988, relatif aux laits fermentés et au yaourt ou yoghourtyoghourt réserve la dénomination yaourt ou yoghourt au "lait fermenté obtenu, selon des usages loyaux et constants, par le développement des seules bactéries lactiques thermophiles spécifiques dites Streptococcus salivarius subsp. thermophilus et Lactobacillus delbrueckii subsp. bulgaricus qui doivent être ensemencées et se trouver vivantes dans le produit fini à raison d'au moins 10 millions de bactéries par gramme rapportées à la partie lactée".

Yaourt
Le lait utilisé, écrémé ou non, concentré ou en poudre, enrichi ou non de constituant du lait, doit avoir subi un traitement thermique égal à la pasteurisationpasteurisation. La production d'acide lactiqueacide lactique par les bactéries à partir du sucresucre, le lactoselactose, modifie la structure des protéinesprotéines du lait et conduit à la prise en masse de celui-ci. Le coagulum est ferme, sans exsudationexsudation de lactosérum.
-- le yaourt "ferme", en pots après mélange des ingrédients, passe à l'étuve à 45°C pendant 3 h puis en chambre froide pour stopper l'acidification et éviter l'exsudation du sérumsérum ;
-- le yaourt "brassé" est préparé en vrac avec un brassage lui donnant une consistance crémeuse ou liquide.
-- le yaourt "à boire" est battu après avoir été brassé.
L'adjonction de sucre, colorants, arômes ou fruits, pulpe de fruits se fait avant ou après la fermentationfermentation. Certaines souches bactériennes produisent des filaments qui contribuent à la viscositéviscosité du yaourt.
4 - Fromages
La majorité des fromages sont fabriqués à partir de lait UHT. Le lait destiné au vrai Emmenthal, Parmesan et Grana, quelques fromages extra vieux, ne doit pas être chauffé à plus de 40°C, pour éviter d'en affecter le goût. Si du lait non pasteurisé est utilisé, le fromage doit mûrir au moins 60 jours à une température de 4°C ou moins pour garantir une sécurité envers les agents pathogènespathogènes.
Un certain nombre d'étapes principales communes à la plupart des fromages. Le lait est prétraité, après addition d'une culture de bactéries appropriée au type de fromage, et mélangé avec de la présure.

Fromage
La présure fait coaguler le lait en un gelgel solidesolide connu sous le nom de coagulum ou caillé. Celui-ci est découpé en de petits cubes pour faciliter l'expulsion du petit laitpetit lait. Pendant ce temps, les bactéries croissent, forment de l'acide lactique, et les grumeaux de caillé sont mélangés, et le tout est chauffé. Les effets combinés des 3 différents traitements - croissance des bactéries, traitement mécanique avec mélangeurs et chaleurchaleur permettent la séparationséparation du petit lait du caillé, la synérèse. Le caillé fini est placé dans des moules. Le fromage est pressé. La saveur finale se détermine pendant l'affinage.
Traditionnellement, certains produits chimiques - nitrate de sodiumsodium (NaNO3), eau oxygénéeeau oxygénée - ont été ajoutés au lait pour prévenir le gonflement et le développement de goûts désagréables causés par les bactéries thermophiles formant des spores (Clostridium tyrobutyricum ).
La culture d'amorçage - Deux principaux types de cultures sont utilisés dans la fabrication du fromage :
-- les cultures mésophilesmésophiles qui croissent entre 20 et 40°C
-- les cultures thermophiles, à plus de 45°C.
Ces cultures ne produisent pas que de l'acide lactique mais des composés aromatiquescomposés aromatiques et du CO2 essentiel pour créer des trous.
Trois caractéristiques des cultures d'amorçage :
-- la capacité de produire de l'acide lactique ;
-- la capacité de dégrader les protéines ;
-- la capacité de produire du dioxyde de carbonedioxyde de carbone (CO2).
La tâche principale de la culture est de fabriquer de l'acide dans le caillé.
Quand le lait coagule, les bactéries sont concentrées dans le caillé et donc dans le fromage. Le développement d'acide diminue le pH, ce qui est important pour aider la synérèse et éliminer les bactéries qui ont survécu à la pasteurisation ou les bactéries re-contaminantes. La production d'acide lactique s'arrête quand tout le lactose du fromage (sauf pour les fromages doux) a été fermenté. En outre, les sels de calcium et de phosphorephosphore sont ajoutés, ce qui influence la consistance du fromage et aide à raffermir le caillé.

Plateau de fromage
Autres apports possibles
Chlorure de calcium pour atteindre un temps de coagulationcoagulation constant et engendrer une fermeté suffisante.
Le phosphatephosphate de sodium augmente l'élasticitéélasticité du coagulum due à la formation de phosphate de calcium colloïdal Ca3(PO4)2.
Dioxyde de carbone pour améliorer la qualité du lait, diminuer le pH du lait, réduire le temps de coagulation, obtenir le même temps de coagulation avec moins de présure
Salpêtre (NaNO3 ou KNO3) pour contrecarrer des bactéries productrices d'acide butyrique et/ou des bactéries de type coliformes
Les colorants : le carotènecarotène, l'orléana, chlorophyllechlorophylle verte
Bref une jolie panoplie ...
5 - Formation du vinaigre.
Il faut du vin de raisinraisin, de pommes ou autres c'est-à-dire des fruits ayant subi une fermentation alcooliquefermentation alcoolique. Les solutions peuvent atteindre une concentration maximale en alcoolalcool de 15% en volumevolume; un taux plus important empêcherait la fermentation.
Si on laisse du vin à l'airair libre à température ambiante, il deviendra acide, on dit alors que le vin est piqué. Les romains connaissaient et utilisaient le vinaigre.
L'appellation vinaigre décrit bien cette réaction parasiteparasite. Le vin devient aigre, du latin acer, aigre, acéré. C'est Lavoisier (1743-1794) qui a découvert que la formation du vinaigre correspondait à l'oxydationoxydation de l'alcool. Mais c'est à Pasteur (1808-1873) que nous devons la découverte du processus de formation du vinaigre. La bactérie du vinaigre "aceto-bacter" se développe dans le vin non bouché. Les petites mouches qui sont fortement attirées par le vin placé à l'air libre et qu'on appelle mouches du vinaigremouches du vinaigre (drosophiles) véhiculent l'aceto-bacter. Les bactéries de l'acide acétique forment la mère du vinaigre. L'aceto-bacter utilise l'énergieénergie libérée par l'oxydation : processus aérobieaérobie. Au taux d'alcool correspond à la quantité d'acide acétique qui résultera de la transformation.

Vinaigre d'Orléans - Orléans est considérée comme la capitale du vinaigre depuis le 18ème siècle.
Interruption du processus.
Lors de la fermentation du vin, le processus de transformation du vin en vinaigre est indésirable. C'est pourquoi on ferme les fûts de moût en fermentation avec des dispositifs qui laissent sortir le dioxyde de carbone formé sans permettre à l'air de pénétrer. Le dispositif employé empêche non seulement la pénétration de l'oxygèneoxygène de l'air mais aussi celle de l'aceto-bacter et d'autres microorganismesmicroorganismes qui contribuent à la détérioration du vin. Pour rendre les amphores étanches les Romains utilisaient de l'argileargile, du plâtreplâtre, de l'écorce de chênes-liègeschênes-lièges, de résine de pin qui conférait au vin un goût particulier. Le vin de l'antiquité ne se consommait pas pur, on l'aromatisait avec des herbes et des épices; ces additifs permettaient une meilleure conservation du vin. L'adjonction de SO2 entrave l'activité des bactéries de l'acide acétique.
6 - Drainage minier acide ou DMA, ou les choses qui fâchent…
Les minérauxminéraux sulfurés sont sujets à une oxydation par l'air et l'eau. Ce phénomène entraîne l'apparition d'acide sulfuriqueacide sulfurique et la solubilisation des métauxmétaux présents. Lors des travaux miniers, des gisementsgisements de sulfuressulfures métalliques profonds sont brutalement en conditions oxydantes et cette réaction prend une ampleur suffisante pour générer des écoulements acides appelés drainagesdrainages miniers acides (DMA)
Mécanismes de formation et origine du phénomène.
Les minéralisations du sous-sol sont dues à des circulations de fluides qui transportent des cationscations métalliques qui vont être piégés dans les horizons réducteurs. Or l'exploitation minière va les exposer à l'air et à l'eau ! Les DMA se forment, soit dans les galeries ennoyées, soit par percolationpercolation d'eau sur les tas de solides contenant des sulfures. Les quantités peuvent atteindre plusieurs millions de tonnes comme à Chuquimata, au Chili, la plus grande mine de cuivrecuivre où il s'agit d'une surface de 48 km². Les réactions chimiquesréactions chimiques principales qui donnent lieu à un DMA sont l'oxydation du ferfer et du soufresoufre de la pyritepyrite.

Mines de cuivre
L'oxydation de la pyrite est un processus complexe faisant intervenir des réactions de complexationréactions de complexation et d'hydrolysehydrolyse. Singer et Stumm (1968) ont proposé un modèle d'oxydation de la pyrite en trois étapes faisant intervenir des moléculesmolécules d'oxygène et des ionsions ferriques.
Oxydation aqueuse par l'oxygène dissout :
FeS2 + 7/2 O2 + H2O = Fe2+ + SO4 2- +H2SO4

Pyrite
seul le soufre est oxydé en sulfate, le fer est solubilisé sous forme d'ions ferreux.
Oxydation des ions ferreux en ions ferriques par l'oxygène dissout :
Fe2+ + 1/4 O2 + H+ = Fe3+ + ½ H2O
n'affecte pas la pyrite, mais est préalable à l'étape suivante, où l'oxydation ne requiert plus l'action de l'oxygène.
Oxydation aqueuse par les ions ferriques :
FeS2 + 8 H2O + 14 Fe3+ = 15 Fe2+ + 2 SO4 2- + 16 H+
Cette réaction a lieu en présence ou en l'absence de bactéries et varie en fonction du pH. La particularité de cette réaction est d'être autocatalysée, l'oxydation des sulfures produit du fer ferrique, qui entraîne l'oxydation d'autres sulfures....Le DMA est favorisé par des microorganismes mais les détails de ce phénomène sont encore mal compris.
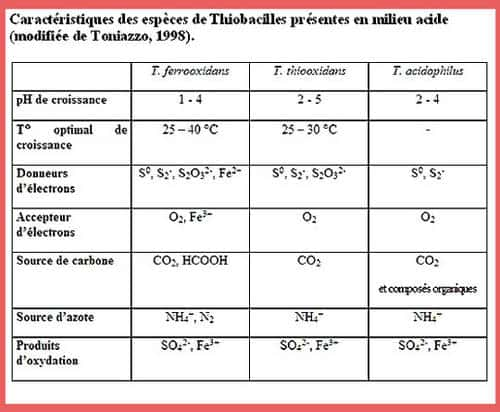
Tableau Thiobacilles
Pollutions induites : les DMA sont source de pollution acide et métallique pour les milieux aquatiques et les aquifèresaquifères en libérant des composés métalliques toxiques. La présence simultanée de plusieurs métaux peut engendrer une toxicitétoxicité supérieure à celle de chaque métal séparé : mortalité des poissonspoissons, perturbations de croissance et de reproduction. Les effets indirects sont la dégradation de l'habitat et une interruption de la chaîne alimentairechaîne alimentaire. Presque aucune espèceespèce ne survit à des pH inférieurs à 5.
Dans les régions de terrains acides, l'acidité des eaux est conservée et les métaux sont transportés sous forme soluble à grande distance.
Dans les régions de terrains calcaires, les eaux acides sont neutralisées par les carbonates, et la plupart des métaux précipitent. Lors des crues, les particules solides riches en métaux seront entraînées en aval et peuvent redevenir solubles si les caractéristiques changent. Exemple, le cadmiumcadmium de la Gironde provient du bassin du Lot, est solubilisé dans l'estuaireestuaire et peut être transporté à plus de 400 km de sa source et se retrouver dans des huîtres.
En dégradant la qualité de l'eau, les DMA conduisent à la disparition de ses usages en aval, ils sont responsables de la corrosioncorrosion des infrastructures minières et des équipements.
La pollution par les métaux est aussi ancienne que l'activité minière mais ce n'est pas une excuse !. Dans l'estuaire du Rio Tinto (Espagne), petit fleuve acide qui draine la plus grosse minéralisation sulfurée du monde, un sondage a recoupé un horizon contaminé contenant des sablessables à sulfures avec des scoriesscories et des charbonscharbons datés de l'âge du cuivreâge du cuivre (-2500 ans).

Rio Tinto - Espagne - Détail des eaux acides (pH 2,0) et rouges (forte charge sulfatée et métallique) du fleuve Rio Tinto, circulant dans le sud de l'Espagne, à Huelva. Ce fleuve, qui se situe dans l'une des zones les plus polluées du monde, fait l'objet d'une étude menée par huit laboratoires européens. L'analyse des nombreux échantillons d'eau devraient permettre d'améliorer la gestion des ressources hydrologiques, dans une région qui souffre d'un manque chronique d'eau, afin d'assurer les besoins vitaux, agricoles et industriels.
© CNRS Photothèque M. Leblanc
Tous droits réservés
Détail des eaux acides (pH 2,0) et rouges (forte charge sulfatée et métallique) du fleuve Rio Tinto, circulant dans le sud de l'Espagne, à Huelva. Ce fleuve, qui se situe dans l'une des zones les plus polluées du monde, fait l'objet d'une étude menée par huit laboratoires
européens. L'analyse des nombreux échantillons d'eau devraient permettre d'améliorer la gestion des ressources hydrologiques ,dans une région qui souffre d'un manque chronique d'eau, afin d'assurer les besoins vitaux, agricoles et industriels.
Ce type de pollution a longtemps été occulté pour ne pas entraver le développement industriel. En fait, il a fallu deux accidentsaccidents majeurs pour toucher l'opinion mondiale : Aznalcóllar (Espagne), en 1998, déversement de 4 millions de m3 de DMA dans un fleuve adjacent ; à Baia Mare (Roumanie), en 2000, le déversement de 100000 m3 de DMA, contenant 100 tonnes de cyanure, ont contaminé le Danube sur plus de 2000 Km.
Solutions techniques : elles sont toujours chères quand elles existent. Pour terminer signalons que le BRGMBRGM a un dossier sur le sujet.