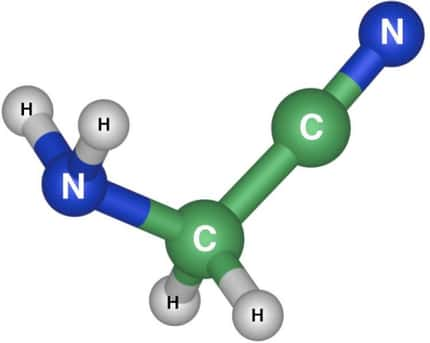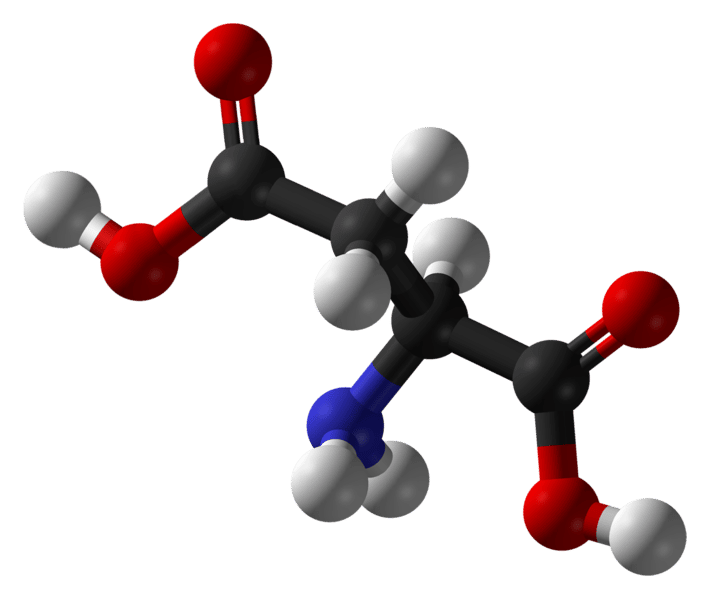
L'acide aspartique est un acide aminé acide (carbone en noir, oxygène en rouge, azote en bleu et hydrogène en blanc). © Ben Mills, domaine public
L'acideacide aspartique (Asp, D ou aspartate) est l'un des 22 acides aminés qui entrent dans la composition des protéines.
Structure de l’acide aspartique
L'acide aspartique possède deux groupements fonctionnels, comme tout acide aminé : un groupe carboxyle (COOH) et un groupe amine (NH2). Sa chaîne latérale est la suivante : -CH2-COOH.
L'acide aspartique est polaire, dicarboxylique, ce qui en fait le plus acide des acides aminés.
Fonction de l’acide aspartique
L'acide aspartique n'est pas un acide aminé essentiel puisqu'il peut être synthétisé par l'organisme à partir d'oxaloacétate.
Il est un métabolite du cycle de l'urée et participe à la gluconéogenèsegluconéogenèse, ainsi qu'à la synthèse de l'inosine, un précurseur des bases azotéesbases azotées.
L'acide aspartique est aussi un neuromédiateurneuromédiateur, moins puissant que le glutamateglutamate.