au sommaire
- À lire aussi
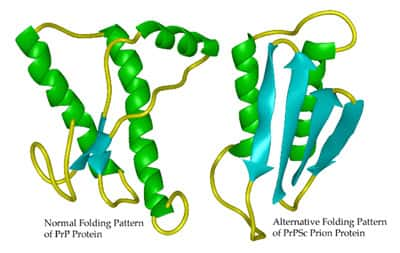
La théorie des prions validée
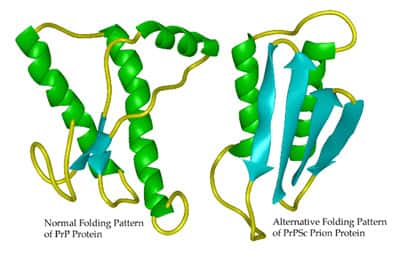
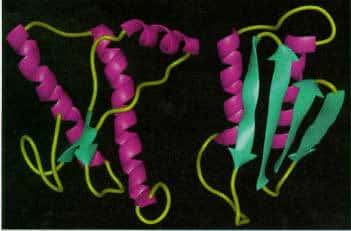
La théorie du prion développée par Stanley Prusiner a été récompensée par le prix Nobel de médecine en 1997. Sa théorie décrit qu'une protéine (nommée Prpc) peut changer de conformation et devenir infectieuse Prpsc . Ce changement de conformation se propage alors aux moléculesmolécules Prpc, les rendant ainsi infectieuses à leur tour. Cette protéine est supposée être l'agent pathogène responsable de la maladie de la vachevache folle (l'encéphalopathie spongiforme bovineencéphalopathie spongiforme bovine; l'ESB).
Malgré de nombreux travaux, jusqu'à présent aucune équipe n'avait pu prouver que l'agent pathogène était constitué uniquement par une protéine, et il existait toujours une possibilité qu'un virus inconnu soit aussi impliqué. Un début de preuve vient justement d'être apporté, en montrant qu'il était possible de synthétiser in-vitro la protéine pathogène. Les implications de cette découverte sont nombreuses sur le plan théorique et devraient aussi permettre de découvrir de nouveaux moyens pour soigner la variante humaine de la maladie de la vache folle.
Jusque-là les chercheurs utilisaient la protéine Prp entière pour tenter de rendre cette protéine pathogène in vitroin vitro. Cette fois ci l'équipe de Prusiner a utilisé un fragment plus petit de la protéine, dont on pensait qu'il changeait de conformation plus facilement que la protéine entière. Le fragment a ainsi été synthétisée par une bactériebactérie avant d'être purifié, puis les chercheurs ont tenté de provoquer son changement de structure pour former des fibres amyloïdes, caractéristiques de la forme Prpsc .
Les souris témoins ont reçu une injection d'un extrait de cerveaucerveau ne contenant pas le prion synthétique. Après 670 jours, aucune souris n'a développé de signes cliniques de la maladie. Contrairement aux souris ayant reçu le prion synthétique qui ont développé la maladie en 380 jours. Un broyat de cerveaux de ces souris a été de nouveau injecté dans des souris saines, qui ont alors développé la maladie en seulement 154 jours. Ceci suggère que le nombre de prions pathogène initial était très faible mais s'est accru au cours du premier cycle d'infection.
Ces résultats suggèrent qu'initialement un prion pathogène s'est formé in vitro. Même si une explication alternative pourrait être que le prion pathogène est apparu au cours du premier cycle d'infection dans la souris. Des expériences sont actuellement en cours, afin de déterminer si l'injection d'un broyat de cerveaux de souris saines peut provoquer ou non spontanément l'apparition du prion.