au sommaire
Nous sommes quotidiennement exposés à de multiples composés exogènesexogènes tels que des polluants environnementaux, des médicaments ou des substances provenant de notre alimentation. Certaines de ces moléculesmolécules, appelées perturbateurs endocriniens, sont fortement suspectées d'interagir inopportunément avec des protéines régulatrices de nos cellules et d'induire de nombreux troubles physiologiques ou métaboliques (cancers, obésité et diabète...). Par ailleurs, la combinaison de ces molécules dans les mélanges complexes avec lesquels nous sommes généralement en contact pourrait exacerber leur toxicité.
Dans un article publié dans Nature Communications, les chercheurs du Centre de biochimiebiochimie structurale (CNRS, Inserm, université de Montpellier), de l'Institut de recherche en cancérologiecancérologie de Montpellier (Inserm, université de Montpellier, ICM) et de l'Institut de génomique fonctionnelle (CNRS, Inserm, université de Montpellier) dévoilent un mécanisme qui pourrait contribuer à cet effet de mélange pour lequel aucune explication rationnelle n'avait à ce jour été apportée. Ils montrent que certains estrogènesestrogènes comme l'éthinylestradiol (un des composants actifs des pilules contraceptives) et des pesticides organochlorés tels que le trans-nonachlor, bien que très faiblement actifs par eux-mêmes, ont la capacité de se fixer simultanément à un même récepteur situé dans le noyau des cellules et de l'activer de façon synergique.
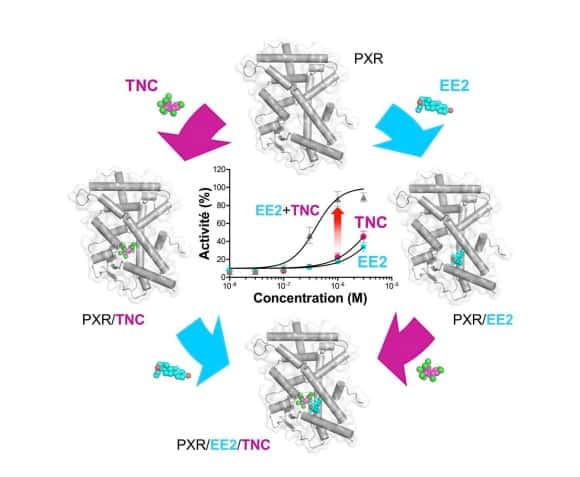
Séparément, l’éthinylestradiol (EE2) et le trans-nonachlor (TNC) se lient seulement à forte concentration au récepteur des xénobiotiques (PXR) et sont des activateurs faibles de ce récepteur. Lorsqu’ils sont utilisés ensemble, les deux composés se stabilisent mutuellement dans la poche de liaison du récepteur. Le « ligand supramoléculaire » ainsi créé possède une affinité augmentée pour PXR, de sorte qu’il est capable d’induire un effet toxique à des doses auxquelles chaque composé est inactif individuellement. © Vanessa Delfosse, William Bourguet
150.000 molécules aux interactions inconnues sur la santé humaine
Des analyses à l'échelle moléculaire indiquent que les deux composés se lient coopérativement au récepteur, c'est-à-dire que la fixation du premier favorise la liaison du second. Cette coopérativité est due à de fortes interactions au niveau du site de liaison du récepteur, de sorte que le mélange binairebinaire induit un effet toxique à des concentrations largement plus faibles que les molécules individuelles.
Ces résultats obtenus in vitroin vitro constituent une preuve de concept qui ouvre la voie à un large champ d'études. Il existe effectivement dans notre environnement environ 150.000 composés dont l'action combinée pourrait avoir des effets inattendus sur la santé humaine au regard de leur innocuité reconnue ou supposée en tant que substances isolées. Si ces travaux sont confirmés in vivoin vivo, des retombées importantes sont attendues dans les domaines de la perturbation endocrinienne, la toxicologietoxicologie et l'évaluation des risques liés à l'utilisation des produits chimiques.