au sommaire
- À lire aussi

Origine des maladies auto-immunes : le scénario se confirme
Elles sont la conséquence d'une réaction de défense anormale du système immunitaire d'un individu, qui attaque ses propres cellules, tissus ou organes, sans raisons expliquées. Une équipe de chercheurs de l'Inserm et de l'hôpital Bicêtre (Assistance Publique-Hôpitaux de Paris) vient de démontrer, dans le syndrome de Sjögren -un modèle de maladie auto-immune- la responsabilité des protéines de défense contre les infections dans la survenue et l'entretien de ces pathologies invalidantes. Ces résultats, qui suggèrent un scénario faisant intervenir facteurs d'environnement et facteurs génétiques, sont publiés dans les Proceedings of the National Academy of Science (PNAS) du 21 février 2006.
Le syndrome de Gougerot-Sjögrensyndrome de Gougerot-Sjögren (ou syndrome de Sjögren), qui touche 0,1 à 0,2 % de la population mondiale, arrive, en terme de fréquence, au deuxième rang des maladies autoimmunes affectant plusieurs organes (maladies auto-immunesmaladies auto-immunes systémiques), après la polyarthrite rhumatoïde. Il se manifeste par une sécheressesécheresse très invalidante de la bouche et des yeuxyeux, des douleursdouleurs diffuses, une inflammationinflammation des articulationsarticulations, une grande fatigue, des atteintes de différents organes (peau, poumonspoumons, reinsreins, cerveaucerveau, etc.) et un risque de lymphomelymphome (cancercancer des organes lymphoïdeslymphoïdes) 20 à 40 fois plus élevé que dans la population générale.
L'origine de ces maladies auto-immunes est inconnue mais il existe de façon certaine une interaction entre des facteurs génétiques et environnementaux. Parmi ces derniers, le rôle des infections est suspecté depuis longtemps.
Le rôle majeur des interféronsinterférons (protéines permettant la défense contre les infections) vient d'être mis en évidence dans le syndrome de Sjögren, considéré comme un modèle de maladie auto-immune systémique, dans les travaux menés par les unités Inserm U802 (IFR Bicêtre) et U567 (Institut Cochin, Paris), en collaboration avec le service de rhumatologie de l'Hôpital Bicêtre (Assistance Publique-Hôpitaux de Paris) et l'Université Paris-Sud 11.
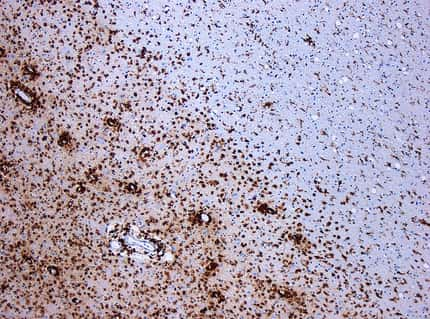
Ces équipes ont effectué des prélèvements dans les organes affectés par la maladie (tissus salivaires et oculairesoculaires) et ont comparé ces prélèvements à ceux effectués chez des sujets sains, grâce à la technique innovante et puissante des puces à ADNADN qui permet l'étude simultanée de plusieurs milliers de gènesgènes. Les résultats ont montré, chez les malades, une surexpression de nombreux gènes dont il est établi que l'expression est liée à la présence d'interférons, protéines de défense contre les infections virales. Les auteurs ont ensuite recherché la présence de cellules dont le rôle est de sécréter l'interféron après une infection virale ou bactérienne : les cellules dendritiques plasmacytoïdes. Si ces cellules permettant une défense rapide contre les infections sont bien présentes dans les tissus salivaires de tous les malades étudiés, elles n'ont jamais été trouvées chez les sujets sains.
Dans ce modèle de maladie auto-immune, le rôle de l'interféron, qui avait été mis récemment en évidence dans le lupus érythémateuxlupus érythémateux disséminédisséminé, vient donc d'être démontré. Les chercheurs proposent un scénario expliquant le déclenchement puis la persistance des maladies auto-immunes : rôle initial d'un facteur environnemental, probablement d'une infection virale, conduisant à la sécrétionsécrétion des interférons. Chez des individus ayant certains facteurs de risquefacteurs de risque génétiques, cette sécrétion d'interférons active le système immunitaire qui provoque et entretient l'agression des organes cibles.
Enfin, ces découvertes offrent de nouveaux espoirs pour le traitement des maladies autoimmunes avec la perspective de nouveaux médicaments bloquant l'action des interférons, actuellement en cours d'essai cliniqueessai clinique. Cependant, bloquer l'interféron peut entraîner des effets indésirables infectieux voire perturber certaines défenses anti-cancéreuses. En effet, l'interféron est utilisé dans le traitement de certaines maladies infectieuses comme l'hépatite Chépatite C, mais aussi de certains cancers, comme le mélanome, un cancer de la peaucancer de la peau.
Faudra-t-il choisir entre pathologie auto-immune et cancer ? L'avenir pour le traitement des maladie auto-immunes dépendant de l'interféron réside peut-être dans l'utilisation d'inhibiteurs non de l'interféron lui-même mais des moléculesmolécules induites par l'interféron, l'un des meilleurs candidats étant la cytokinecytokine BAFF (B-cell Activating Factor of the TNF Family) ou BlyS (B LymphocyteLymphocyte Stimulator) qui est produite en excès dans de nombreuses maladies auto-immunes.