au sommaire
C'est un vieux fantasme humain : comment aider les personnes non-voyantes à retrouver ce sens qu'elles ne possèdent plus ? La médecine moderne semble montrer que l'exploit est de l'ordre du possible, surtout que l'œil est particulièrement étudié et l'un des premiers organes à bénéficier des thérapies les plus modernes : rétines artificielles, thérapie génique et thérapies cellulaires.
La transplantation de cellules rétiniennes conçues à partir de cellules souches embryonnaires (CSE) n'est pas nouvelle. Par la taille de l'œil, qui ne nécessite pas l'implantation de millions ou de milliards de cellules, et la faiblesse du système immunitairesystème immunitaire dans cette région, la réussite d'une telle entreprise est crédible.
Des chercheurs américains ont même entamé des essais cliniquesessais cliniques sur la question, afin d'aider des personnes atteintes de rétinopathie (ici des patients touchés par la maladie de Stargardtmaladie de Stargardt ou la DMLADMLA) à recouvrer leurs capacités visuelles. Dans ce cas précis, signalé l'an dernier, les CSE sont transformées en épithéliumépithélium pigmentairepigmentaire, des cellules de soutien pour les photorécepteurs, ces cellules en forme de cônecône ou de bâtonnetbâtonnet, directement impliquées dans la vision et connectées au cerveaucerveau, afin qu'il traduise le signal en information visuelle.
Des cellules souches aux photorécepteurs fonctionnels
Désormais, des scientifiques britanniques de l'University College de Londres dirigés par Robin Ali ont franchi un nouveau cap. Ce ne sont plus les cellules de soutien qui ont été conçues depuis des CSE, mais bel et bien des photorécepteurs. Et comme ils l'expliquent dans la revue Nature Biotechnology, une fois transplantées chez l'animal, ces cellules semblent occuper leur position et jouer leur rôle en établissant les liaisons avec le nerfnerf optique.
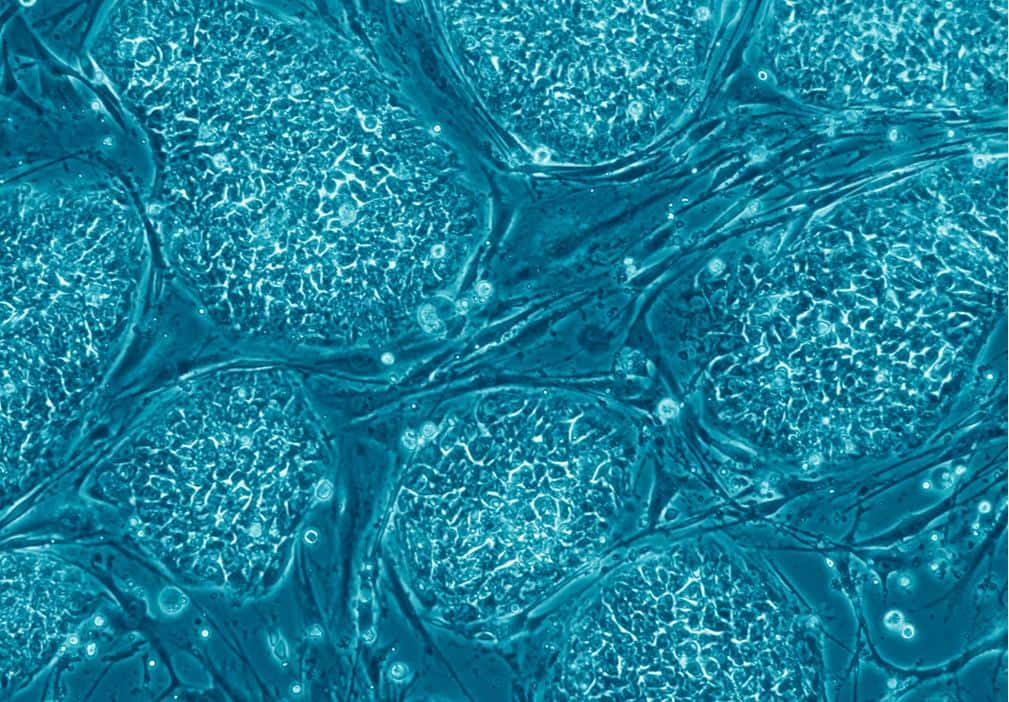
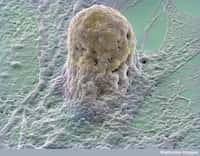
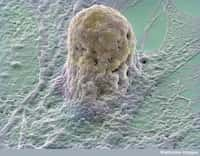
Les cellules souches embryonnaires ont la particularité de pouvoir se différencier en n'importe quel tissu adulte, si tant est qu'on les place dans le milieu de culture adapté. Dans cette expérience, elles sont devenues des photorécepteurs. © Eugene Russo, Plos One, cc by 2.5
Les auteurs ont réalisé une culture en trois dimensions de CSE de souris, de manière à les pousser vers une destinée de photorécepteurs. Pour s'assurer de la bonne différenciation des cellules, ils ont vérifié que les gènesgènes exprimés étaient biologiquement équivalents. Une rétinerétine de synthèse a ainsi pu croître en boîte.
Environ 200.000 de ces photorécepteurs artificiellement créés ont alors été transplantés dans la rétine de souris aveugles. Trois semaines après l'opération, les cellules avaient migré et avaient trouvé leur position dans l'œil de leur hôte. Elles avaient l'aspect de cellules en bâtonnet matures normales, et étaient toujours sous cette forme six semaines plus tard. Des synapsessynapses, les connexions avec le système nerveux, ont même pu être observées.
Un futur traitement contre de nombreuses formes de cécité ?
La description s'arrête là : on ne sait donc pas si les rongeursrongeurs ont retrouvé au moins une partie de leur vision. Pour Robin Ali, si seulement 20.000 des 200.000 cellules transplantées prennent, cela devrait être suffisant pour redonner la vue. Cependant, il semble que seules 1.000 d'entre elles aient réellement trouvé leur place. La technique est à perfectionner pour augmenter le ratio et donc améliorer le traitement.
D'ici cinq ans, le Britannique espère pouvoir entamer les essais cliniques chez l'Homme, après avoir ajusté le protocoleprotocole et obtenu les accords nécessaires. Si la thérapie cellulaire aboutissait, elle pourrait aider des personnes atteintes de maladies oculairesoculaires dégénératives, comme la rétinite pigmentairerétinite pigmentaire, la DMLA, la maladie de Stargardt ou les cécités provoquées par le diabètediabète de type 2, de retrouver goût à la vue.