au sommaire
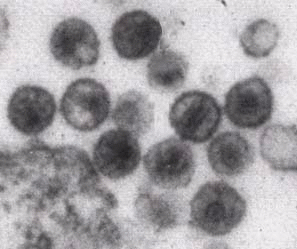
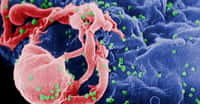
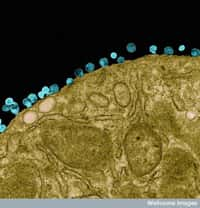
Des virus VIH observés au microscope électronique. © DR
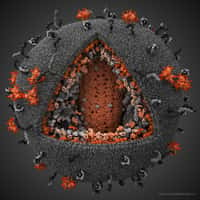
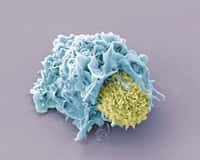
Pourquoi certaines personnes résistent-elles mieux que d'autres au virus VIH, vecteur du Sida ? L'une des raisons possibles est génétique. Le virus se fixe sur les lymphocytes TT (qui font partie des globules blancsglobules blancs) en se liantliant à un récepteur, appelé CD4, et à un co-récepteur, qui peut être le CXCR4 ou le CCR5. Il arrive que le gènegène servant à fabriquer ce dernier soit muté, rendant ce co-récepteur non fonctionnel. Les virus qui s'attachent à lui ne peuvent donc plus attaquer les lymphocytes.
Un moyen de lutter contre l'infection est donc de fermer cette porteporte d'entrée. L'idée d'empêcher la fixation du VIH est explorée depuis plusieurs années, avec différents moyens. Carl June, du Abramson Family CancerCancer Research Institute (université de Philadelphie), et son équipe s'inscrivent dans cette voie de recherche en s'attaquant aux co-récepteurs.
Sur des lymphocytes T d'origine humaine mis en culture, les chercheurs ont modifié le gène du CCR5 en utilisant un outil d'une précision extrême, les protéinesprotéines en doigt de zinczinc. Ces moléculesmolécules sont ainsi appelées car elles portent une chaîne d'acides aminésacides aminés capables de fixer un ionion de zinc. On les a découvertes à l'intérieur des cellules et leur fonction est d'interagir avec les acides nucléiquesacides nucléiques, ARNARN ou ADNADN. Elles jouent un grand rôle dans la cellule et on en trouve également sur la capsidecapside (l'enveloppe) du virus VIH.
Bons résultats mais à confirmer
Pour le biologiste, ces protéines en doigt de zinc servent aussi à inciser une molécule d'AN à un endroit précis. C'est ainsi que les chercheurs américains ont altéré le gène du co-récepteur CCR5, rendant celui-ci non fonctionnel, mimant la mutation qui rend certaines personnes plus résistantes au Sida. Environ la moitié des gènes codant pour le CCR5 ont pu être effectivement désactivés dans les cellules en culture. Mis en présence du virus VIH, ces lymphocytes T modifiés ont montré une plus grande résistancerésistance.
L'expérience s'est poursuivie chez des souris, qui ont reçu par injection des lymphocytes T modifiés ou non. L'apport de cellules au gène désactivé conduit à un nombre moins important de virus VIH dans les cellules du sang. Ces souris présentent aussi un taux plus élevé de lymphocytes T CD4+, c'est-à-dire portant le récepteur CD4. Pour les chercheurs, c'est le signe d'une fonction immunitaire reconstituée par l'augmentation du nombre de lymphocytes CD4+ résistant au virus VIH.
Leurs résultats, qui viennent d'être publiés dans la revue Nature Biotechnology, ouvrent donc de belles perspectives thérapeutiques, mais qui restent bien sûr à confirmer. Le virus VIH s'accroche aussi au co-récepteur CXCR4. Faudra-t-il également muter le gène codant pour lui ? L'effet est-il suffisant pour contrer une infection ? Quels sont les effets secondaires ? Cette technique hautement sophistiquée est-elle praticable à grande échelle ? Voilà quelques questions auxquelles il faudra répondre dans les années à venir...