au sommaire

Un cristal d'arsenic retrouvé dans des mines japonaises. © Rob Lavinsky, iRocks.com – CC-BY-SA-3.0
Un poison qui soigne ? Difficile à croire mais classique. Paracelse avait raison : « Rien n'est poison, tout est poison : seule la dose fait le poison ». Malgré sa réputation de tueur (joliment appelé poudre de succession au XVIIe pour sa faculté à précipiter les héritages), l'arsenic a révélé son côté sympathique. Déjà dans l'Antiquité, les médecins connaissaient ses bienfaits et dans nos sociétés occidentales l'arsenicarsenic, en doses infimes, est connu depuis quelques années comme un bon moyen de traiter des maladies auto-immunes ou des leucémies.
Parmi celles-ci, la leucémie aiguë promyélocytaire ne touche qu'environ 100 personnes par an en France mais se développe rapidement. Cette forme de leucémie est caractérisée par une anomalie chromosomiqueanomalie chromosomique des cellules de la moelle osseuse, qui possèdent donc une version endommagée du génome. L'expression d'un gène défaillant mène à la synthèse d'une oncoprotéine, appelée PML/RARA, qui favorise l'apparition du cancercancer en dérégulant les gènes cellulaires et en incitant les cellules à proliférer de manière incontrôlée.
C'est là que le trioxyde d'arsenic entre en scène. Une équipe dirigée par Hugues de Thé (collaboration Inserm/CNRS/Université Paris Diderot), de l'hôpital Saint-Louis, a réussi à mieux caractériser les étapes de son action antitumorale et vient de publier ses résultats dans la revue Cancer Cell.
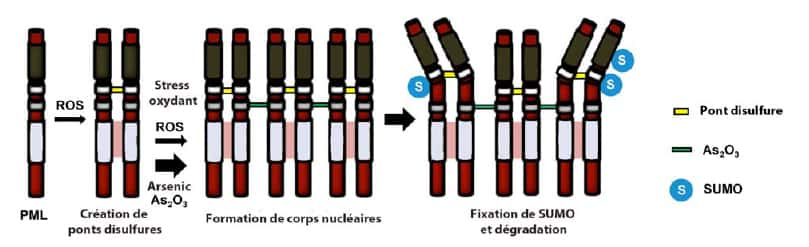
Modèle d'action de l'arsenic sur l'agrégation et la destruction des oncogènes PML/RARA dans le traitement de la leucémie aiguë promyélocytaire. Les ROS favorisent l'agrégation des PML/RARA, encore renforcée par la fixation de l'arsenic. Les corps nucléaires ainsi formés subissent des sumoylations (accrochage de protéines Sumo, Small Ubiquitin-like Modifier), puis une dégradation ciblée. © Inserm / CNRS / Cancer Cell
L’arsenic multifonctionnel dans la destruction de l’oncogène
Cette moléculemolécule d'arsenic inorganique, à l'image des autres métalloïdes, favorise la formation de formes réactives de l'oxygène (ROS), autrement appelés les radicaux libresradicaux libres. L'apparition des ROS entraîne la formation de ponts disulfure, une sorte de liaison chimiqueliaison chimique entre deux oncoprotéines PML/RARA.
D'autre part, l'arsenic est aussi capable de se fixer sur l'oncoprotéine PML/RARA. Habituellement, c'est la fixation de l'arsenic sur les protéinesprotéines qui est mortelle. Elle empêche, par exemple, le bon fonctionnement des protéines de la chaîne respiratoirechaîne respiratoire cellulaire. Dans le cas de la leucémie, c'est justement cette fixation qui est bénéfique pour le patient : la protéine PML/RARA, couplée à l'arsenic, favorise encore davantage la formation de ponts disulfure, ce qui induit l'agrégation des oncoprotéines dans un corps nucléaire.
L'arsenic favorise ensuite les étapes qui mèneront à la destruction des oncoprotéines : la modification des PML/RARA, ou sumoylationsumoylation (fixation de peptidespeptides SUMO), et enfin, le recrutement d'un facteur nommé RNF4, qui induit la dégradation ciblée des PML/RARA.
Sans oncoprotéines, pas de cancer : voilà pourquoi l'arsenic est si efficace dans le traitement de la leucémie aiguë promyélocytaire. En plus d'avoir répondu à cette interrogation, ces travaux peuvent aussi ouvrir la voie vers la compréhension et l'établissement de nouvelles thérapiesthérapies ciblées pour d'autres types de cancers.