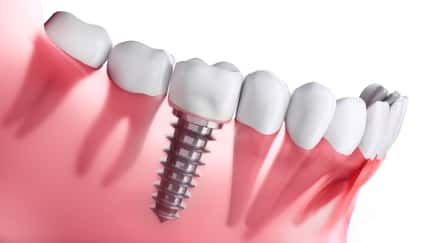
Les dispositifs médicaux implantables (prothèses orthopédiques, pacemakers, valves cardiaques, implants dentaires) constituent une interface idéale pour les micro-organismes qui peuvent facilement coloniser leur surface. L'infection bactérienne peut alors survenir et entraîner une réaction inflammatoire. Elle risque d'aboutir au rejet de l'implant. Ces infections sont principalement dues aux bactéries hébergées par l'organisme, telles que les staphylocoques dorés (Staphylococcus aureusStaphylococcus aureus), et au bacillebacille pyocyanique. Elles sont aussi parfois causées par des champignonschampignons ou des levureslevures. L'enjeu lié à l'implantation des dispositifs médicaux dans l'organisme est de prévenir l'apparition de ces infections engendrant des réactions immunitaires qui compromettent le succès de l'implantation. Actuellement, des antibiotiquesantibiotiques sont utilisés mais l'émergenceémergence de bactéries multirésistantes limite dorénavant leur action.
Dans ce contexte, les chercheurs de l'unité 1121 « Biomatériaux et Bioingénierie » (Inserm/université de Strasbourg), en collaboration avec quatre laboratoires, ont mis au point un film biologique aux propriétés antimicrobiennes et anti-inflammatoires. Pour sa mise au point, les scientifiques ont utilisé la combinaison de deux substances : la poly(argininearginine) (PAR) et l'acide hyaluroniqueacide hyaluronique (HA) pour réaliser un film invisible à l'œilœil nu (entre 400 et 600 nanomètresnanomètres d'épaisseur) constitué de plusieurs couches. L'arginine est métabolisée par les cellules immunitaires pour combattre les pathogènespathogènes, c'est pourquoi elle a été utilisée pour communiquer avec le système immunitairesystème immunitaire afin d'obtenir l'effet anti-inflammatoireanti-inflammatoire souhaité. L'acide hyaluronique, un composant naturel de l'organisme, a été choisi pour sa biocompatibilité et son effet inhibiteur de la croissance bactérienne.
L'originalité du film vient également du fait qu'il embarque des peptidespeptides antimicrobiens naturels, en particulier la catéstatine, pour empêcher d'éventuelles infections autour de l'implant. Ceux-ci constituent une alternative aux antibiotiques actuellement utilisés. En plus d'avoir une activité antimicrobienne importante, ces peptides sont peu toxiques pour l'organisme qui en sécrète également. Ils sont capables de tuer les bactéries en créant des trous dans leur paroi cellulaire tout en empêchant une contre-attaque de leur part.
Philippe Lavalle, directeur de recherche à l'Inserm, explique les risques d'infection liés à la pose d'un implant médical et présente sa découverte. © Inserm vidéos, YouTube
Des peptides antimicrobiens sur une fine couche d’argent
Dans cette étude parue dans la revue Advanced Healthcare Materials, les chercheurs montrent que la poly(arginine) associée à l'acide hyaluronique possède une activité antimicrobienne contre le staphylocoque doré pendant plus de 24 heures. « Pour prolonger cette activité, nous avons déposé sur l'implant en titanetitane un précurseur à base d'argentargent avant l'apposition du film. L'argent est une substance anti-infectieuse actuellement utilisée sur les cathéterscathéters et les pansements. Cette stratégie nous a permis d'obtenir une activité antimicrobienne à long terme », explique Philippe Lavalle, directeur de recherche Inserm.
Les résultats des nombreux tests réalisés sur ce nouveau film révèlent qu'il limite l'inflammation et prévient les infections bactériennes et fongiques les plus courantes.
Les chercheurs montrent qu'au contact du sang humain, la présence du film sur l'implant supprime l'activation des marqueurs de l'inflammationinflammation produits en temps normal par les cellules du système immunitaire en réaction à l'implantation. D'autre part, « en présence de bactéries staphylocoques (Staphylococcus aureus), d'une souche de levure (Candida albicans) ou de champignon (Aspergillus fumigatus) à l'origine d'infections fréquentes associées à l'implant, le film inhibe leur croissance et leur prolifération à long terme », souligne Philippe Lavalle.
Selon les chercheurs, ce film pourrait, d'ici quelques années, être utilisé in vivoin vivo sur les implants ou dispositifs médicaux pour contrôler le micro-environnement complexe autour des implants et protéger l'organisme des infections.