au sommaire
L’épilepsie est la deuxième maladie neurologique la plus fréquente après la migraine. © DR
- Pour tout savoir sur l'épilepsie, consultez notre dossier

L'épilepsie du lobe temporaltemporal est la forme d'épilepsie la plus fréquente chez l'adulte. Elle apparaît le plus souvent après une agression du cerveau comme un traumatisme crânien ou une infection de type méningite. Christophe Bernard, directeur de recherche Inserm et son équipe marseillaise (Unité Inserm 751 « Épilepsie et cognition »), en collaboration avec une équipe américaine, viennent de découvrir un gènegène clé dans le mécanisme de la transformation d'un cerveau sain en cerveau épileptique.
Ce gène activé suite à l'agression initiale du cerveau contrôle l'expression de 1.800 autres gènes dont les dérèglements participeraient à la constructionconstruction d'un cerveau épileptique. En empêchant l'activité de ce « gène interrupteur » chez des rats, les bénéfices thérapeutiques sont immédiats. Ces travaux font l'objet d'une publication dans la revue Annals of Neurology.
Cette vidéo explique l'apparition de l'épilepsie, ses conséquences dans le cerveau et le mode de fonctionnement du gène interrupteur : en position « off » dans un cerveau sain, il se met en position « on » dans un cerveau qui subit une agression et provoque l'hyperactivité. © Inserm
À l'origine de la maladie, une agression du cerveau
L'épilepsie est la maladie neurologiquemaladie neurologique la plus fréquente après la migraine. Elle touche 1 à 2 % de la population mondiale. L'épilepsie du lobe temporal (ELTELT) est la forme d'épilepsie la plus fréquente chez l'adulte. Elle est résistante à tout traitement pharmacologique dans 30 % des cas. De plus, l'ELT est souvent associée à des déficits de mémoire et d'apprentissage ainsi qu'à des états dépressifs ou anxieux. Ces désordres sont souvent vécus par les patients comme étant plus invalidants que les crises d'épilepsiecrises d'épilepsie elles-mêmes.
L'épilepsie du lobe temporal a souvent comme origine une agression du cerveau (méningite, traumatisme crânien, etc.). Des dizaines d'années peuvent s'écouler entre cette agression et l'apparition des premières crises. Cet intervalle libre permet d'envisager la recherche de traitements préventifs. Mais pour cela, il est essentiel de déterminer les mécanismes qui sont responsables de la transformation d'un cerveau « sain » en cerveau « épileptique » après une agression.

L'épilepsie se déclenche suite à une agression du cerveau. © pratis.com
Des milliers de gènes impliqués
La recherche fondamentale a montré qu'une agression initiale du cerveau conduit à une réorganisation considérable des réseaux de neuronesneurones qui le composent. Cette réorganisation est responsable de l'apparition des crises et des désordres associés, comme les déficits de mémoire. Un des éléments les plus frappants de cette réorganisation est une modification de l'expression de milliers de gènes qui déterminent l'organisation fonctionnelle des cellules du cerveau.
Chaque gène modifié constitue donc une cible thérapeutique potentielle. C'est la direction prise par la recherche fondamentale et pharmaceutique pendant de nombreuses années. Restaurer la fonction d'un gène pourrait être suffisant pour empêcher le développement de l'épilepsie. Mais ce type de stratégie - cible unique - n'est pas très efficace.
L'équipe « Épilepsie » dirigée par Christophe Bernard de l'Unité Inserm U751 à La Timone (Marseille), en collaboration avec une équipe américaine (Tallie Z. Baram, Université de Californie à Irvine) a voulu comprendre les mécanismes responsables de la réorganisation des gènes. « L'idée est que plus on agit en amont, plus le traitement sera efficace » déclare le chercheur français.
Contrôler le gène NRSF permettrait de maîtriser l'épilepsie. © Inserm
Un gène qui en contrôle 1.800 autres
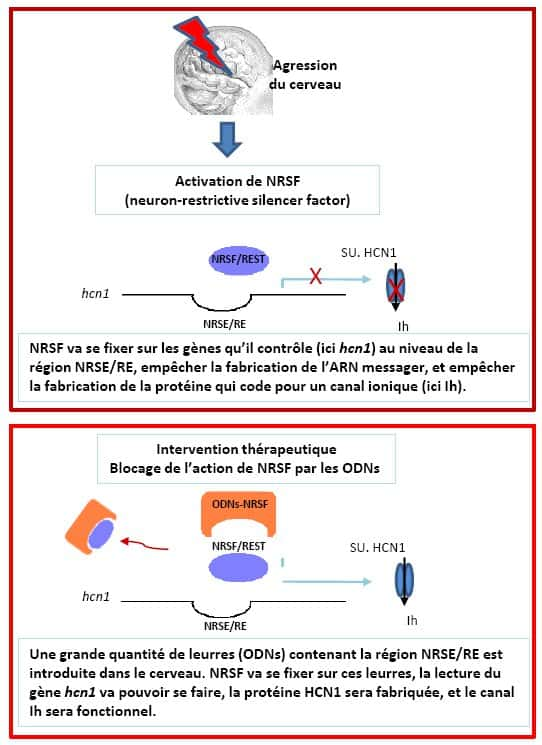
Les auteurs de l'étude ont identifié un gène qui est activé par l'agression initiale, et qui a la capacité de contrôler l'expression de 1.800 autres gènes. Ce gène s'appelle NRSF (NeuronNeuron Restrictive Silencing Factor). La protéineprotéine NRSF ainsi générée va recruter d'autres protéines qui vont empêcher la lecture de l'ADN au niveau de certains gènes, et donc empêcher la production des protéines codées par ces gènes.
En utilisant des modèles animaux d'ELT, ils ont ensuite fabriqué et injecté des leurres chimiques (des peptidespeptides appelés oligodéoxynucléotides) qui captent et fixent la protéine NRSF produite, empêchant ainsi son action sur ses gènes cibles. Ce traitement permet de restaurer l'expression des gènes bloqués par NRSF, de restaurer la production des protéines codées par ces gènes, et les fonctions assurées par ces protéines.
Ces leurres chimiques, injectés chez les animaux, ont un effet thérapeutique important : ralentissement de la progression de l'épilepsie, diminution du nombre de crises, et restauration d'une activité cérébrale (rythme thêta) qui joue un rôle central dans de nombreuses fonctions de mémorisation et d'apprentissage.
Il s'agit de la première identification d'un interrupteur majeur responsable de la transformation d'un cerveau « sain » en cerveau « épileptique » ; ce qui ouvre la voie aux traitements préventifs chez les personnes risquant de développer une épilepsie suite à une agression du cerveau.
Contact chercheur :
- Christophe Bernard
- Unité Inserm 751 "Épilepsie et cognition"