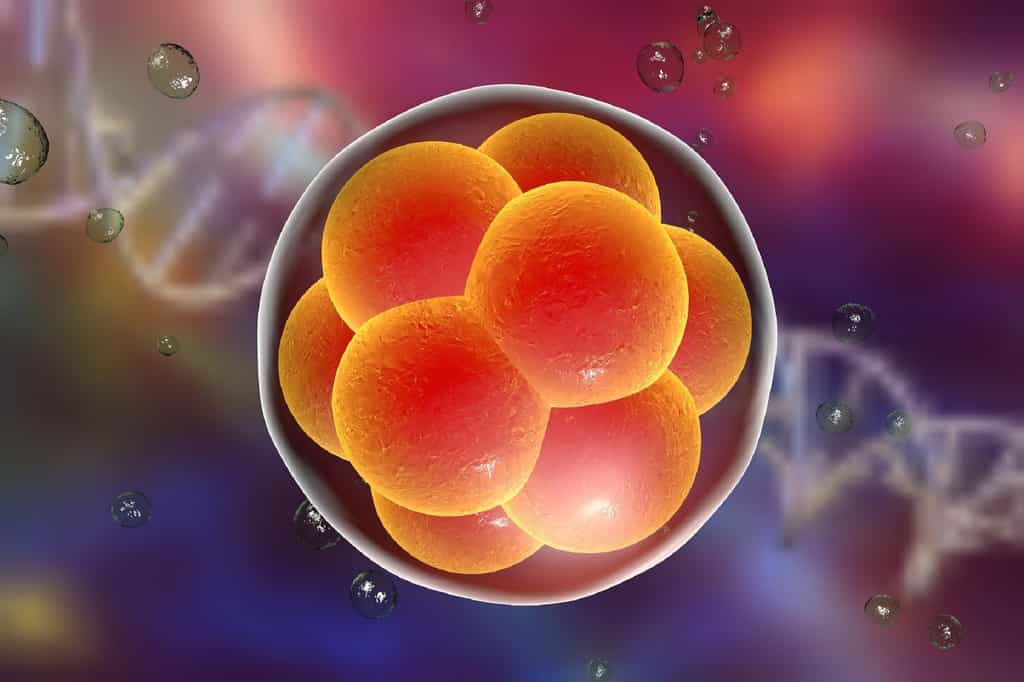
Des chercheurs ont montré qu'il était possible de supprimer une mutation responsable d'une maladie cardiaque grave chez des embryons humains. Ces travaux suscitent de nouveau un débat éthique à propos de l'utilisation de l'édition génomique en médecine reproductive et ses dérives possibles.
au sommaire
Les maladies génétiques affectent des millions de personnes dans le monde. Certaines sont dues à des mutations dominantes, c'est-à-dire qu'une seule version mutée du gène suffit à transmettre la maladie. C'est le cas de la mutation MYBPC3 qui cause la cardiomyopathie hypertrophique, une maladie cardiaque connue pour provoquer des décès brutaux chez de jeunes sportifs. Comme ces mutations ne donnent pas de symptômes durant l'enfance mais plus tard, à l'âge adulte, elles peuvent se transmettre facilement d'une génération à une autre.
Pour empêcher la transmission de mutations des parents aux enfants, une solution peut être d'utiliser le diagnostic préimplantatoire et de sélectionner des embryonsembryons non mutés pour la Fivete. Si un parent porteporte une mutation dominante, 50 % des embryons seront bons pour le transfert. Mais si l'on pouvait corriger le gène défectueux, il serait possible d'augmenter le nombre d'embryons implantables, et donc les chances de grossessegrossesse.
Pour la première fois aux États-Unis, des chercheurs ont réussi la prouesse consistant à corriger un gène dans un embryon humain : c'est une première dans ce pays. Lors de cette expérience, ils se sont servis des techniques de l'édition génomiqueédition génomique, avec les ciseaux moléculaires CRISPR-Cas9CRISPR-Cas9. Les chercheurs ont utilisé les ovocytesovocytes de 12 femmes en bonne santé et les spermatozoïdesspermatozoïdes d'un homme qui portait la mutation MYBPC3, responsable de la cardiomyopathie hypertrophique.

Une modification du gène responsable de la maladie
Quand le spermatozoïde a été injecté dans l'ovocyte, les chercheurs ont modifié le gène responsable de la maladie. Les cassures double brindouble brin dans le gène du père ont été réparées avec le gène sain de la mère plutôt qu'avec un ADNADN synthétique. L'embryon ne s'est développé que quelques jours et il n'était pas prévu de l'implanterimplanter pour une grossesse. Les résultats paraissent dans Nature.
Quand l'embryon s'est divisé et que les cellules se sont multipliées, beaucoup d'entre elles semblaient avoir intégré la copie saine du gène, venant de la mère. Environ 72 % auraient été corrigées, ce qui est plutôt élevé. D'après les chercheurs, il n'y aurait pas eu d'autres modifications hors cible. Ceux-ci affirment avoir réussi à moduler le mosaïcisme (le fait que l'embryon soit une mosaïque de cellules différentes). Ils proposent de minimiser ce risque en co-injectant le spermatozoïde et CRISPR-Cas9 lors de la métaphase II de l'ovocyte.
Le saviez-vous ?
La cardiomyopathie hypertrophique provoque un épaississement du muscle cardiaque. Elle peut rester inaperçue jusqu’à ce qu’elle cause un décès soudain. Il n’existe pas de traitement. La maladie toucherait environ un adulte sur 500. Quand elle n’est pas fatale, celle-ci affecte la qualité de vie (arythmie, insuffisance cardiaque, activité physique limitée, peur d’un décès soudain). Les mutations MYBPC3 représentent 40 % des causes génétiques.
CRISPR suscite des débats éthiques dans la communauté scientifique
La technique employée pourrait s'appliquer à d'autres maladies. D'après le Washington Post, les chercheurs seraient intéressés pour la tester avec le gène BRCA1, dont les mutations favorisent le cancer du seincancer du sein. Ces travaux sont sensibles car ils touchent des cellules de la lignée germinalelignée germinale, et donc des gènes qui pourront être transmis aux générations suivantes. Le Royaume-Uni fait figure de pionnier en la matièrematière : il a autorisé de telles expériences sur les embryons, dans des conditions très encadrées. D'autres pays sont plus réservés. Aux États-Unis, il ne peut pas y avoir de financement public sur de telles recherches. En mars, un rapport parlementaire français a souligné l'intérêt thérapeutique de l'outil CRISPR-Cas9 et s'est prononcé en faveur d'un débat public sur cette question.
Le sujet de la modification des embryons humains suscite un vrai débat éthique. Dans quelle mesure est-il possible d'autoriser des modifications génétiques si celles-ci « corrigent » des gènes ? En 2015, un groupe international de scientifiques avait déjà tiré la sonnettesonnette d'alarme sur les risques liés à l'utilisation de CRISPR pour modifier l'embryon ; car la technique présente aussi des risques à cause des mutations « hors cible » qui peuvent apparaître.
Les premiers travaux de manipulation d'embryons avec CRISPR émanaient de chercheurs chinois qui avaient modifié le gène responsable de la bêta-thalassémiebêta-thalassémie. Toujours en Chine, d'autres expériences ont utilisé la technique pour introduire une résistancerésistance au VIHVIH (voir ci-dessous).
Des chercheurs chinois utilisent de nouveau CRISPR pour modifier des embryons
Article de Marie-Céline Jacquier publié le 13 avril 2016
Des chercheurs chinois ont utilisé l'édition génétique (le système CRISPR-Cas9) pour introduire une résistance au VIH dans des embryons humains. C'est la deuxième publication scientifique qui décrit une telle modification génétique, un an après une première mondiale, déjà en Chine, en avril 2015.
Le système CRISPR-Cas9 est un outil puissant d'édition génétique qui a été appliqué avec succès pour modifier les génomesgénomes de différentes espècesespèces. Depuis un an, cette technique suscite la controverse dans la communauté scientifique en raison de son applicationapplication possible à l'espèce humaine. En avril 2015, une équipe chinoise avait annoncé avoir modifié un gène lié à une maladie du sang dans des embryons humains non viables. Cet article, qui décrivait une première mondiale, avait suscité beaucoup d'interrogations éthiques, et des scientifiques avaient appelé à un moratoire sur ces expériences.
À l'époque, des rumeurs couraient que d'autres équipes faisaient le même type d'expériences. Un nouvel article paru dans Journal of Assisted Reproduction and Genetics en apporte la preuve. Les chercheurs ont cette fois voulu tester la technologie CRISPR-Cas9 pour introduire une autre modification génétique dans des embryons humains. Ces embryons non viables ont été détruits au bout de trois jours. Il s'agit seulement du deuxième article publié sur l'édition génétique dans des embryons humains.
L'équipe de Yong Fan, de l'université médicale de Canton, en Chine, a récupéré 213 embryons humains entre avril et septembre 2014. Ces embryons provenaient de 87 patientes et ne pouvaient pas être utilisés pour une implantation dans le cadre d'une FIV (fécondation in vitro) car ils contenaient un jeu supplémentaire de chromosomeschromosomes. L'équipe a utilisé le système CRISPR-Cas9 pour introduire une mutation dans le gène CCR5, qui code pour une protéineprotéine indispensable à l'entrée du VIH dans les globules blancsglobules blancs. La mutation CCR5Δ32, portée naturellement par certaines personnes résistantes au virusvirus VIH, altère la protéine CCR5 d'une telle façon qu'elle empêche l'entrée du virus dans la cellule.
Le débat bioéthique sur l’utilisation de CRISPR-Cas9 se poursuit
Quatre embryons sur 26 ont été modifiés avec succès, mais tous les chromosomes ne portaient pas la mutation. Plusieurs scientifiques internationaux expriment dans Nature leur scepticisme vis-à-vis de la nécessité de réaliser de telles expériences, comme George Daley, un biologiste du Children's Hospital, à Boston, aux États-Unis : « Cet article ne semble pas offrir bien plus que des preuves anecdotiques que cela fonctionne dans les embryons humains, ce que nous savions déjà ».
Pour Xiao-Jiang Li, neuroscientifique à l'université Emory (Atlanta, États-Unis), cet article « souligne simplement qu'il y a encore beaucoup de difficultés techniques pour faire de l'édition précise dans les cellules d'embryon humain ». Il pense que les chercheurs devraient plutôt essayer de résoudre ces difficultés techniques chez des primatesprimates non humains, au lieu de continuer à modifier le génome humain avec CRISPR-Cas9.
Tetsuya Ishii, spécialiste de bioéthique de l'université Hokkaido, à Sapporo, au Japon, ne voit pas de problème dans la façon dont ces expériences ont été menées, car un comité d'éthique local les a approuvées. Toutefois, il s'interroge lui aussi sur la nécessité de ces expériences : « Introduire CCR5Δ32 et essayer de réparer, même dans des embryons non viables, c'est tout simplement jouer avec des embryons humains ».
En février dernier, les autorités britanniques ont donné leur accord pour des expériences de modification d'embryons humains. Ces recherches, menées par Kathy Niakan à l'Institut Francis CrickFrancis Crick de Londres, ont pour but d'inactiver des gènes impliqués dans le développement précoce de l'embryon dans l'espoir de mieux comprendre pourquoi certaines grossesses s'arrêtent spontanément. Ce travail sera réalisé dans des embryons viables mais les chercheurs devront arrêter les expériences au bout de 14 jours. Le travail de Kathy Niakan vise à répondre à des questions sur l'embryologie, alors que celui de l'équipe de Yong Fan est de montrer comment générer un individu résistant au VIH. Deux objectifs bien différents donc. L'édition génétique n'a probablement pas fini de faire parler d'elle...
Ce qu’il faut
retenir
- L'outil d'édition du génome CRISPR-Cas9 permet de modifier génétiquement des embryons.
- Il a servi à corriger le gène responsable d'une maladie cardiaque mortelle.
- En Europe, le Royaume-Uni a déjà autorisé ces modifications controversées de l'embryon humain pour des recherches très précises.