Fabriquer des neurones à partir de cellules de la peau ? L'opération est réalisable depuis quelques années déjà. Il est en effet possible de reprogrammer des cellules de peau en cellules souches particulières, appelées cellules souches pluripotentes induites (CSPiCSPi). Celles-ci peuvent ensuite être utilisées pour fabriquer n'importe quel type de cellules différenciées telles que des neurones ou des globules rouges.
Dans une étude publiée dans Cell Reports, l'équipe de Su-Chun Zhang, professeur de neurosciences à l'université du Wisconsin à Madison, est allée encore plus loin : reprogrammer des cellules de peau d'un singe en cellules nerveuses, puis les transplanter dans son cerveau !

Le singe rhésus est souvent utilisé dans les recherches médicales. L’un d’entre eux a été cloné pour la première fois en janvier 2000. © J. M. Garg, Wikimedia Commons, cc by sa 3.0
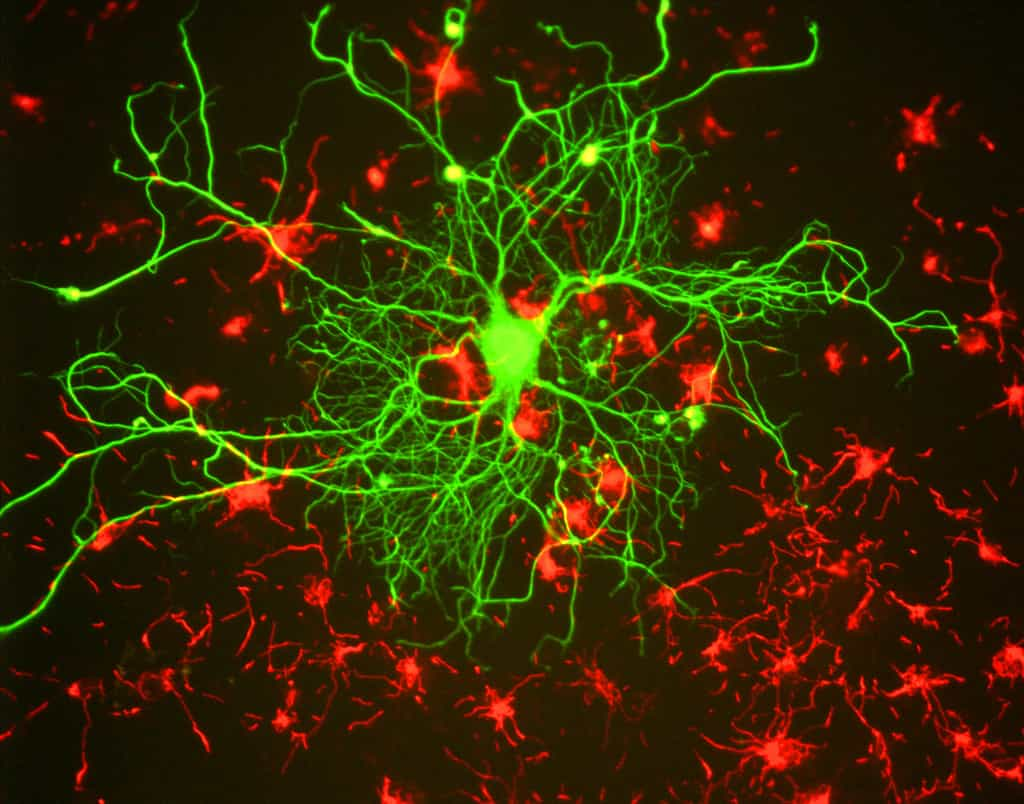
Pour réaliser l'expérience, trois singes rhésus atteints de la maladie de Parkinson ont été utilisés. Des cellules de peau ont tout d'abord été extraites et rendues fluorescentes par la production de protéine GFP (green fluorescent proteingreen fluorescent protein). Les auteurs les ont ensuite reprogrammées en cellules neuronales primitives, puis les ont transplantées à l'intérieur du cerveau des trois singes.
Des neurones fonctionnels à partir de cellules de la peau
Leurs résultats sont prometteurs : une fois implantées dans le cerveau, les cellules neuronales primitives ont achevé leur stade de différenciation en neurone ou en cellule gliale. D'autre part, au bout de 6 mois, les neurones implantés avaient un aspect normal et possédaient de longs axonesaxones caractéristiques. Selon le professeur Su-Chun Zhang, « le cerveau de ces singes ressemble à un cerveau normal, et l'on ne peut se douter qu'il a subi une greffegreffe ». Leur aspect suggère donc qu'ils ont correctement maturé et ne sont pas cancéreux. Ces résultats ont pourtant leur limitation : le nombre de cellules transplantées n'était pas suffisant pour permettre la fabrication de cellules productrices de dopamine, le neurotransmetteurneurotransmetteur qui se trouve en quantité trop limitée chez les personnes atteintes de la maladie de Parkinsonmaladie de Parkinson. De ce fait, le comportement des singes malades ne s'est pas amélioré au cours de cette expérience.
Une des grandes forces de cette technique repose sur l'utilisation de cellules de peau d'un malade pour soigner ses propres lésions cérébrales. Elle limiterait donc considérablement le problème de rejet de greffe. D'autre part, l'absence de signes de cancercancer 6 mois après l'implantation est un résultat très encourageant.
Pourtant, de grands défis scientifiques doivent encore être relevés avant que cette technologie puisse être généralisée. Peut-on estomper les symptômessymptômes de la maladie ? Que se passe-t-il après 6 mois ? Y a-t-il des effets secondaires associés à la greffe ? Néanmoins, ces nouvelles avancées prometteuses nous rapprochent un peu plus d'un traitement destiné à combattre les maladies dégénératives telles qu'Alzheimer et Parkinson.