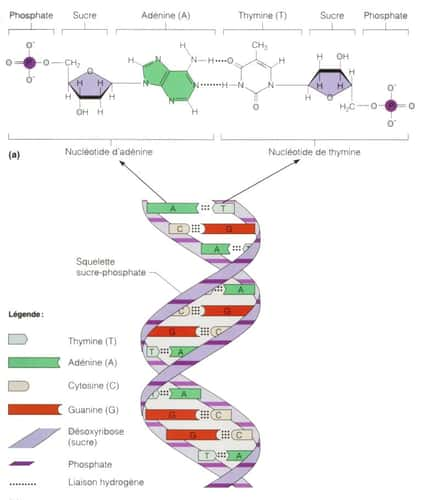
au sommaire

Même encore dans le ventre de leur mère, les enfants peuvent bénéficier d'une analyse de leur génome. © DR
Avant la naissance, il est déjà possible de détecter certaines maladies génétiques du fœtus. Actuellement, les techniques utilisées sont l'amniocentèse, qui consiste en un prélèvement du liquide amniotique, entourant le fœtus, à l'aide d'une longue seringue, ou un prélèvement placentaire. Dans les deux cas, les cellules obtenues sont cultivées afin de réaliser des caryotypes de cellules en division. Bien que très efficaces, ces techniques ne sont pas sans risque pour l'enfant, puisque l'on constate une légère augmentation du nombre de fausses couches suite à ces examens.
Pour éviter ces risques, et aller plus loin dans l'identification des gènesgènes malades, une nouvelle technique de séquençage de l’ADN fœtal a été développée et publiée tout récemment dans la revue Science Translational Medicine par des chercheurs de l'université chinoise d’Hong Kong. Elle consiste en un simple prélèvement sanguin de la mère !
L'ADN du fœtus est présent dans le sang maternel
En effet, au cours de la grossessegrossesse, environ 10 % de l'ADNADN circulant dans les veines de la future maman proviennent du fœtus, suite à la mort de certaines cellules du fœtus ou du placentaplacenta. Ce fait est connu depuis plus de 10 ans, ce qui a permis aux scientifiques de développer des moyens de déterminer quelques caractéristiques de l'enfant. Cela est déjà possible puisqu'il suffit de détecter un gène que l'on sait absent de la mère, pour savoir qu'il provient du père et donc appartient à l'enfant : un morceau de chromosomechromosome Y indique que l'enfant est un garçon et la présence du gène antigènique D (spécifique aux individus rhésus positif) chez une mère rhésus négatif prouve qu'il est rhésus positif.
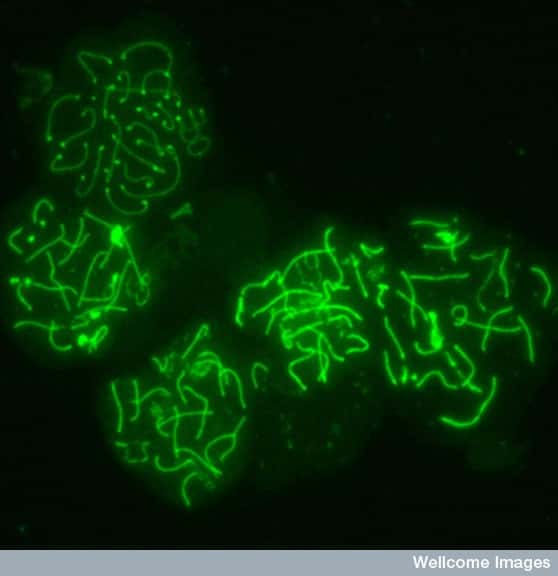
ADN de cellules de souris en méiose. La méiose permet une recombinaison des chromosomes lors de la fabrication des gamètes, et modifie donc l'organisation des allèles. © MRC NIMR, Wellcome Images
Mais lorsque la future maman est hétérozygotehétérozygote pour un gène, comment savoir si l'enfant porteporte lui-même deux versions différentes du gène ou au contraire, deux identiques ? Il faut pour cela réussir à différencier d'une manière ou d'une autre l'ADN de l'enfant de celui de la mère. C'est le défi qu'on relevé avec brio les scientifiques chez une mère dont l'enfant risquait de porter deux allèlesallèles malades du gène HBB codant pour l'hémoglobinehémoglobine, menant à une possible β-thalassémiethalassémie.
Analyse des génomes parentaux
Pour cela, ils ont analysé d'abord les génomesgénomes des deux parents, grâce à l'analyse de l'ADN contenu dans les cellules leucocytaires obtenues par prises de sang. Les polymorphismes (SNPSNP) ont pu être repérés grâce à une puce à ADN, ce qui a permis de mettre en évidence les différences génétiquesgénétiques des deux parents.
Mais les chromosomes de l'enfant ne sont pas les reflets exacts des chromosomes parentaux. La méioseméiose ou recombinaisonrecombinaison permet un subtil mélange des deux chromosomes de la mère et des deux chromosomes du père lors de la fabrication des gamètesgamètes. L'organisation de la suite de gènes au sein d'un chromosome, ou haplotypehaplotype, varie.
Une réussite mais pas de généralisation
Malgré ces complications, leur méthode complexe de dosagedosage relatif des haplotypes dans le sang de la mère, confirmée par les résultats du séquençage du génome de l'enfant grâce au prélèvement d'un échantillon de placenta, semble être une réussite. Plus de 94 % du génome du bébé a pu être identifié et séquencé, menant à la conclusion que le fœtus possède heureusement une version correcte de l'allèle, et n'est donc pas atteint de β-thalassémie.
Que faut-il espérer de cette nouvelle technique ? Elle est efficace et sans danger particulier, mais elle a aussi un coût, en temps, en personnel et en matériel. La grande quantité d'informations obtenues est en soi un progrès, mais revient également aussi à chercher une aiguille (une mutation inconnue) dans une botte de foin (un génome de 4 milliards de paires de bases). Il n'est donc pas encore prévu de généraliser cet examen, mais le développement très rapide des technologies laisse envisager qu'une applicationapplication sera peut-être possible dans le futur.