Le passage chez le dentiste sera bientôt une partie de plaisir ! Plutôt que de cureter le tartre avec des instruments agressifs, des microrobots se chargeront de décomposer la plaque bactérienne de manière ciblée et d’éliminer les résidus pour prévenir sa formation. Un dispositif très efficace et applicable à n’importe quelle surface confinée comme les sondes ou les cathéters.
au sommaire
Bactéries, sucre et salive forment un redoutable enduit collant qui se dépose sur les dents et se calcifie pour se transformer en tartretartre. Non éliminé, celui-ci peut entraîner caries, gingivites voire déchaussement dentaire. Pour éliminer cette plaque dentaire, le dentiste va devoir curer manuellement les dépôts, utiliser des ultrasonsultrasons ou polir les dents avec de l'eau sableuse. Des opérations pas franchement agréables et laborieuses.
Des biofilms très collants
Et si demain une armée de microrobots se chargeait du travail ? Une équipe de chercheurs de l'université de Pennsylvanie vient ainsi de mettre au point des microrobots chargés de nettoyer les dents avec une redoutable efficacité. À l'origine, leur invention visait plutôt les tubes et espaces confinés comme les canalisationscanalisations, les sondes ou les cathéterscathéters médicaux. Des endroits où les biofilms bactériens sont particulièrement résistants aux traitements antimicrobiens car ils collent au support, provoquant infections et dégradation des surfaces.
Une astucieuse alliance de la santé et de l’ingénierie
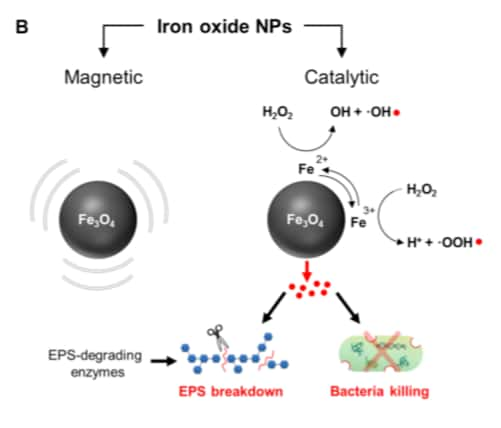
L'invention est un remarquable exemple de comment l'interdisciplinaritéinterdisciplinarité peut faire avancer la science. Hyun Koo, chercheur au département de médecine dentairemédecine dentaire et principal auteur de l'étude publiée dans la revue Science Robotics le 24 avril, avait précédemment expérimenté plusieurs solutions contre ces biofilms, dont une solution à base de nanoparticulesnanoparticules d'oxyde de ferfer. Ces dernières catalysent la réaction avec le péroxyde d'hydrogènehydrogène pour libérer des radicaux libres qui décomposent la matrice d'exopolysaccharides du biofilm. Il s'est un jour aperçu que ses collègues de l'école d'ingénierie et de sciences appliquées utilisaient ces mêmes nanoparticules de fer pour élaborer des microrobots que l'on peut diriger par champ magnétiquechamp magnétique.
Un « chasse-neige » qui racle la plaque dentaire
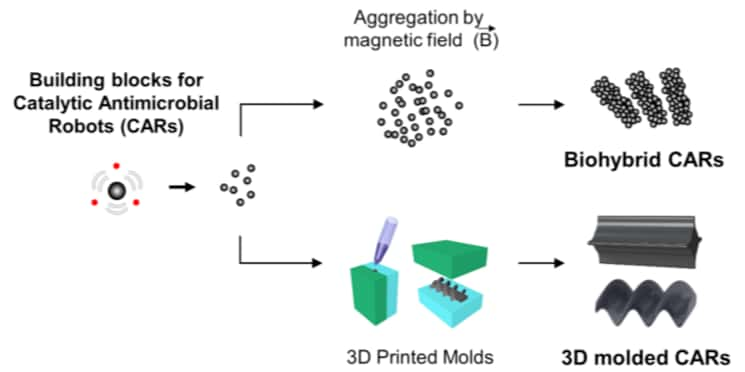
Les deux équipes ont alors décidé de rapprocher leurs savoir-faire pour mettre au point des microrobots à double fonction, catalytique et magnétique, capables de cibler précisément les biofilms. Deux types de ces robotsrobots antimicrobiens catalytiques (RAC) ont été développés. Le premier consiste à suspendre des particules d'oxyde de fer dans une solution, celle-ci pouvant alors être dirigée par des aimantsaimants pour éliminer le biofilm à la manière d'un chasse-neige. « Ces RAC biohybrides peuvent ainsi être balayés sur des larges bandeslarges bandes ou sur une trajectoire bien définie pour une élimination localisée à l'échelle microscopique », assure Hyun Koo. Le second type de robot implique l'incorporation des nanoparticules dans un gelgel polymèrepolymère, moulé en 3D dans une forme personnalisée à l'endroit que l'on souhaite traiter. « Les RAC en forme d'ailettes conviennent par exemple aux courbes des tubes cylindriques, tandis que ceux en hélice peuvent percer un biofilm qui obstrue un canal », illustre le chercheur.
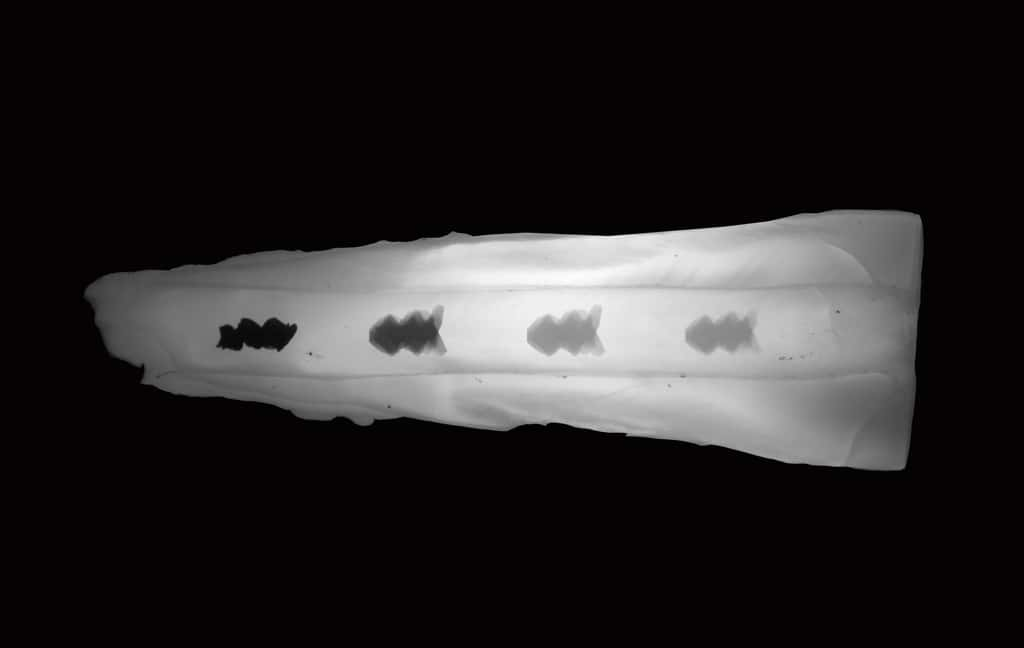
Atteindre des endroits de la dent jusqu’ici inaccessibles
L'équipe a testé les RAC sur des tubes et plaques en verre avant de les appliquer sur les dents. Ils se sont avérés particulièrement efficaces pour éliminer les biofilms bactériens, non seulement à la surface de la dent mais aussi à des endroits habituellement inaccessibles aux outils du dentiste, comme les canaux radiculaires situés à la racine de la gencive où s'accumulent les bactéries. « Les traitements existants sont inefficaces parce qu'ils sont incapables de dégrader simultanément la matrice protectrice du biofilm, de tuer les bactéries incrustées et d'éliminer les résidus, explique Hyun Koo. Nos robots peuvent faire les trois à la fois, ne laissant absolument aucune trace du biofilm. » Débarrasser les dents des restes de la dégradation diminue ainsi le risque que la plaque ne se redépose dessus. Les chercheurs espèrent déboucher rapidement sur une applicationapplication clinique.
Ce qu’il faut
retenir
- Des microrobots à base de nanoparticules d’oxyde de fer peuvent éliminer les biofilms bactériens tout en étant dirigés précisément par des aimants.
- Selon les configurations, ils permettent d’éliminer efficacement les biofilms sur des surfaces confinées.
- Les applications visent non seulement la plaque dentaire, mais aussi les sondes et les cathéters particulièrement sujets aux infections bactériennes.