La campagne de vaccination contre le SARS-CoV-2 fait partie de celles qui ont connu une ampleur inédite dans le monde. Des chercheurs s'interrogent sur la façon dont ces biotechnologies modifient l'évolution des agents pathogènes.
au sommaire
Bien loin de la désinformation alarmiste anti-vaccination qui suggérait que les vaccins allaient faire émerger un virus plus dangereux et plus létal, des chercheurs en mathématiques et en biologie se demandent comment la vaccination, cette biotechnologiebiotechnologie qui fait désormais partie intégrante de nos vies, va influencer l'évolution des agents pathogènes. Ils proposent des catégories conceptuelles pour définir et étudier l'adaptation d'un virus à son environnement en se concentrant spécifiquement sur le cas de la pandémie de Covid-19. Ils publient leur essai, actuellement non revu par les pairs, dans la revue Public Library of Science in Biology.
Comprendre l'évolution d'un agent pathogène
Tout d'abord, les chercheurs proposent une définition assez classique de la façon dont on peut considérer l'adaptation d'un agent pathogène à son environnement : soit en considérant le taux de croissance absolu, c'est-à-dire le nombre moyen de personnes que le variant a infecté, soit en considérant le taux de croissance relatif, c'est-à-dire en comparant le taux de croissance absolu au taux de croissance absolu du variant d'origine. Le premier indicateur informe sur la diffusiondiffusion du variant dans la population et sa capacité à infecter ses hôtes tandis que le second indique si une souche tend à devenir dominante.
Nous savons désormais que pour qu'un variant se répande, son taux de croissance - le fameux R - doit être supérieur à 1. Pour qu'un variant en remplace un autre, c'est le même principe avec le coefficient de sélection S : s'il est supérieur à 1, le variant va probablement devenir dominant. Ce qui détermine ces deux chiffres, ce sont toujours la proportion d'individus dits naïfs et immunisés. Dès lors, un variant peut être plus ou moins adapté à un type de population précis et sa propension à se répandre au sein d'une de ces populations permet de savoir dans quel environnement un variant donné est dit adapté.
Quatre types de variants
Afin de s'adapter, les variants exploitent plusieurs mécanismes : l'évasion immunitaire (en changeant d'antigène, en supprimant leur antigène, en élargissant leur répertoire d'antigène ou encore en accroissant l'infection entre les cellules), la suppression immunitaire (entrave de la sécrétionsécrétion d'enzymesenzymes, production de moléculesmolécules régulatrices d'immunitéimmunité, production de molécules conduisant à une réponse immunitaire inappropriée, production de molécules « écran de fumée » qui vont distraire le système immunitairesystème immunitaire) et l'exploitation immunitaire (infection dépendante des anticorpsanticorps). D'autres facteurs peuvent également entrer en jeu comme la vitessevitesse de réplicationréplication des variants (une grande vitesse peut submerger la réponse immunitaire tandis qu'une faible vitesse peut contribuer à une infection plus ou moins chronique en restant sous le seuil de détection du système immunitaire).
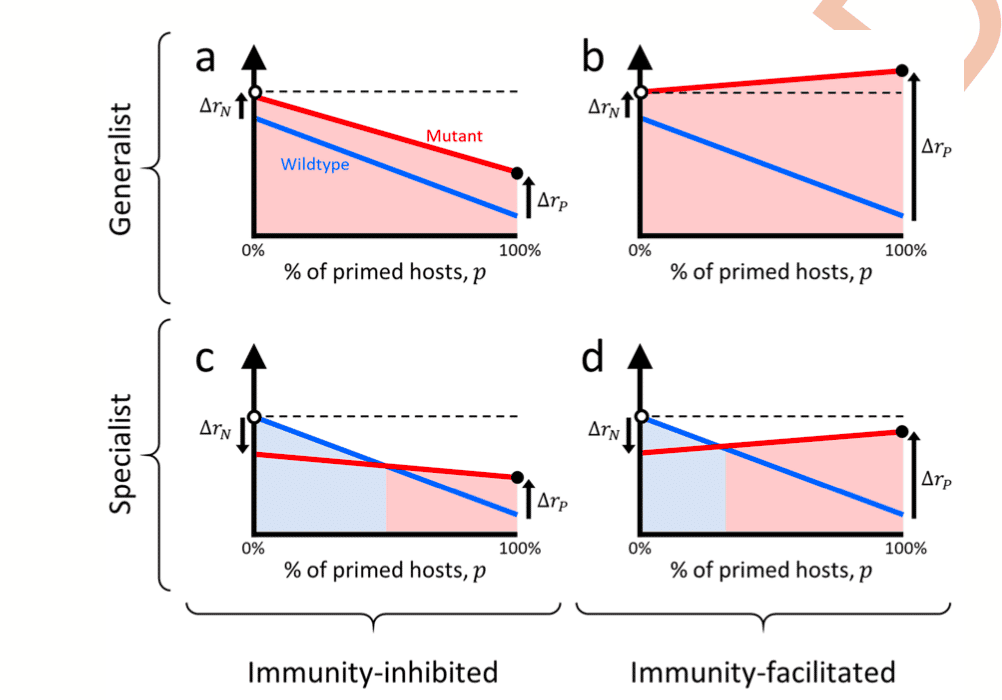
Toutes ces considérations mènent les auteurs à conceptualiser deux grandes familles de variants pathogènes : les « généralistes » et les « spécialistes ». Imaginons un variant qui se serait adapté à l'aide de certains mécanismes immunitaires cités ci-dessus et également adapté à une population naïve, alors on pourra dire que ce variant est généraliste, c'est-à-dire que sa propagation sera meilleure que celle de la souche originelle, peu importe le type de population considérée. En revanche, si un variant est uniquement adapté à des populations déjà immunisées, on pourra dire que ce variant est spécialiste, c'est-à-dire que sa propagation sera meilleure que la souche originelle dans les populations déjà immunisées.
Au sein de ces deux familles, on peut aussi se demander si l'immunité va inhiber ou faciliter l'infection. Pour rendre compte de cette spécificité, les auteurs créent deux autres catégories : les variants inhibés par l'immunité et les variants facilités par l'immunité. Tandis que le taux de croissance des premiers va diminuer au fil des infections ou d'une campagne de vaccination, celui des seconds va probablement augmenter.
Comment la vaccination impacte-t-elle l'évolution des virus ? Le cas du SARS-CoV-2
Avant de parler des hypothèses des auteurs concernant les différents variants du SARS-CoV-2SARS-CoV-2, il est important de rappeler que la plupart des vaccins entravent l'évolution et l'adaptation des agents pathogènes pour deux grandes raisons : en tant qu'intervention prophylactique, le vaccin limite la réplication du virus au sein de l'hôte, donc le nombre de générations et donc la transmission ; aussi, les vaccins induisent généralement une réponse immunitaire large contre le virus et de multiples changements génétiquesgénétiques sont généralement nécessaires pour s'adapter à l'immunité conférée par un vaccin.
Concernant le SARS-CoV-2, les chercheurs suggèrent que les variants Alpha et DeltaDelta entrent dans la catégorie des « généralistes » inhibés par l'immunité. En effet, Alpha et Delta semblent, selon les données épidémiologiques, s'être autant répandus dans des pays où le taux de vaccination était faible que dans ceux où il était élevé. Cela fait d'eux des généralistes car ils se répandent indépendamment du caractère naïf ou immunisé de la population. En revanche, même si les données sont moins convaincantes, il semble que plus le taux de vaccination augmentait, plus le taux de croissance de ces variants diminuait, d'où la classification de généralistes inhibés par l'immunité.
Omicron, quant à lui, est sans aucun doute un variant spécialiste adapté aux populations immunisées étant donné son apparition tardive lorsque l'immunité acquise par infection naturelle et par la couverture vaccinalecouverture vaccinale était répandue. Les observations préliminaires suggèrent qu'il serait également inhibé par l'immunité. Aucun variant facilité par l'immunité ne semble avoir émergé de la souche originelle du SARS-CoV-2.