Le cœur artificiel Carmat de l'entreprise du même nom vient d'obtenir la certification européenne pour être commercialisé et il est pris en charge forfaitairement par la Sécurité sociale.
au sommaire
Le cœur Carmat de l'entreprise du même nom a obtenu il y a peu la certification européenne pour être commercialisé en Europe et dans certains pays qui acceptent ladite certificationcertification comme gage de qualité. Il a aussi obtenu, il y a peu, un forfait d'innovation.
Qu'est-ce que le cœur Carmat ?
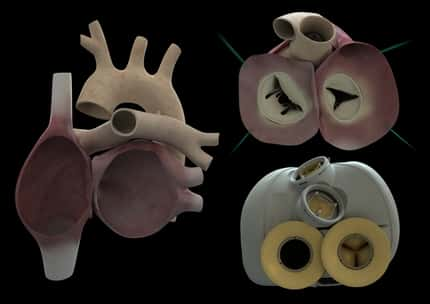
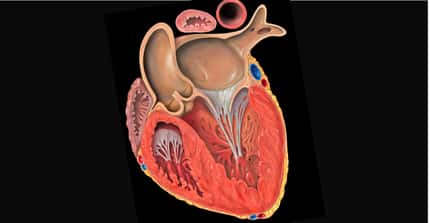
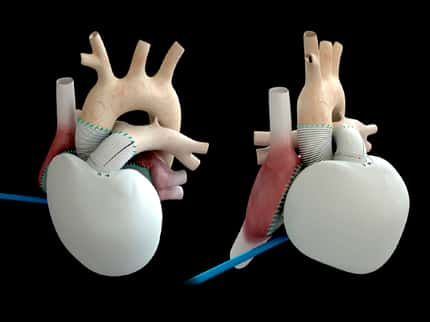
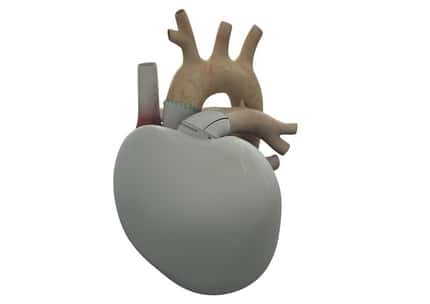
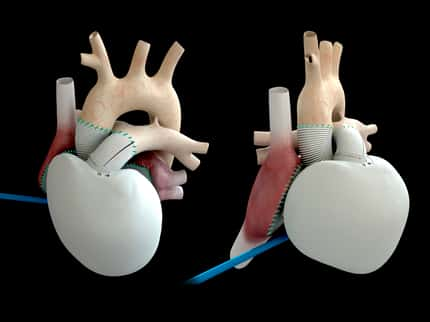
Le cœur artificiel Carmat contient deux chambres, dont chacune est séparée par une membrane en un compartiment sanguin et un compartiment liquideliquide. Ce fluide visqueux, mis en mouvementmouvement par deux pompes électrohydrauliques, actionne les membranes, produisant un écoulement pulsatile. Des capteurs de pressioncapteurs de pression et des composants électroniques qui pilotent le système et s'adaptent aux besoins du patient sont intégrés dans la prothèse. Des valves biologiques sont placées aux entrées et sorties des ventricules. Le cœur artificiel est connecté aux oreillettesoreillettes avec des brides de suture bioprothétique. Les conduits de sortie en Dacron sont suturés sur l'aorte et l'artère pulmonaire. Le dispositif est partiellement recouvert par un sac souple de compliance qui contient le fluide d'actionnement. Une transmission percutanée alimente le cœur artificiel et récupère des informations sur les performances de l'appareil. Dans la configuration actuelle, la transmission est connectée à une console d'hôpital.
Forfait d'innovation et certification européenne
En l'espace de quelques mois, le cœur Carmat a obtenu un forfait d'innovation, suite à l'avis favorable de la Haute autorité de santé le 1er avril 2020, et à l'accord du ministère des Solidarités et de la Santé dans un arrêté du 28 septembre 2020. Le forfait d'innovation en place depuis 2009 est « un pari éclairé sur une innovation à fort potentiel » pour reprendre les mots de la présentation qu'en fait le ministère. Le cœur Carmat va donc être pris en charge selon cet arrêté pendant une duréedurée de 48 mois pour un maximum de 52 patients. La certification européenne permet à l'entreprise de commercialiser son cœur et assure que son produit répond à des exigences dites essentielles, comme le fait que l'utilisation du produit ne compromettra ni l'état clinique ni la sécurité des patients.