Une souche d’un virus commun du rhume, Coxsackie A, montre une efficacité remarquable dans le traitement du cancer de la vessie. Injecté directement dans la tumeur, ce virus se réplique et entraîne une destruction massive des cellules cancéreuses sans affecter les cellules saines. Un gros espoir pour tous les patients atteints de ce cancer, alors que les traitements actuels sont lourds et inefficaces.
au sommaire
L'immunothérapie, qui consiste à stimuler le système immunitaire des patients cancéreux afin que celui-ci s'attaque à la tumeur, fait l'objet de recherches complexes ayant recours à des procédures parfois très compliquées, comme l'immunothérapie par inhibiteur de point de contrôle, l’injection de cytokines, la fabrication de récepteurs CAR-TT, la modification génétique de lymphocytes ou même des bactéries radioactives. Des chercheurs de l'université de Surrey et du Royal Surrey County Hospital de Guildford, au Royaume-Uni, viennent pourtant d'identifier un moyen potentiellement beaucoup plus simple : un simple virus commun du rhume.
« Toutes les traces de la maladie ont disparu après seulement une semaine de traitement »
Quinze patients atteints d'un cancercancer de la vessievessie non invasifinvasif se sont vu injecter un virusvirus Coxsackie A (CVA21), une souche courante du rhume, une semaine avant l'opération chirurgicale programmée pour retirer la tumeur. Le virus a été injecté directement dans la vessie via un cathétercathéter. Les résultats sont allés au-delà des attentes : en analysant les tissus tumoraux retirés, les chercheurs ont constaté que le virus s'était bien infiltré dans les cellules cancéreuses et s'était répliqué, provoquant la mort massive des cellules. Des échantillons d'urine prélevés tous les deux jours ont ainsi révélé une « excrétion » du virus, indiquant que celui-ci continuait à se multiplier et à infecter toujours plus de cellules cancéreuses. Encore mieux : CVA21 s'avère extrêmement sélectif, ne ciblant que les cellules tumorales en laissant intactes les cellules saines. « Chez un des patients, toutes les traces de la maladie ont disparu après seulement une semaine de traitement », s'est même félicité Hardev Pandha, professeur d'oncologie à l'université de Surrey et principal auteur de l'étude parue dans la revue Clinical Cancer Research.
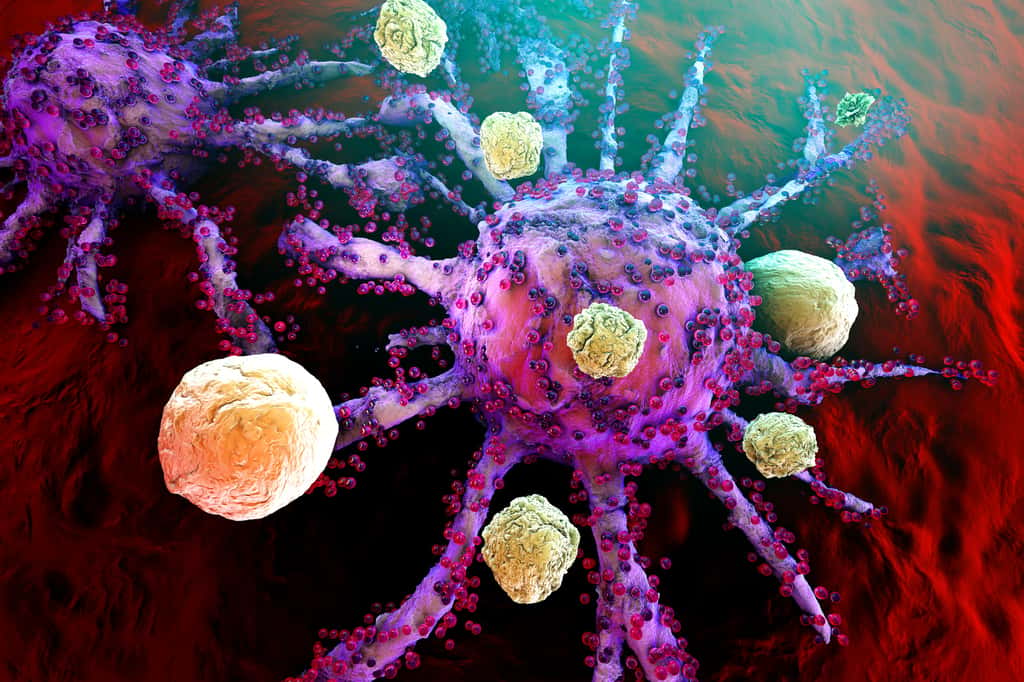
Une « zone chaude » pour attirer les cellules immunitaires
Les tumeurs de la vessie sont d'habitude inaccessibles à l'immunothérapie car elles sont dépourvues de cellules immunitaires, empêchant ainsi la destruction de la tumeur au fur et à mesure qu'elle grandit. Ces tumeurs, dépourvues de cellules immunitaires, sont appelées « zones froides ». Le virus CVA21 crée, lui, une « zone chaude », une inflammationinflammation locale qui entraîne l'affluence des cellules immunitaires dans l'environnement de la cellule. Lorsque la cellule cancéreuse meurt, elle éclate et relâche des milliers de particules virales qui vont alors se propager et cibler d'autres cellules cancéreuses. La lyse des cellules libère également des protéinesprotéines servant d'identifiant au système immunitaire pour qu'il s'attaque aux autres cellules.
Les traitements actuels sont lourds et peu efficaces
Le cancer de la vessie est le 7e cancer le plus courant en France, et touche majoritairement des hommes. On estime que 12.000 nouveaux cas sont diagnostiqués chaque année. Ce cancer est habituellement traité chirurgicalement par résectionrésection transurétrale, une procédure invasive qui présente un taux élevé de récidiverécidive allant de 50 % à 70 %. L'autre traitement courant, l’immunothérapie par Bacille Calmette-Guerin (BCG), entraîne, quant à lui, de graves effets secondaires chez un tiers de patients, un autre tiers ne répondant pas du tout au traitement. C'est dire les espoirs que suscite cette nouvelle piste. « Le Coxsackievirus pourrait révolutionner le traitement de ce type de cancer, assure Hardev Pandha. De plus, il n'entraîne pas le moindre effet secondaire significatif chez aucun des patients », souligne-t-il.
Cette étude n'est pas la première à investiguer les effets du virus CVA21 contre le cancer. Ce dernier a ainsi été identifié comme tueur de tumeurs sur un large éventail de cellules cancéreuses. Le laboratoire Viralytics a ainsi mis au point un traitement nommé Catavak à base de ce virus, dont les essais de phase 2 ont montré une bonne efficacité et une bonne tolérance pour le mélanomemélanome malin. D'autres essais sont en cours pour le cancer de la vessie, du poumonpoumon ou de la prostateprostate.
Un virus pour lutter contre le cancer du pancréas
Article de l'Inserm publié le 21/01/2015
Des chercheurs de l'Inserm ont créé un virus oncolytique capable de détruire les cellules cancéreuses du pancréaspancréas. Après des résultats encourageants in vitroin vitro et in vivoin vivo, la prochaine étape sera de le tester chez l'homme.
Bientôt une nouvelle approche thérapeutique pour lutter contre le cancer du pancréas ? C'est ce qu'espèrent les cliniciens souvent démunis face à ce cancer redoutable. En effet, plus de trois quarts des patients décèdent au cours de l'année qui suit le diagnosticdiagnostic et à peine 2 % sont encore en vie après cinq ans. À Toulouse, une équipe de l'Inserm étudie la faisabilité d'un traitement reposant sur l'injection de virus oncolytique, c'est-à-dire capable d'infecter et de détruire spécifiquement les cellules cancéreuses.
L'idée n'est pas nouvelle et plusieurs autres équipes à travers le monde ont déjà testé certains virus dans différents cancers. Cette fois, les chercheurs de l'Inserm ont travaillé avec un virus dérivé d'Herpes simplex, rendu inoffensif vis-à-vis des cellules saines de l'organisme mais capable de se répliquer spécifiquement dans les cellules cancéreuses du pancréas et de les détruire. Cette prouesse a nécessité de nombreux remaniements du génomegénome viral. L'objectif : rendre l'expression de protéines virales (impliquées dans la réplicationréplication et la toxicitétoxicité) dépendante de la présence d'un gènegène actif uniquement dans les cellules cancéreuses du pancréas. Ce virus modifié est actuellement licencié par une entreprise privée et produit par une société de biotechnologiebiotechnologie française.
Une efficacité démontrée in vitro et in vivo
In vitro, le virus se comporte comme attendu : il n'affecte pas les cellules saines du pancréas mais se multiplie dans les cellules cancéreuses, se propage dans les cellules malades voisines et les élimine. Les chercheurs ont donc fait le test in vivo, sur des tumeurs humaines greffées à des souris. Une unique injection du virus modifié, associée à une chimiothérapie, a drastiquement réduit la taille des tumeurs, sans effet indésirable dangereux pour les animaux.
Selon Pierre Cordelier, chercheur en cancérologie, un essai clinique chez l'homme devrait pouvoir être lancé pour tester ses travaux. © Universcience, Science Animation Midi-Pyrénées, Ombelliscience Picardie, Lacq Odyssée, CCSTI des pays de l'Adour, CCSTI La Turbine. Série Qui cherche cherche
« Cette approche oncolytique est étudiée depuis longtemps pour une raison simple : alors qu'une cellule saine lutte efficacement contre la réplication d'un virus, une cellule cancéreuse est beaucoup plus vulnérable. Le processus de cancérisation fait sauter des verrousverrous protecteurs, facilitant l'entrée et la réplication des virus dans ces cellules malades », explique Pierre Cordelier, responsable de l'étude et directeur de recherche au Centre de recherche en cancérologiecancérologie de l'Oncopôle de Toulouse. « Mais il faut utiliser un virus qui reconnaisse très spécifiquement les cellules concernées et très efficace d'emblée, car le traitement repose sur une injection intratumorale unique. Nous supposons en effet qu'une seconde injection déclencherait une réaction immunitaire rapide, qui entraînerait la neutralisation du virus », explique-t-il.
Avec ces travaux, les chercheurs ont apporté la preuve du concept de l'efficacité de ce virus modifié. « Il s'agit d'une nouvelle ère thérapeutique contre le cancer du pancréascancer du pancréas, estime Pierre Cordelier. Plus rien ne s'oppose au lancement d'un essai cliniqueessai clinique chez l'homme, si ce n'est l'organisation, la réglementation et le coût », explique-t-il. « Mais, compte tenu de la pauvreté de l'arsenal thérapeutique contre ces tumeurs et de notre expérience dans ce domaine, il y a de bonnes chances pour que cela ait lieu ! Au cours de cet essai il faudra par ailleurs rechercher des marqueurs prédictifs de réponse au traitement, afin de pouvoir, à terme, administrer le virus aux patients qui en bénéficieront le plus », conclut le chercheur.