au sommaire
Pourquoi le ciment colle-t-il aussi bien une fois sec ? Contrairement à ce que l'on pourrait croire et bien que l'on utilise ce matériau depuis des siècles (et les Romains savaient déjà en réaliser), on ne sait pas très bien pourquoi il est si solide. Mais des chercheurs du Massachusetts Institute of Technology disent avoir percé un de ses mystères, ce qui permettrait d'espérer un procédé de fabrication moins consommateur de dioxyde de carbonedioxyde de carbone (CO2). Ceux qui savent tout de la fabrication du ciment peuvent sauter les deux paragraphes suivants...
Très schématiquement, le ciment est obtenu par cuisson d'un mélange de calcairecalcaire et d'argileargile, à une température de 1 450 °C. Dans cette pâte presque liquide se déroulent un grand nombre de réactions chimiques, que les cimentiers sont loin de connaître toutes. Le résultat est une sorte de roche que l'on appelle le clinkerclinker, lequel est broyé et additionné de gypsegypse et, éventuellement, de quelques autres ingrédients. C'est le ciment, que l'on mélange ensuite à du sablesable, des graviers et de l'eau pour fabriquer du bétonbéton.
L'eau ajoutée au ciment dissout en partie le composé principal, le silicatesilicate tricalcique, ce qui libère des ionsions (silicates, hydroxyles et calciumcalcium). Ces trois composants réagissent pour former du silicate de calcium hydraté, que l'on appelle le CSH, selon la terminologie anglaise (calcium silicate hydrate). Les propriétés du ciment sec doivent beaucoup à ce CSH, qui colle, littéralement, les grains de sable et le gravier du béton.
Nanoparticules empilées comme des oranges
L'équipe du MIT, en collaboration avec le cimentier Lafarge, a travaillé sur les propriétés mécaniques du CSH à l'échelle microscopique, avec un appareillage sophistiqué, dont il n'existe que quatre ou cinq exemplaires au monde. Première découverte : le CSH se présente sous deux formes, de compositions identiques mais structurellement différentes. Georgios Constantinidesa et Franz-Josef Ulm, les deux auteurs, parlent de deux phases, l'une à haute densité, l'autre à faible densité. Ces deux densités correspondent exactement aux valeurs maximales théoriques connues des mathématiciensmathématiciens pour le rangement d'objets sphériques selon les deux méthodes possibles : en les jetant en vrac dans une boîte et les empilant soigneusement en pyramide comme des oranges sur un bel étalage.

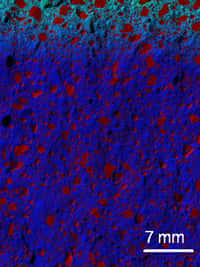
Au microscope électronique, le ciment (après gâchage à l'eau et sec) dévoile sa structure granulaire. Les particules sont de tailles variables (l'image montre un carré de 150 x 150 μm). Les auteurs de l'étude ont montré qu'on peut caractériser la structure du ciment en étudiant des surfaces de 100 x 100 μm. Crédit : K. Scrivener.
Malgré leurs structures différentes, ces deux phases montrent le même comportement mécanique, qui n'est pas celui que l'on attendait. Les propriétés du CSH viendrait des forces naissant au contact des minuscules particules (d'environ 5 nanomètresnanomètres) qui le composent et non pas du minéralminéral lui-même. Selon eux, ces propriétés mécaniques auraient leur origine dans les réactions d'hydratationhydratation, qui surviennent à l'ajout de l'eau de gâchage. Elles conduisent à une précipitation du CSH sous forme de nanoparticulesnanoparticules qui viennent au contact les unes des autres.
Voilà de quoi donner du grain à moudre pour de futures recherches sur la compréhension des propriétés mécaniques du ciment et sur l'amélioration des performances (temps de séchage, résistancerésistance, élasticitéélasticité...) que les cimentiers n'ont jamais cessé de rechercher.
Oublier le calcaire ?
Mais, expliquent les auteurs, il pourrait exister un autre avantage, concernant l'environnement cette fois. Jusque-là, personne ne s'est vraiment préoccupé de la participation de la fabrication du ciment à l'effet de serreeffet de serre. Elle est pourtant significative. Chaque année, l'humanité produit 2,3 milliards de tonnes de ciment, soit un mètre cube de béton par personne... Optimistes, les chercheurs expliquent que si l'on comprend bien le mécanisme d'adhérence des nanoparticules, il deviendra possible de trouver ou de fabriquer un matériau différent du silicate tricalcique et dont la fabrication nécessitera des températures inférieures à 1 500 °C. L'émissionémission de CO2 lors de la combustioncombustion dans les fours à ciment en sera réduite, « de 10 % à l'échelle mondiale », affirment-ils.
Franz-Josef Ulm explique qu'il planche actuellement sur le remplacement du calcium par le magnésiummagnésium et pense que ces recherches aboutiront à une nouvelle génération de ciment dans cinq ans...