Souvent considérée comme de l’eau salée, l’eau de mer présente une composition chimique bien plus complexe. Ainsi, on y retrouve quasiment tous les éléments du tableau de Mendeleïev. Siège de nombreux équilibres et réactions chimiques, cette composition résulte d’étroites interactions avec l’atmosphère, la biosphère et la croûte terrestre.
au sommaire
L'un des effets du réchauffement climatique actuel est la modification de la chimiechimie des océans et notamment leur acidification, mais pas uniquement. Les interactions océan-atmosphère-continents sont en effet complexes et la dynamique de ces échanges a largement influencé les climats du passé et impacté l'ensemble de la vie terrestre au cours du temps. L'état chimique de l’océan joue d'ailleurs un rôle déterminant dans sa capacité d'absorptionabsorption du CO2 atmosphérique et donc dans sa capacité à jouer un rôle de régulateur du climat. Pour étudier l'évolution du climat, il est donc important de comprendre les équilibres et les réactions chimiquesréactions chimiques qui se jouent au sein des océans du globe.
Bien plus que de l’eau salée
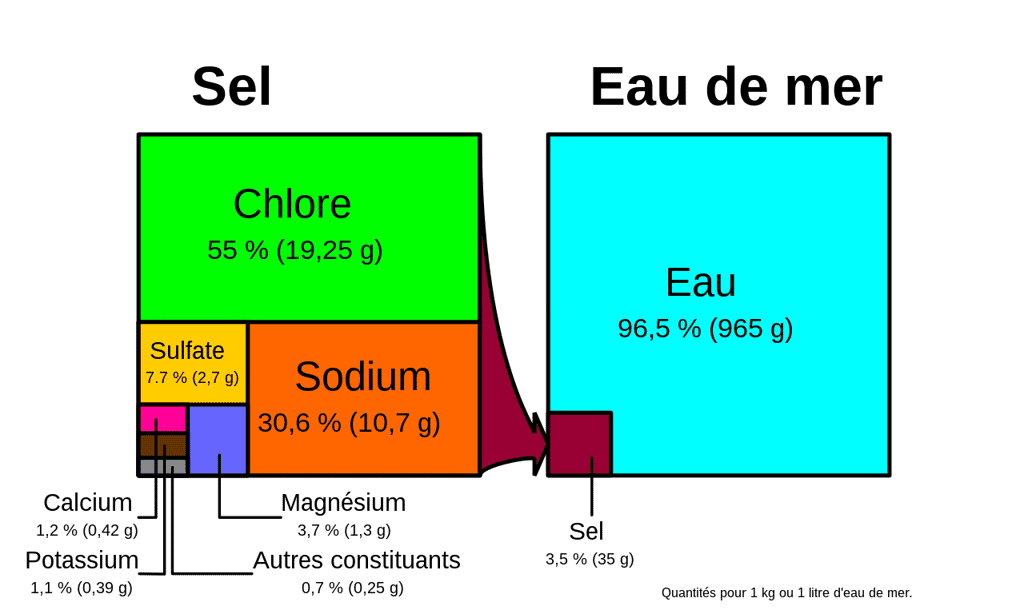
Il faut en effet savoir que l'eau de mer, ce n'est pas uniquement de l’eau salée. Certes, cette solution se compose à 96,5 % d'eau pure et 3,5 % de sels et gazgaz dissous. Mais parmi ces derniers, on retrouve un très grand nombre d'éléments chimiqueséléments chimiques. Quatre-vingt-douze éléments sont en effet présents, bien qu'en quantité très variable et souvent uniquement à l'état de traces. ChloreChlore (Cl) et sodiumsodium (Na) sont naturellement les plus abondants car ils entrent dans la composition du sel de mer (chlorure de sodium). Il en résulte que la salinitésalinité de l'eau de mer est relativement élevée, d'environ 35 grammes par litre, mais cette valeur peut varier de manière significative en fonction des endroits du globe.
De manière générale, la composition de l'eau de mer est variable d'une région à une autre mais également au cours du temps. Car il s'agit d'un système ouvert, soumis à des flux entrants qui apportent certains éléments (rivières, eau de pluie, dépôts volcaniques, sources hydrothermales), et à des flux sortants, souvent représentés par le terme de « puits » (minéralisation, diagenèse des sédimentssédiments, évaporation, processus biologiques). Chaque élément va donc avoir un temps de résidence dans l'océan qui lui est propre. De manière générale, les ionsions majeurs qui ne réagissent pas chimiquement ont des temps de résidence de l'ordre du million d'années. Les ions mineurs (souvent présents à l'état de trace), sont quant à eux bien plus réactifsréactifs et vont voir leur distribution modifiée par les diverses réactions chimiques dans lesquels ils seront impliqués, comme les réactions d'oxydo-réduction par exemple, mais également par l'activité biologique. Leurs temps de résidence sont ainsi plutôt de l'ordre de quelques dizaines à milliers d'années. Ce sont ces éléments très réactifs qui vont permettre de suivre l'évolution de la composition chimique de l'océan au cours du temps.
11 sels minéraux qui définissent la composition chimique de l’eau de mer
À l'échelle humaine, les principaux constituants de l'eau de mer sont cependant présents en quantité à peu près constante. On dénombre 11 éléments majeurs en solution (sels minérauxminéraux dissous) dans de l'eau pure (classés par ordre d'importance) :
- le chlorure (Cl-) ;
- l'ion sodium (Na+) ;
- le sulfate (SO42-) ;
- l'ion magnésiummagnésium (Mg2+) ;
- l'ion calciumcalcium (Ca2+) ;
- l'ion potassiumpotassium (K+) ;
- le bicarbonatebicarbonate (HCO3-) ;
- le bromure (Br-) ;
- l'acideacide borique (B(OH)3) ;
- le carbonate (CO32-) ;
- le fluorure (F-).
Mais on trouve également sous forme de traces des ions strontiumstrontium, lithiumlithium, rubidiumrubidium, baryumbaryum, de l'uraniumuranium, du vanadiumvanadium, des ions fersfers, du titanetitane, des ions aluminiumaluminium...

Des gaz dissous qui ont joué des rôles majeurs pour la vie océanique
À ces composants il faut ajouter les principaux gaz dissous :
- azoteazote (64 %) ;
- oxygène (34 %) ;
- dioxyde de carbonedioxyde de carbone (CO2) (1,8 %).
Cependant, la solubilité des gaz dépend fortement de la température de l'eau (elle augmente avec la température). Elle décroît cependant avec la salinité. Le comportement du gaz carbonique est quant à lui plus complexe, car il réagit avec l’eau pour former de l’acide carbonique qui va lui-même réagir avec les ions bicarbonate et carbonate présents dans l'eau. De plus, la teneur en CO2, mais également celle en O2, va dépendre des échanges avec l'atmosphère ainsi que des processus métaboliques des organismes biologiques présents (ou non) dans l'océan.
On observe ainsi une différence de concentration en oxygène entre les eaux de surface (sursaturées du fait des échanges avec l'atmosphère et de la photosynthèsephotosynthèse) et les eaux profondes. Celles-ci sont sous-saturées à cause de la consommation d'O2 par la respiration des organismes mais surtout par le processus de décomposition de la matièrematière organique (oxydationoxydation). Il existe ainsi une zone dite à oxygène minimum (ZOM), qui correspond à une tranche d'eau très pauvre en oxygène. Elle est habituellement située entre 500 et 1 200 mètres de profondeur. On observe cependant de très fortes variations de la profondeur de cette zone au cours des temps géologiques. Durant des événements particuliers appelés événements anoxiquesanoxiques, cette zone d'oxygène minimum s'est étendue vers le haut, signe d'un appauvrissement très poussé en oxygène dans les océans. Ces événements sont souvent associés à des crises biologiquescrises biologiques et des extinctions de masse dans le milieu océanique.