au sommaire
" Laissez-vous emporter par la fascinante et improbable histoire de la rencontre de l'homme et de l'argileargile il y a 12 000 ans. " Elle modela notre vie et nos civilisations, des hommes du néolithique, des civilisations Sumérienne, Précolombienne, en passant par le Moyen Age occidental, profita de l'ère industrielle pour aujourd'hui occuper une place prépondérante dans notre quotidien, jusqu'à nous guider vers les étoiles. De la Terre aux étoiles ou la fabuleuse histoire de l'aventure de la Terre. »

Poteries en terre cuite. © SandeepHanda, Pixabay, DP
Telle est l'introduction du site de l'Ecomusée de la Tuilerie de Pouligny, un site à visiter qui vous racontera l'argile et le feu.
A - L’argile
C'est une roche formée de phyllosilicatesphyllosilicates d'aluminium, plus ou moins hydratés. Elle représente 50% des sédimentssédiments (et jusqu'à 70 % des sédiments continentaux) et les constituants principaux des sols, particules finesparticules fines, de l'ordre du µm.

Carrière d' argile
Leurs principaux composants :
- phyllosilicates dominants
- quartzquartz jusquà 30%
- calcédoine d'origine organique
- oxydes et hydroxydes et sulfures de fer si le milieu est réducteur
- oxyde d'aluminiumoxyde d'aluminium sous climatclimat chaud et humide
- carbonates
- matièrematière organique:
- éléments figuréséléments figurés: pollenspollens, spores, débris ligneux
- matière amorpheamorphe (décomposition par bactériesbactéries)
Les argiles ont des propriétés remarquables pour des roches :
- absorptionabsorption d'eau
- plasticitéplasticité
- rôle de « couche savon » pour glissements de matériaux (glissement de terrain)
- compaction importante par expulsion d'eau. Les pores diminuent alors et la roche devient imperméable
- pouvoir adsorbant
- dispersion dans l'eau, les particules restent en suspension longtemps et décantent avec une -vitessevitesse de chute très faible (Loi de Stockes).
Leurs utilisations sont nombreuses et importantes dans :
- les cimentsciments
- les céramiquescéramiques

Effet de matière
- en pharmacie et cosmétique
- comme pigmentspigments: ocresocres (argiles + oxydes de fer)
B - Les minéraux argileux
Ce sont des phyllosilicates d'aluminium dont les feuillets sont constitués :
- de couches d'octaédres Al(OH)6 et
- de couches de tétraédres SiO4
reliées par les atomesatomes O et OH mis en commun.
D’après la structure du feuillet, on distingue :
- les argiles 1/1 : 1 couche tétraédrique et 1 couche octaédrique et
- les argiles 2/1 : 2 couches tétraédriques pour 1 couche octaédrique.
- la kaolinite 1/1 : elle se forme dans les sols drainés, acidesacides, en climat subtropical et tropical. Ses cristaux sont grands.
- les illites 2/1 : le minéralminéral est ubiquiste et sa structure est proche de la muscovitemuscovite (plus d'eau, moins de K+).
- la glauconie (illite) : minéral vert ferrifère exclusivement formé en milieu marin peu profond.
- les smectites 2/1 : l 'empilement est désordonné ; les substitution d'atomes sont fréquentes. La faible charge des feuillets facilite l'adsorptionadsorption de moléculesmolécules variées (eau, cationscations, etc). Les smectites, ou montmorillonites, sont calciques, rarement sodiques. Elles sont formées dans les sols mal drainés plutôt alcalins.
les chlorites 2/1 : l'espace entre feuillets contient des ionsions de Mg et OH. L'Al est remplacé localement par le Fe.
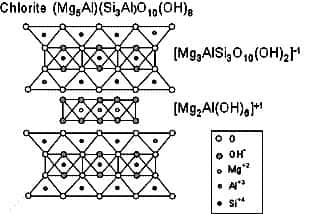
Chlorite structure
- existent en grands cristaux dans les roches magmatiquesroches magmatiques
- sont formées pendant la diagenèsediagenèse des roches sédimentairesroches sédimentaires
- se trouvent parmi les éléments détritiques dans les sols sous climat peu agressif.
- la vermiculite 2/1 : sols de la zone tempérée. La couche octaédrique contient du Fe et du Mg. Proche des illites et des chlorites, elle montre des propriétés « gonflantes »
- les argiles fibreusesfibreuses : feuillets discontinus, ex : sépiolite, attapulgite, paligorskite. On les trouve dans les milieux confinés.
Ils se forment lors de la destruction des roches, peuvent rester sur place ou être transportés.
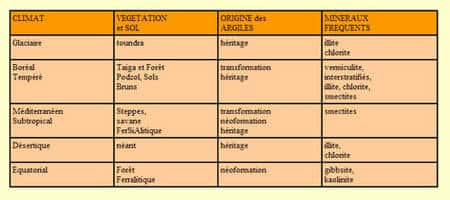
Les origines des minérauxminéraux argileux
Selon les roches et les climats et les situations, les minéraux argileux sont différents. Par exemple :
L'altération d'une roche acideroche acide, granitegranite, donnera de la kaolinite.
L'altération d'une roche basiqueroche basique, basaltebasalte, donne des smectites.
Une pente, drainagedrainage et lessivage bons, la kaolinite et favorisée.
Dans un milieu confiné, solutions concentrées, on aura plutôt des smectites.
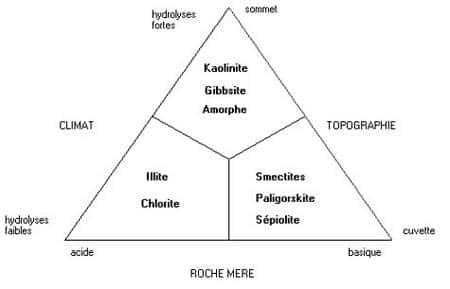
Phyllosilicates et altérations
Certains minéraux argileux se forment en dehors des sols à partir des ions en solution, par exemple la glauconie dans les vases littorales. On distingue des transformations par soustraction d'ions ou, au contraire, par fixation d'ions supplémentaires. Ces transformations ont lieu aussi bien au cours de l'altération que de la diagenèse.

Cliquez pour agrandir le texte ci-dessus
Surface spécifique de quelques minéraux argileux
Les argiles, avec l'eau, augmentent de volumevolume : l'ensemble eau-argile devient plastiqueplastique, puis visqueux et finalement les particules se dispersent en formant une solution colloïdale. L'argile imprégnée d'eau qui se dessèche se rétracte et se casse. Les argiles confèrent au sol sa structure et ses propriétés mécaniques. Elles sont associées aux autres composants et constituent les complexes argilo-humiques.
C - Le retrait, les retraits
A cause de la préparation de l'argile par adjonction d'eau, il y a un retrait au séchage, puis à la cuisson. Une argile préparée pour la sculpture ou la poterie contient environ un tiers d'eau "libre" en termes de poids (non associée à l'argile à l'échelle moléculaire). Cette première perte de massemasse de l'ordre de 3 à 8%.
Les argiles les plus fines et les plus "pures", se rapprochant de la kaolinite, donc de la terre à porcelaine, perdant toujours plus d'eau.
Les autres, "argiles ouvertes", contiennent des corps imperméables (quartz, sablesable, feldspath, etc.) ouvrant des "canaux" permettant une bonne évacuation de l'eau. Après cuisson, les terres "ouvertes" s'avèrent souvent plus résistantes aux chocs thermiques.
L'eau libre demeure donc présente en quantité importante dans l'argile (eau dite "hygrométrique"). Le séchage doit être lent, en atmosphèreatmosphère modérément humide, et homogène. Le reste est éliminé au début de la cuisson.
Les terres chamottées ne posent pas ces problèmes. La diminution de la plasticité par l'adjonction d'éléments imperméables est dans ce cas plutôt souhaitable. L'excellent comportement de ces terres au séchage et à la cuisson autorise la création de pièces plus grandes.
D - La cuisson
La perte d'eau "hygrométrique" est considérable, s'effectue par évaporation et non par capillaritécapillarité, et pose des problèmes différents. La quantité d'eau restante, après le séchage, est en effet de l'ordre de 20 à 30% de la masse des pièces
Les accidentsaccidents courants sont liés à l'accumulation interne de vapeur dans les premiers temps de la cuisson. Les risques d'éclatement sont importants.
A 100°C, une progression très lente doit être respectée pour laisser à la vapeur le temps de s'échapper. De 350 à 500°C, l'eau des associations moléculaires s'évapore. Cette masse de 14% doit être, elle aussi, libérée très progressivement à cause d'un risque d'éclatement.
A partir de 500°C, l'aération du four devient essentielle pour oxyder l'argile et supporter ces températures.
A 573°C, c'est le changement d'état du quartz (Lire à ce sujet le dossier "Au coeur de la silice"..... )
Avant 900°C, se produit l'élimination du carbonecarbone, du soufresoufre, du calciumcalcium etc.. Là aussi, la lenteur permet de diminuer le risque. La présence d'airair et son renouvellement constituent des facteurs déterminants.
Le but de cette cuisson est l'élimination des éléments produisant des effets chromatiques indésirables: il s'agit simplement d'une transformation de la matière.

ConstructionConstruction d'un four primitif
Au delà de 900°C, c'est la vitrificationvitrification qui occasionne un nouveau retrait.
Cette étape correspond au passage à l'état pâteux, puis à l'état vitreux au refroidissement. Des cristaux de mullite se forment, tissant un réseau solidifiant à l'intérieur de la masse vitreuse. Il ne faut pas monter trop haut en température sinon la terre « fond » mais il faut monter assez pour qu'elle vitrifie et soit étanche ! Cette étape pose un gros problème : la déformation.
Les terres rouges contiennent une importante quantité d'oxydes de fer. Ces composés favorisent la vitrification en se liquéfiant avant les autres. Aussi ce type de terre a-t-il une température de fusionfusion de 1250°C (± 30°C environ) alors qu'une terre blanche pure se liquéfie aux alentours de 1800°C.
Le passage à l'état liquideétat liquide, puis à un état solideétat solide vitreux, modifie le volume, tandis que la masse diminue. Le retrait peut être important.

















