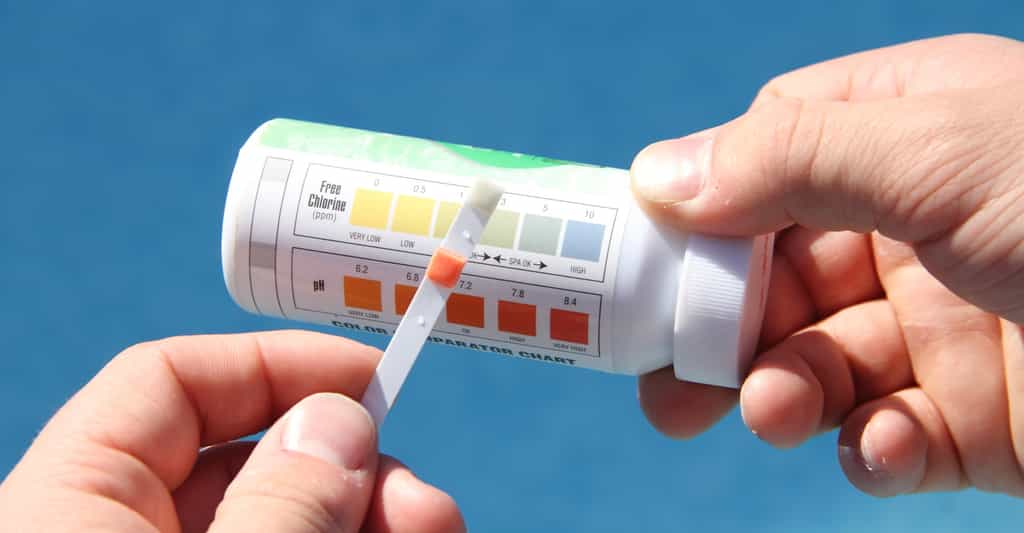
L'adjectif alcalin peut être associé à différents termes. Il qualifie par exemple des roches riches en ions Na et/ou K, qui se trouvent en particulier dans les feldspaths alcalins et dans certains micas. On parle également d'une eau -- ou plus généralement d'une solution -- alcalinealcaline lorsque son pH affiche une valeur supérieure à 7. Ainsi en médecine, une substance qui a pour effet d'augmenter le pH du sang est appelée substance alcaline. On appelle piles alcalines celles dont l'électrolyte, l'hydroxyde de potassiumpotassium (KOH), est alcalin.
Historiquement, le terme alcalin était employé pour qualifier les composés qui présentaient les propriétés -- et notamment celle de ramollir les matièresmatières organiques -- de ceux que l'on appelait les alcalis en d'autres mots, des bases, des sels ou des solutions basiques concentrées. Aujourd'hui, les alcalis constituent une sous-classe des bases et le terme est plus volontiers employé pour désigner une solution basique concentrée.

Le point de vue des chimistes
Dans le tableau de Mendeleïev, la première colonne -- hors hydrogènehydrogène (H) -- regroupe ceux que l'on nomme les métauxmétaux alcalins. LithiumLithium (Li), sodiumsodium (Na), potassium (K), rubidiumrubidium (Rb), césiumcésium (Cs) et franciumfrancium (Fr) sont des métaux malléables et très réactifsréactifs. Ils sont caractérisés par leur couche externe qui comporte un seul électronélectron. Pour se rapprocher de la configuration électroniqueconfiguration électronique du gazgaz rare le plus proche, ils ont tendance à former des cationscations, Li+ ou Na+. Au contact de l'airair, ils forment rapidement des oxydes -- ou du nitrurenitrure dans le cas du lithium -- et au contact de l'eau, ils forment des hydroxydes qui sont des bases très fortes.
Notez par ailleurs que l'expression terre alcaline désignait par le passé, pour les chimistes, un oxyde de métal alcalino-terreux. Car les métaux de ce type, que l'on retrouve dans la deuxième colonne du tableau périodique des élémentstableau périodique des éléments, présentent une tendance alcaline lorsqu'ils sont oxydés. L'oxyde de calciumcalcium (CaO) en constitue un exemple bien connu. Il est le principal composant de la chaux vivechaux vive. Cette dernière est utilisée aussi bien pour équilibrer le pH des sols que dans l'industrie. Dans la sidérurgie tout particulièrement, elle apparaît comme agent purificateurpurificateur et fait aussi fonction de fondant. Ainsi pour produire une tonne de fer, on emploie quelque 50 kilogrammeskilogrammes d'oxyde de calcium.