au sommaire

Généralités sur l’uranium, carburant des centrales nucléaires
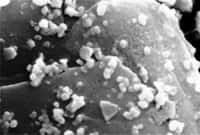
L'uranium est un élément naturel, blanc argenté, brillant, dense et faiblement radioactif. Il est omniprésent dans la nature et on le trouve en quantités variables mais faibles dans les roches, le sol, l'eau, l'air, les plantes, les animaux et les êtres humains.
L'uranium (U) est l'élément le plus lourd qu'on trouve dans la nature, jamais à l'état métallique, toujours combiné à l'oxygène, sous forme d'oxydes ou de silicatessilicates. Il est moins abondant que le cuivre, le nickel ou le zinczinc, mais il est 500 fois plus abondant que l'or, plus abondant aussi que l'argentargent, le cadmiumcadmium ou le mercuremercure. L'uranium naturel se compose de trois isotopesisotopes radioactifs :
- 238U (99,27 % de la massemasse totale) ;
- 235U (0,72 %) ;
- 234U (0,0054 %).

Un échantillon de roche contenant de l’uranium. © DR
Cet élément a été découvert en 1789 par le chimiste allemand Martin Klaproth. Il doit son nom à la planète UranusUranus. Pendant plus d'un siècle, l'uranium ne fut qu'une curiosité. On s'en servait pour fabriquer un verre de couleurcouleur verte, mais ses applicationsapplications restaient peu nombreuses : un résidu des mines de pechblende telle celle de Gilbert Labine au Grand lac de l'Ours, Canada, dans les années 1930. La pechblende était exploitée parce qu'elle contenait du radiumradium, élément qui intéressait les chercheurs intrigués par la radioactivitéradioactivité.
Qu'est-ce que la demi-vie d'un élément radioactif ?
La demi-viedemi-vie d'un élément radioactif est le temps pour que la moitié de ses noyaux se désintègrent. Par exemple, la demi-vie du radium 226 est de 1.600 ans : en 1.600 ans, un gramme de radium 226 va se transformer en un demi-gramme de radium 226 et en un demi-gramme de quelque chose d'autre. Une quantité de n'importe quel élément radioactif diminue d'un facteur 1.000 en l'espace de dix demi-vies. Par conséquent, en 16.000 ans, un gramme de radium 226 se décomposera en un milligramme de radium 226 et en 999 milligrammes d'autres produits.
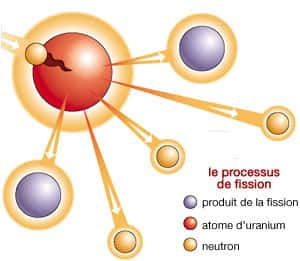
La fission d’un atome d’uranium donne naissance à des produits de fissions et à des neutrons libres. © DR
Il y a en moyenne dans l'organisme humain approximativement 90 µg d'uranium qui proviennent de l'air, de l'eau et des aliments absorbés :
- 66 % se trouvent dans le squelette ;
- 16 % dans le foiefoie ;
- 8 % dans les reinsreins ;
- 10 % dans les autres tissus.
L'uranium est utilisé principalement dans les centrales nucléairescentrales nucléaires. Néanmoins, la plupart des réacteurs fonctionnent à l'uranium enrichi en 235U (1,5 à 3 % environ au lieu de 0,72 % normalement).
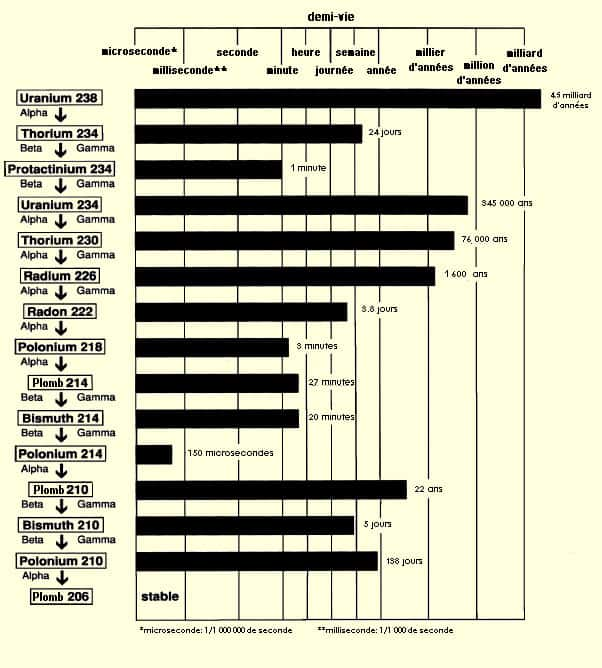
Chaîne de désintégration de l’uranium. © DR
Quelques informations sur l’uranium
- Numéro atomiqueNuméro atomique : 92
- Masse atomique : 238,03 u
- Électronégativité de Pauling : 1,38
- Masse volumiqueMasse volumique : 19,1 g/cm3
- Température de fusionfusion : 1.132 °C
- Température d'ébullition : 3.818 °C
- Rayon atomique (Van der Waals) : 0,121 nm
- Rayon ionique : 0,103 nm (+3) ; 0,093 nm (+4)
- Isotopes les plus stables : trois
- Configuration électroniqueConfiguration électronique : [Rn] 5f3 6d1 7s2
- Isolé pour la première fois par Péligot en 1841
Effets de l'uranium sur la santé
On est sans cesse exposé à une certaine quantité d'uranium à travers la nourriture, l'air, le sol et l'eau, étant donné qu'il y est naturellement présent. Les concentrations d'uranium dans les aliments de la mer sont en général tellement faibles que l'on peut les ignorer sans risque. Ses effets sur la santé ont été étudiés. Les scientifiques n'ont pas détecté d'effet nocif des radiations en présence d'un niveau naturel d'uranium. Quand on est exposé pendant une longue période à des radionucléidesradionucléides d'uranium, on risque de développer des problèmes rénaux ou un cancercancer. Les risques sont plus élevés lorsqu'on est exposé à de l'uranium enrichi. Cette forme d'uranium dégage des radiations nocives. L'uranium enrichi peut se retrouver dans l'environnement lors des accidentsaccidents dans les centrales nucléaires (Tchernobyl). On ne sait pas encore si l'uranium a des effets sur la reproduction.
Effet de l'uranium sur l'environnement
L'uranium est un métalmétal radioactif très réactifréactif, on ne peut le trouver sous sa forme d'élément. Les composés sont plus ou moins solubles et leur solubilité dans l'eau détermine leur mobilité dans l'environnement :
- dans l'air, les concentrations sont faibles, principalement des poussières qui retombent dans les eaux ou sur le sol ;
- dans l'eau, l'uranium est dissout et provient des roches et des sols que l'eau recouvre. Une partie est en suspension. La quantité d'uranium dans l'eau potable est très faible. L'uranium n'a pas tendance à s'accumuler dans les poissonspoissons ou les légumes, et l'uranium absorbé est éliminé dans les urines et les fècesfèces ;
- dans le sol, on trouve des concentrations diverses, très faibles. L'Homme en augmente les quantités du fait de ses activités industrielles. L'uranium se combine avec d'autres composés, et peut rester des années sans rejoindre les eaux souterraines. Les concentrations en uranium sont souvent plus élevées dans les sols riches en phosphatephosphate.
Les plantes stockent l'uranium dans leurs racines. Les légumes racines, tels que les radisradis, peuvent donc contenir des concentrations plus élevées.
Pénurie et fin progressive de l'uranium
Les chiffres qui suivent proviennent d'Uranium Resources and Nuclear Energy de l'Energy Watch Group, et datent de décembre 2006 :
- une pénurie d'uranium se produirait dès 2015 ;
- la production atteindrait son maximum en 2025 ;
- aucune autre technologie nucléaire ne sera disponible avant 2040 ;
- le prix de l'uranium a été multiplié par dix en quatre ans ;
- le coût du combustiblecombustible prend une importance croissante dans le coût de l'électricité nucléaire ;
- l'uranium est une ressource limitée.
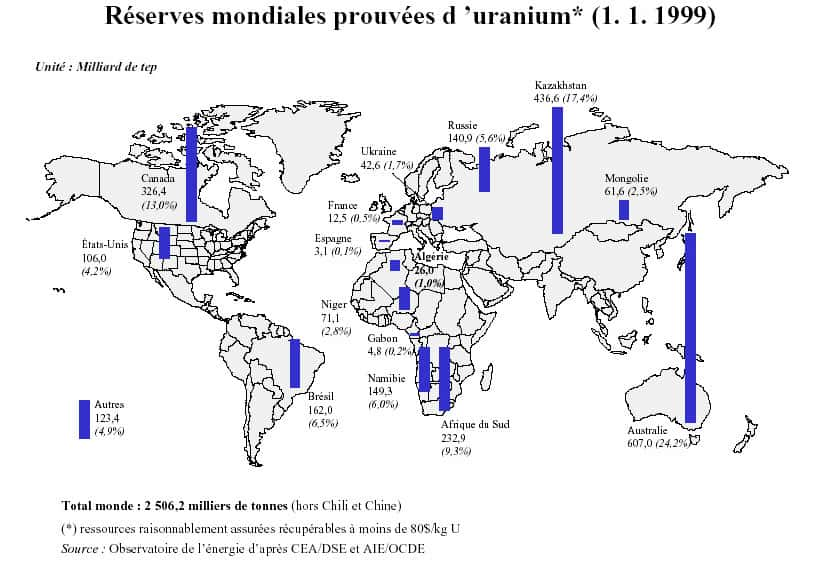
Les réserves mondiales d’uranium, estimées en 1999. © DR
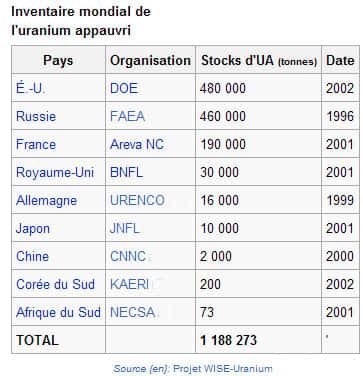
Des réserves d'uranium limitées et aléatoires
L'Agence pour l'énergieénergie nucléaire (AEN) a publié un état des réserves (des ressources certaines) et ressources (supposées) d'uranium selon différents niveaux de coût et de certitude en 2006 :
- ressources raisonnablement assurées (réserves) : 3.297 kt ;
- ressources supposées : 4.743 kt ;
- ressources pronostiquées (probabilité faible) : 7.262 kt.
La France possède bien des réserves d'uranium, mais les mines sont fermées. Entre 1956 et 2002, 75.000 tonnes d'uranium ont été produites en France, avec un maximum de 3.400 tonnes en 1989. En 1985, les réserves étaient de 112.000 tonnes.
Une pénurie d'uranium en 2015 ?
La consommation mondiale d'uranium est de 67.000 tonnes par an, tandis que la production est de 42.000 tonnes. La différence provient des stocks civils et militaires, qui seraient épuisés en 2015. Depuis 1989, la consommation est supérieure à la production, qui a commencé à raugmenter vers 2000, mais pas assez pour atteindre le niveau de la consommation.
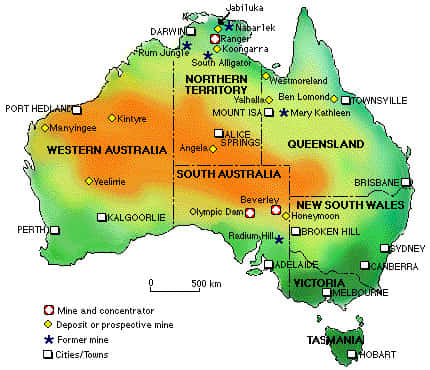
Des gisementsgisements importants sont connus, mais la mise en exploitation prend du retard. Cigar Lake, au Canada, devait produire sept millions de tonnes chaque année, mais n'a pu être mise en exploitation en 2007 à la suite d'inondationsinondations et de problèmes techniques. L'ouverture de l'exploitation est annoncée pour l'année 2014. La mine d'uranium Ranger, en Australie, a été inondée en mars 2007. Elle a produit environ 400 tonnes d'oxyde d'uranium par an depuis.
Souvent, la prospection ne donne guère de résultats, et la mise en exploitation prend souvent dix ans. La capacité sera insuffisante, sans compter la perte des mines devant fermer.
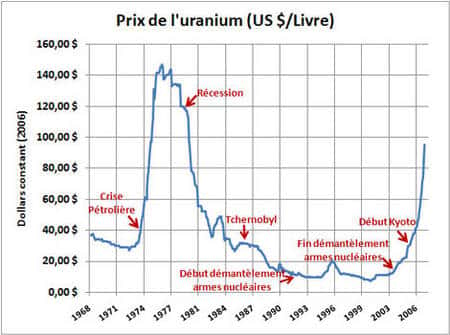
Évolution du prix de l’uranium de 1968 à 2006 en regard de différents événements, en dollars constants. © DR
L'augmentation rapide du prix, multiplié par dix en quatre ans, montre l'existence d'un problème de ressources minières. Entre 2003 et 2007, le prix du kilogrammekilogramme de yellowcake est passé de 22 à 249 dollars.
Pour aller plus loin, découvrez le fonctionnement schématique d’une centrale. Vous pourrez également découvrir de très nombreuses autres informations sur l'uranium les diverses rubriques de notre site.