au sommaire
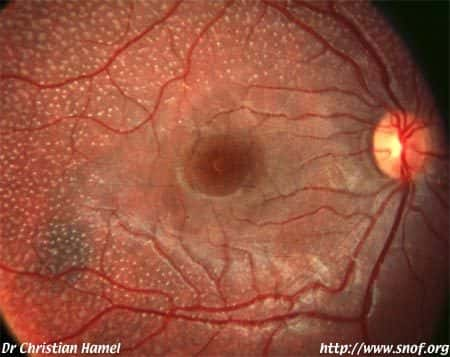
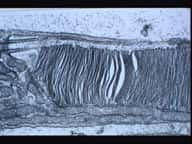
Dans neuf cas sur dix, la rétinopathie pigmentaire affecte les bâtonnets, photorécepteurs servant à la vision crépusculaire, première affectée par la maladie. Les cellules touchées, de plus en plus nombreuses, deviennent colorées et insensibles à la lumiè
Quasiment aveugle, Elisabeth Bryant, une américaine de 63 ans, a recouvré en partie la vue grâce à une première mondiale : la greffegreffe d'une couche de cellules rétiniennes prélevées sur un fœtusfœtus. L'équipe de Robert Aramant, de l'université de Louisville (Kentucky), a opéré il y a deux ans et demi cette femme qui souffrait de rétinopathie pigmentairepigmentaire. Cette maladie dégénérative de la rétinerétine, caractérisée par la disparition progressive des photorécepteurs (les cônescônes et les bâtonnetsbâtonnets, sensibles à la lumière), est héréditaire et réputée incurable, évoluant inexorablement vers la cécité. Aujourd'hui, Elisabeth Bryant peut lire et, nous précise l'article du New Scientist où a été publiée la nouvelle, "jouer à des jeux sur ordinateurordinateur et consulter son courrier électronique".
Le temps écoulé depuis l'intervention exclut que cette amélioration puisse être un effet transitoire. Depuis, six autres patients, atteints de la même maladie ou de dégénérescence maculairedégénérescence maculaire - une autre maladie dégénérative de la rétine - ont reçu eux aussi une greffe de cellules rétiniennes fœtales. Quatre d'entre eux bénéficient déjà d'une amélioration de leur vue.
Ce n'est pas la première tentative de transplantationtransplantation de cellules dans la rétine pour réduire les effets de ce genre de maladie dégénérative, principale cause de cécité dans les pays riches. Les autres équipes misent sur les cellules souchescellules souches, ces cellules indifférenciées, présentes en nombre chez l'embryonembryon, mais que l'on a découvert également chez les adultes. Les scientifiques parviennent désormais à diriger leur différenciation et cherchent à les utiliser dans les situations les plus variées pour leur faire reconstruire tel ou tel tissu lésé. Mais, pour l'instant, ces essais ont toujours échoué.
L'équipe de Robert Aramant explique son succès par le fait que le morceau de rétine transplanté était intact et comportait la partie supérieure du tissu rétinien, contenant les cellules sensibles à la lumière.
Mieux que le fœtus, le porc génétiquement modifié
Cette belle réussite suscite un grand espoir pour les millions de malades atteints par ces affections dégénératives. Mais il y a des limites. Tout d'abord, comme dans tous les essais de ce genre, il ne s'agit pas d'une greffe de la totalité de la rétine, mais seulement d'un petit morceau (2 millimètres carré). Le patient ne peut donc retrouver qu'une partie de ses capacités visuelles initiales. Ensuite, l'utilisation de cellules provenant de fœtus limite énormément la source de rétines transplantables par cette méthode et pose aussi un problème éthique.
Seul le Royaume-Uni s'est doté d'une loi autorisant l'utilisation de cellules fœtales tout en l'encadrant strictement. Aux Etats-Unis, où l'avortementavortement est toujours un sujet sensible, cette première médicale a suscité quelques réactions, exprimant la crainte que des femmes soient tentées par une grossessegrossesse et un avortement volontaires afin d'obtenir un fœtus utilisable pour guérir une cécité chez elles-mêmes ou chez un de leurs proches. "Des gens vont penser que nous favorisons l'avortement", explique Norman Radtke, le chirurgien qui effectué la transplantation.
Mais les recherches continuent. Robert Aramant, qui ne croit guère à la solution des cellules souches, imagine d'utiliser des rétines de porcs, génétiquement modifiés pour éviter les risques de rejet de la grefferejet de la greffe.