au sommaire
Le diagnostic de la grippe aviaire
L'OMS a déterminé les cas possibles de grippe aviaire afin de pouvoir poser un diagnostic plus rapidement.

Il existe un diagnostic clinique et un diagnostique biologique de la grippe aviaire. © DR
Le diagnostic clinique de la grippe aviaire
1. En dehors des zones d'épizooties à virus aviaires hautement pathogènes
Suite à l'épidémieépidémie de grippe aviairegrippe aviaire aux Pays-Bas en 2003, la Direction générale de la santé dépendant du ministère français de la Santé, avait émis une directive le 7 juillet 2003, réactualisée le 22 mars 2006, à l'intention des professionnels de santé. Cette note définit « le cas humain suspect de grippe à influenzainfluenza A hautement pathogènepathogène », notamment à A (H5N1H5N1). Les définitions de cas, possible, probable et confirmé de grippe aviaire ont été élaborées par l'OMSOMS et tiennent compte de l'évolution de la situation épidémiologique mondiale.
Cas possible (ou suspect) :
- toute personne présentant un syndromesyndrome respiratoire aigu fébrilefébrile, ayant eu dans les sept jours précédant les symptômessymptômes : une exposition professionnelle à des cas humains ou animaux, avérés ou présumés, de grippe aviaire, ou à tout lieu ou matériel biologique avéré ou présumé contaminé par le virus A (H5N1) ; ou un contact direct, prolongé, répété, ou à moins d'un mètre dans les pays avec épizootiesépizooties et cas humains de grippe Agrippe A (H5N1), avec des oiseaux vivants ou morts, sauvages ou domestiques, ou leurs fientesfientes ; ou un contact proche et répété avec une personne infectée par un virus influenzavirus influenza A (H5) ou fortement suspectée de l'être ;
- toute personne présentant un syndrome grippal avec détresse respiratoire aiguë : de retour d'un pays atteint par les épizooties de grippe aviaire A (H5N1), depuis moins de sept jours ; de retour d'un pays où le virus A (H5N1) a été détecté chez les oiseaux sauvages et qui a eu un contact direct avec des oiseaux sauvages malades ou morts.
L'analyse des cas possibles se fait en fonction des listes des pays atteints par la grippe humaine d'origine aviaire et par les épizooties de grippe A (H5N1) ; ces listes sont actualisées en permanence et sont disponibles respectivement sur le site de l'OMS (OMS 2006 3) et le site de l'OIEOIE.
2. En zone d'épizooties à virus grippal aviaire hautement pathogène
Dans les pays où une activité grippale aviaire est suspectée ou identifiée, le diagnosticdiagnostic de grippe humaine d'origine aviaire fait partie du diagnostic différentiel des pneumoniespneumonies aiguës sévères. Le contexte d'épidémie de grippe saisonnière en rapport avec des virus influenza A/H1, A/H3 ou B, ou de tout syndrome grippal en relation avec d'autres pathogènes des voies respiratoires rend le diagnostic clinique difficile.
L'OMS a édité un guide de prise en charge des personnes susceptibles d'être infectées par le virus influenza A (H5N1) (OMS 2004 1).
Cas possible :
- pendant les sept jours précédant les symptômes, toute personne ayant été en contact avec : des oiseaux sauvages ou de la volaille domestique, vivants ou morts, à une distance de moins de un mètre ; des élevages de volaille domestique ayant fait l'objet d'un confinement dans les six semaines précédentes ; toute personne faisant l'objet d'une suspicion ou d'un diagnostic de grippe A (H5N1) ; toute personne décédée à la suite d'une pneumopathiepneumopathie aiguë inexpliquée ;
- toute personne exposée professionnellement à des isolats cliniques humains ou animaux de virus influenza hautement pathogènes, pendant les sept jours précédant le début de la symptomatologie.

Grippe aviaire : les symptômes doivent être pris au sérieux pour poser rapidement un diagnostic. ©1999- 2006 Body1, reproduction et utilisation interdites
Tout cas possible doit faire l'objet d'investigations virologiques. Le diagnostic clinique est subordonné au diagnostic biologique.
Diagnostic biologique (de Jong and Hien 2006, 29)
1. Le diagnostic direct
Il est virologique (Beby-Defaux, Giraudeau et al. 2003 10) (Playford and Dwyer 2002 77) (OMS 2005 2). Il repose sur la mise en évidence du virus grippal, ou de ses antigènesantigènes, sur différents prélèvements : écouvillonnage nasopharyngé, aspiration nasale, expectorationexpectoration, liquide de lavage nasal. Les prélèvements doivent être effectués dès le début des symptômes, avant quatre à cinq jours chez l'adulte, l'excrétion virale diminuant rapidement. Par contre, chez le jeune enfant, l'excrétion virale se fait sur une plus longue période et les prélèvements sont justifiés et utiles au-delà de cinq jours. Des échantillons respiratoires multiples sur plusieurs jours sont hautement recommandés.
- Détection rapide de l'antigène viral : les résultats sont obtenus en 15 à 30 minutes (Beigel, Farrar et al. 2005 11). L'immunofluorescence est une méthode largement utilisée et d'une bonne sensibilité ; elle permet de diagnostiquer soit la grippe A ou la grippe B, soit la grippe A/B parmi cinq autres virus respiratoires. L'identification du sous-type par les kits commerciaux a montré ses limites, les anticorps monoclonauxanticorps monoclonaux dirigés contre l'influenza A/H1 donnent une réaction croisée avec le sous-type H5. Les résultats doivent donc être confirmés par le kit OMS qui contient un pool d'anticorps monoclonaux spécifiques du type A/H5, un pool dirigé contre le type A et B et un pool spécifique de A/H1 et A/H3. Les méthodes immunoenzymatiques (comme l'ELISA) permettent la mise en évidence du virus influenza A uniquement (par la nucléoprotéine NP). Elles ont une sensibilité équivalente à l'immunofluorescence, mais sont plus faciles à mettre en œuvre, et moins subjectives dans leur interprétation.
L'utilisation de ces tests rapides n'est en général pas recommandée par l'OMS pour le diagnostic des infections humaines dues à un virus grippal aviaire. Ils permettent le diagnostic d'une grippe de type A ou B. Ils ne permettent pas la différenciation certaine du sous-type et un résultat négatif ne peut exclure la présence d'une infection. Ils peuvent être utilisés uniquement dans le cas où la confirmation peut être apportée par un test de RT-PCRRT-PCR (voir ci-dessous), disponible localement, ou dans le cas contraire, par l'envoi des prélèvements à un laboratoire de référence national ou du réseau de l'OMS.
- Technique de RT-PCR ou technique d'amplification en chaîne par polymérisation après transcriptiontranscription inverse. Elle permet d'amplifier le génomegénome viral, de détecter spécifiquement un ARN viral et donc d'identifier le type et le sous-type viral (Coiras, Aguilar et al. 2001 25) (Ellis and Zambon 2001 33). Les résultats sont disponibles en quelques heures. Elle utilise la transcription inverse de l'acide ribonucléiqueacide ribonucléique (ARN) viral en ADNADN complémentaire (ADNcADNc). Elle requiert une paire d'amorces oligonucléotidiques; les amorces sont basées sur les séquences connues de la protéineprotéine HA et N1 des virus influenza A et permettent d'amplifier spécifiquement un sous-type.
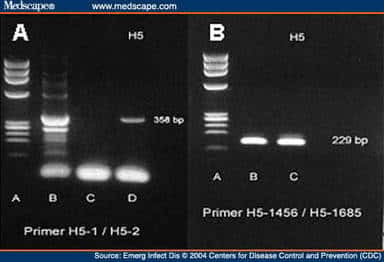
Diagnostic par technique de RT-PCR du virus H5. © Center for disease control and prevention, reproduction et utilisation interdites
Récemment, des tests multiplex appliqués à la détection du virus A (H5N1) sont apparus (Payungporn, Chutinimitkul et al. 2006 75), ciblant de façon simultanée :
- deux régions différentes du gènegène HA du virus A (H5N1)(Ng, Cheng et al. 2005 70) ;
- ou des séquences des gènes M, H5 et N1 en seul passage (single set) ; les amorces sont sélectionnées à partir de 75 séquences conservées répertoriées du gène de la protéine M et de 50 régions invariables connues, spécifiques des gènes H5 et N1(Amonsin, Payungporn et al. 2005 6).
L'OMS recommande l'utilisation des amorces pour l'amplification des gènes H5, H9 et N1.
C'est une technique qui tend progressivement à remplacer les méthodes traditionnelles ; elle bénéficie d'une excellente sensibilité, la spécificité est dépendante de la pertinence des amorces utilisées ; elle ne nécessite pas de virus vivant et peut donc s'opérer en laboratoire de niveau de sécurité classique.
L'OMS a mis en place un comité technique dont le travail consiste à développer et actualiser les amorces en fonction de l'évolution antigénique des virus.
Isolement du virus
- L'inoculation se réalise soit sur œufs de poule embryonnés d'une dizaine de jours (peu utilisé actuellement), soit sur culture de cellules rénales de chienchien (cellules MDCK) et donne des résultats en deux à dix jours. Pour des raisons de biosécurité, l'isolement des souches hautement pathogènes doit être réalisé en laboratoire de confinement de niveau trois ou supérieur.
- Les cultures positives peuvent exhiber ou non des effets cytopathogènes, c'est-à-dire des modifications morphologiques des cellules infectées, par exemple une rétraction des cellules qui apparaissent réfringentes et de tailles inégales, et, surtout, la multiplication virale permet la mise en évidence de l'hémagglutininehémagglutinine par hémadsorption (fixation des globules rougesglobules rouges sur la couche cellulaire).
- L'identification du virus s'obtient par technique d'immunofluorescence des cellules infectées, d'inhibitioninhibition de l'hémagglutination du supernatant, à l'aide d'anticorps monoclonaux spécifiques.
- La culture virale est considérée comme le « gold standard » car elle permet à la fois l'identification du virus, sa caractérisation et l'étude de sa variabilité antigénique et génétiquegénétique, notamment par technique de RT-PCR, la réalisation des tests de sensibilité médicamenteuse et la préparation de vaccinsvaccins (Collins, Ko et al. 2002 26).
Tout diagnostic d'infection par le virus influenza A, suspect d'être d'origine aviaire, doit être confirmé par un laboratoire de référence pour la grippe aviaire de l'OMS, en période d'alerte interpandémique ou pandémique.
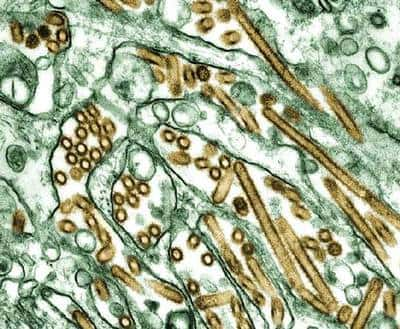
Le virus influenza A(H5N1) en culture sur des cellules MDCK (en vert). © CDC, K.Goldsmith, J. Katz and S. Zaki, reproduction et utilisation interdites
Les laboratoires n'ayant pas la capacité d'effectuer le sous-typage du virus influenza A se doivent d'adresser les échantillons à un centre national pour la grippe ou à un laboratoire de référence pour le virus H5, mis sur pied par l'OMS et d'informer toute instance régionale, nationale ou internationale de l'OMS de la destination des prélèvements et isolats viraux.
Chez l'oiseauoiseau, on évalue la virulence de la souche obtenue en culture par injection intraveineuse chez des poulets. Les virus influenza aviaires hautement pathogènes sont définis dans la directive européenne 92/40/CEE, et au Journal Officiel Arrêté du 8 juin 1994.
Il est important de mener les études d'épidémiologie moléculaire de façon parallèle chez l'animal et l'homme, en cas d'épizootie concomitante, afin de suivre l'évolution de l'infection humaine et sa propagation, soit directe à partir des oiseaux, soit inter-humaine.
La souche H5N1, isolée chez l'homme au Vietnam a été en partie séquencée et a révélé que tous les gènes sont d'origine aviaire.
2. Le diagnostic indirect
La sérologie présente peu d'intérêt en pratique clinique ; elle est très importante a posteriori dans les enquêtes épidémiologiques sur les flambées épidémiques.
L'identification sérologique du virus influenza A (H5N1) repose sur la mesure d'anticorps spécifiques par méthode immunoenzymatique, inhibition de l'hémagglutination ou test de neutralisation.
Les anticorps neutralisants apparaissent une dizaine de jours après la contaminationcontamination.
- L'inhibition de l'hémagglutination est l'examen de référence pour la détection des anticorps dirigés contre les virus grippaux humains, mais dans sa forme standard, il a montré ses limites dans le diagnostic des infections à virus aviaires. Récemment (Stephenson, Wood et al. 2003 88), une modification du test classique qui utilise des érythrocytes de cheval en remplacement des érythrocytes de dinde, a montré une sensibilité équivalente au test de micro-neutralisation dans les études sérologiques des personnes exposées aux virus A (H7N7) en 2003, aux Pays-Bas. La présence des liaisons galactose/acide sialique de type α(2,3) à la surface des érythrocytes de cheval explique l'affinité de l'hémagglutinine des virus aviaires pour ce type de récepteur (Meijer, Valette et al. 2005 65) (Puzelli, Di Trani et al. 2005 79).
- La technique ELISA nécessite des antigènes hautement purifiés ; de plus, une réactivité croisée a été signalée entre des différents sous-types d'hémagglutinine.
- Le test de microneutralisation est le test de choix pour la mise en évidence d'anticorps dirigés contre les virus aviaires hautement pathogènes. Il permet la détection d'anticorps spécifiques anti-HA, à des titragestitrages que ne permettent pas les techniques d'inhibition de l'hémagglutination.
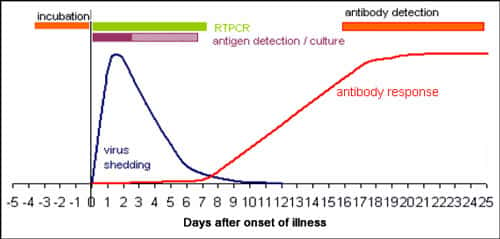
Anticorps sériques dirigés contre le virus influenza. © Marion Zambon, Health Protection Agency, reproduction et utilisation interdites
Le principe repose sur l'inhibition, par les anticorps sériques neutralisants anti-HA, des effets cytopathogènes provoqués par le virus sur des cellules MDCK en culture. Après une incubation du virus en présence de dilutions progressives de sérumsérum, la protéine NP du virus influenza A est mise en évidence par technique ELISA au niveau des cellules infectées. Les résultats sont observables en 48 heures.
En raison de la manipulation de virus vivant, ces tests sont effectués en laboratoire de niveau trois de confinement.
Des études récentes ont éprouvé la performance de l'association de différentes techniques sérologiques. L'utilisation des tests de micro-neutralisation ou ELISA avec confirmation par des méthodes de western-blot a fait ses preuves en termes de sensibilité et spécificité dans les études séroépidémiologiques des infections à A (H5N1) (Rowe, Abernathy et al. 1999 81).