au sommaire
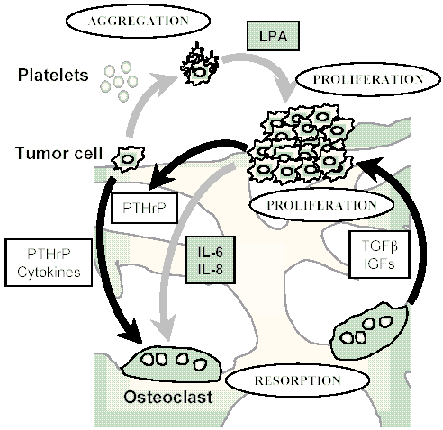
Schéma illustrant le « cercle vicieux » au niveau duquel les phénomènes de résorption osseuse et développement tumoral s'entretiennent mutuellement (INSERM)
Les cancers du sein induisent fréquemment la formation de métastases osseuses au niveau desquelles les cellules tumorales produisent un certain nombre de facteurs (cytokines, PTHrP) qui entraînent la dégradation de l'os. Le tissu osseux est un réservoir de facteurs de croissance tels le TGFb et les IGFs. Ces facteurs de croissance libérés de la matrice osseuse stimulent alors à la fois le développement des cellules tumorales et la production par les cellules tumorales de facteurs (PTHrP) chargés de stimuler l'activité de résorption des ostéoclastesostéoclastes (cf. schéma, flèches noires). On décrit la formation d'un « cercle vicieux » au niveau duquel les phénomènes de résorption osseuse et développement tumoraltumoral s'entretiennent mutuellement.
Les traitements actuels des patients ayant des métastases osseuses, utilisant des inhibiteurs de la résorption osseuse tels que les bisphosphonates, permettent de ralentir la progression de la destruction osseuse mais restent malheureusement inefficaces quant à l'évolution ultime de ces métastases.
OlivierOlivier Peyruchaud et ses collaborateurs ont observé que l'activité mitogènique du LPA (l'activité mitogénique est l'activité qui stimule la prolifération cellulaire) sur une série de lignées cellulaires humaines de cancer du sein était dépendante de la présence des récepteurs du LPA (LPA1, LPA2 et LPA3). En utilisant une de ces lignées cellulaires comme modèle d'étude, les chercheurs ont observé que la sur-expression inductible de l'un de ces récepteurs (LPA1) sensibilise de façon spécifique ces cellules à l'action mitogénique du LPA in vitroin vitro. In vivoIn vivo, la sur-expression de LPA1 dans les cellules tumorales étudiées amplifie la croissance de xénogreffesxénogreffes sous-cutanées et augmente de façon dramatique la formation des métastases osseuses chez l'animal, en augmentant à la fois la croissance de la massemasse tumorale et la destruction osseuse. Ces résultats suggèrent que du LPA est produit localement dans l'environnement tumoral. Les chercheurs de l'Inserm ont montré que le LPA d'origine plaquettaire est actif sur les cellules tumorales, en stimulant leur prolifération et la production des interleukinesinterleukines IL-6 et IL-8 qui sont deux stimulateurs puissants de la résorption osseuse. Par ailleurs, le blocage de la libération du LPA plaquettaire chez l'animal inhibe la progression des métastases osseuses induites par les cellules tumorales, en agissant sur la progression des lésions ostéolytiques et de la masse tumorale.
Ces résultats suggèrent que la métastase osseuse est le siège d'une cascade de réactions impliquant cellules tumorales, LPA, plaquettes sanguinesplaquettes sanguines activées, et interleukines IL-6 et IL-8. L'ensemble de ces interactions aboutit à la croissance tumorale et la résorption osseuse, et à l'amplification du « cercle vicieux » qui s'établit entre les cellules de cancer du sein et les ostéoclastes.