au sommaire

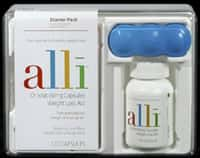
Alli se veut un allié pour perdre du poids. Il ne doit pas empêcher de limiter sa consommation de produits riches en graisses. © Rozmaryna/Fotolia
Un mois avant la commercialisation en France et sans ordonnance d'Alli, le nouveau médicament anti-obésité de GSK, l'Agence française de sécurité sanitaire des produits de santé (AFSSAPS) rappelle l'existence d'un Plan européen de gestion des risques concernant ce médicament (voir les liens au bas de cet article). L'objectif : détecter tout effet indésirable et collecter des informations sur le profil des utilisateurs.
Malgré son nouveau statut de produit d'auto-médication, Alli (un nom de baptême qui vient de la contraction de Al-eye, évoquant phonétiquement, en anglais, le mot allié) est en effet un vrai médicament. Il est une version allégée (60 mg au lieu de 120 mg) de l'actuel Xenical, vendu, lui, sur prescription en France, et aux Etats-Unis sous le nom d'Orlistat. Il inhibe les lipases intestinales, c'est-à-dire les enzymesenzymes qui, dans l'intestin, se chargent de la première étape de la digestion des graisses (les lipides). On peut donc être tenté d'en consommer beaucoup : elles seront peu digérées...
Diffusion sous haute surveillance
Alli a obtenu son Autorisation de mise sur le MarchéAutorisation de mise sur le Marché européenne (AMM) en janvier 2009 et devrait arriver dans les officines début mai. Toutefois, son arrivée s'effectue sous haute surveillance : pharmacovigilance renforcée avec nomination d'un centre régional chargé du suivi national du produit, mise à disposition des pharmacienspharmaciens d'une fiche d'aide à la dispensation et « envoi d'une lettre d'information aux médecins dans le même esprit » précise l'AFSSAPS.
Par ailleurs, ce nouveau médicament est contre-indiqué chez certains patients, notamment les moins de 18 ans, les femmes enceintes ou allaitantes et les personnes sous traitement anticoagulantanticoagulant oral.