au sommaire
Classée VIP- Very Important Paper -, la publication de l'équipe grenobloise de l'ESRF (European Synchrotron Radiation Facility) dans la revue Angewandte Chemie a déjà fait le tour du monde. Défiant les lois de la physique, la découverte ouvre en effet une nouvelle piste pour le stockage de l'hydrogène, un domaine de recherche hyperactif. Chimistes et physiciensphysiciens du monde entier s'acharnent depuis des années sur le sujet pour faire entrer la plus grande quantité possible d'hydrogène dans le volume le plus petit possible et dans des conditions pas trop contraignantes. On pourrait ainsi amener nos voitures électriquesvoitures électriques dans une station service pour faire le plein d'hydrogène (qui aura été fabriqué ailleurs, dans une centrale). Sous le capot, la pile à combustible le combinera à l'oxygèneoxygène de l'airair et en fera de l'eau, plus de l'électricité qui fera tourner le moteur.
Mais l'élément le plus léger de l'universunivers ne se laisse pas dompter facilement. Pour en retenir une quantité suffisante, on peut le liquéfier mais il faut une température extrêmement basse (- 253 °C), ou bien le comprimer, mais à des pressionspressions élevées (plusieurs centaines de barsbars). Les scientifiques cherchent plutôt des composés dans lesquels l'hydrogène est chimiquement lié. Le méthanol est un candidat (mais la réaction produit du CO2). Les hydrures semblent plus intéressants. L'équipe suisse-norvégienne de l'ESRF s'est penchée sur l'un d'eux, un matériaumatériau bien connu, le borohydrure de lithiumlithium (ou lithium borohydride en franglais), de formule LiBH4.
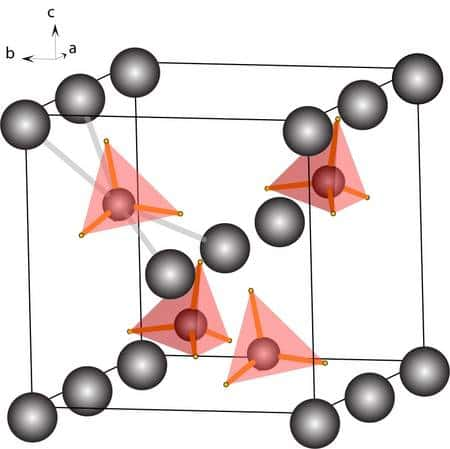
La nouvelle structure du borohydrure de lithium. En gris, les atomes de lithium, en rose-orangé, les tétraèdres d’hydrure de bore, étonnamment proches, les atomes d’hydrogène n’étant éloignés que d’environ 1,9 angström. © Y. Filinchuk, D. Chernyshov, A. Nevidomskyy et V. Dmitriev
Précieuse instabilité
Ce solidesolide (que l'on trouve sous forme de poudre) était déjà candidat pour le stockage d'hydrogène puisqu'il en contient 18 %, en poids. Mais ce composé est stable, beaucoup trop pour en extraire facilement l'hydrogène. Il faut en effet le chauffer à plus de 300 °C. L'équipe a cherché à en obtenir des formes nouvelles et en a effectivement découvertes deux en exerçant une pression de 200.000 atmosphèresatmosphères. Très élevée, cette valeur n'est cependant pas un record.
La surprise est venue de l'une des formes obtenues, qui a pu être étudiée à l'aide d'un rayonnement X synchrotron. C'est l'utilisation de cet instrument particulier (où le rayonnement provient de l'émissionémission de particules de matièrematière accélérées) qui a permis de bien visualiser la structure. En effet, l'hydrogène, si petit, ne se laisse pas facilement voir en radiographieradiographie X classique et il faut la puissance du rayonnement synchrotronrayonnement synchrotron pour y parvenir.
Dans cette forme de LiBH4, les atomesatomes d'hydrogène sont très proches les uns des autres. Cette structure n'avait jamais été prédite par les modèles théoriques, qui doivent donc être révisés... De plus, cette forme est instable, une aubaine pour les scientifiques. En effet, cette instabilité promet une extraction plus facile de l'hydrogène. Cette nouvelle forme « est réellement inattendue et très encourageante » estime Yaroslav Filinchuk, l'un des membres de l'équipe.
On peut donc espérer descendre largement sous les 300 °C pour récupérer l'hydrogène contenu dans le borohydrure de lithium. La pression élevée nécessaire à la fabrication de cette nouvelle forme de LiBH4 n'est sans doute pas un obstacle. « La structure commence à apparaître à 10.000 atmosphères, rapporte Yaroslav Filinchuk, soit la pression utilisée par l'industrie pharmaceutique pour comprimer les pilules ».
Le travail ne fait que commencer. Il reste à vérifier que les possibilités de stockage sont bien réelles puis à trouver un procédé chimique pour obtenir un matériau facilement utilisable. Bref, une piste à explorer...