au sommaire

Une machine dont le fonctionnement ne s'explique que par la nanostructure de ses photoélectrodes. © John Guerra, Nanoptek
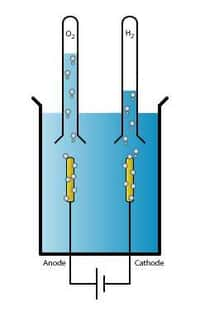
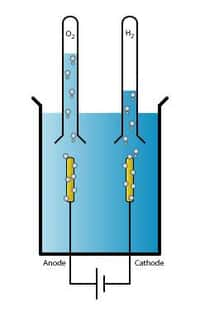
Pour produire de l'hydrogène, dont on espère qu'il pourra servir de carburant, il faut dépenser beaucoup d'énergie. Ce gaz ultra-léger, que la Terre n'a pas pu retenir, est rare sur notre planète et il faut donc le fabriquer. Casser une molécule d'eau est un moyen simple, l'opération produisant de l'oxygène et de l'hydrogène. On connaît bien l'électrolyseélectrolyse, qui utilise une différence de potentiel électrique, l'hydrogène étant alors produit au niveau de la cathodecathode.
Une autre voie, explorée depuis longtemps, est la photolysephotolyse, dans laquelle l'énergie de la lumièrelumière provoque la cassure des molécules d'eau. On utilise des cellules photoélectrochimiques (PEC), constituées d'électrodesélectrodes photosensibles et plongées dans l'eau. La lumière absorbée génère des électronsélectrons (négatifs) et des charges positives formées par des manques d'électrons appelés trous. En présence de ces paires électrons-trous, les molécules d'eau subissent une réaction d'oxydo-réduction. Hydrogène et oxygène partent chacun de leur côté sous forme gazeuse, H2 et O2.
Pour parvenir à un résultat correct, il faut trouver le bon candidat pour les électrodes. Le dioxyde de titanedioxyde de titane (TiO2) fait partie de la liste. On en trouve une forme dans la nature, appelée rutile et il semble que les premiers essais datent de 1970...
C'est ce matériaumatériau qu'ont utilisé les ingénieurs de la société américaine Nanoptek en améliorant ses performances grâce aux nanotechnologiesnanotechnologies. Le dioxyde de titane ne peut nativement absorber que des ultravioletsultraviolets (parce qu'ils sont plus énergétiques). C'est un handicap puisqu'il ne capte qu'une faible partie de l'énergie de la lumière. Pour le rendre plus docile, les ingénieurs de Nanoptek l'ont étalé sur des nanostructures en forme de dômes.
Enfin dans le visible
Le résultat est que les atomesatomes sont plus éloignés les uns des autres que dans le cristal naturel de dioxyde de titane. L'énergie nécessaire pour arracher des électrons (ce que fait la lumière) devient plus faible. Un rayonnement de moindre énergie, donc de longueur d'ondelongueur d'onde plus grande que l'ultraviolet, peut alors extraire ces électrons. L'équipe est parvenue de cette manière à réaliser une PEC au dioxyde de titane produisant du courant électriquecourant électrique à partir de la lumière bleuelumière bleue. Le rendement serait six fois meilleur que celui obtenu avec le dioxyde de titane natif.
La société n'en dit pas plus sur les performances et ce n'est sans doute pas demain que nous verrons fleurir des producteurs d'hydrogène dans les jardins. Mais la voie explorée est classique - la photolyse est connue depuis des lustres - et la méthode originale - l'utilisation de nanostructures pour ajuster les propriétés du matériau photosensible. Ces deux qualités rendent la solution plutôt attractive face aux voies de recherches concurrentes qui consistent à trouver un matériau le plus efficace possible et, en général, à l'enrichir à l'aide d'un dopant pour décaler vers le visible la bande de longueurs d'onde à laquelle il absorbe l'énergie lumineuse.
On attend avec intérêt la première production d'hydrogène significative...