au sommaire
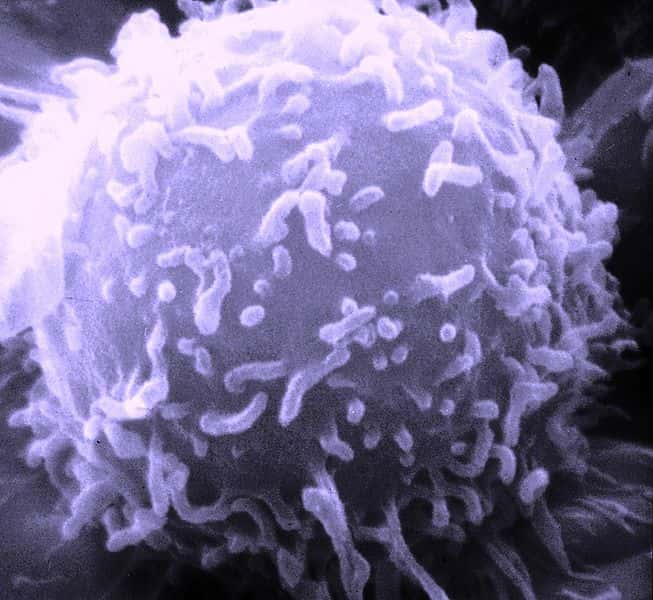
Un lymphocyte vu au microscope électronique à balayage. © DR
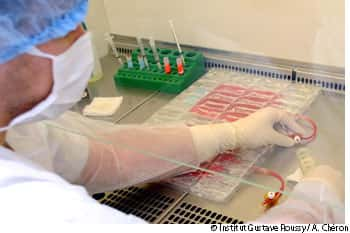
Les vaccins permettent traditionnellement de lutter contre des maladies infectieuses provoquées par des virus ou des bactéries, en présentant au système immunitaire une moléculemolécule d'origine étrangère. Le système immunitaire fabrique des anticorps dirigés contre la molécule en question et sera prêt à attaquer tout envahisseur y ressemblant fortement. Une nouvelle génération de vaccin, testé chez la souris, la protégerait contre son propre système immunitaire ! Cette première a été publiée dans la revue Journal of Clinical Investigation.
L'idée de ce vaccin innovant a immergé par la constatation que le système immunitaire ne réagit pas uniquement contre des molécules étrangères : les cellules immunitaires reconnaissent également des molécules que l'organisme lui-même fabrique. Ces réactions sont à l'origine de maladies dites auto-immunes (polyarthrite rhumatoïde, sclérose en plaques, diabètediabète...) que l'on peut reproduire en laboratoire sur des souris en leur injectant leurs propres antigènesantigènes.
Les NKT protègent des maladies auto-immunes
Les maladies auto-immunes se développent plus volontiers chez des personnes déficientes en un certain type de cellules immunitaires, les lymphocyteslymphocytes natural killer TT (NKT). Les NKT forment un groupe très peu abondant (0,2 % des lymphocytes T) dont le rôle, encore débattu, est de réguler un certain nombre de mécanismes.
Certains articles ont montré leurs rôles dans la régulation des maladies auto-immunesmaladies auto-immunes, dans la tolérance des greffonsgreffons, dans la lutte contre les infections, dans le rejet des tumeurstumeurs, tout cela grâce à la sécrétionsécrétion rapide et en grandes quantités de cytokinescytokines qui régulent les réactions inflammatoires.
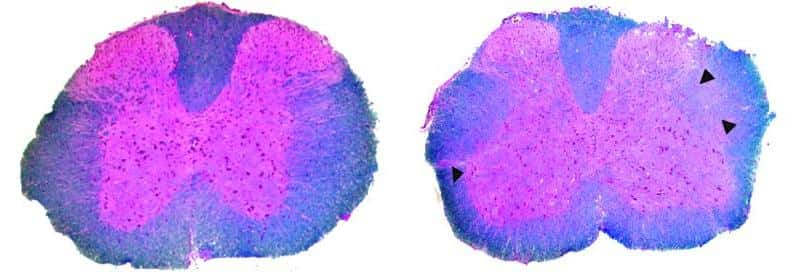
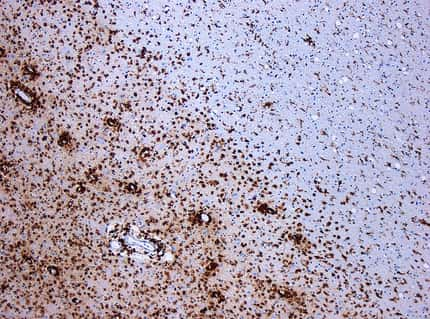
Chez les souris modèles de la sclérose en plaques, la démyélinisation du système nerveux central est moins observée lorsqu'elles sont vaccinées (à gauche) que lorsqu'elles ne le sont pas (à droite). © Journal of Clinical Investigation
La vaccination entraîne un effet anti-inflammatoire non spécifique
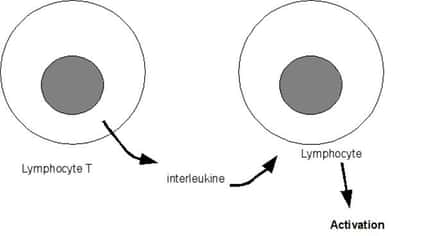
Habituellement, les NKT sont activés par des lipideslipides qui leur sont présentés par des cellules présentatrices d'antigènes. Dans ce nouvel article, les chercheurs ont démontré qu'une molécule autre qu'un lipide peut également activer les NKT : il s'agit d'un peptide (un morceau de protéineprotéine) provenant du collagènecollagène de type II de souris.
Les recherches ont été effectuées chez des souris de huit à 14 semaines, qui ont reçu la vaccinationvaccination, c'est à dire des injections de ce peptide. Dix à 13 jours plus tard, les chercheurs ont constaté une inhibitioninhibition des lymphocytes T helper (Th1 et Th2) qui sont habituellement impliqués dans les réponses immunitaires cellulaires et humorales. Pour observer l'effet de cette inhibition sur l'arthritearthrite rhumatoïde, cette maladie a été déclenchée par l'injection de la protéine entière de collagène, 10 jours après la vaccination. Dans ce cas, la réaction inflammatoire dans les tissus articulaires diminue.
Mais le bénéfice du vaccin ne s'arrêterait pas là : il permettrait aussi de limiter les conséquences d'autres maladies auto-immunes et inflammatoires, non liées au collagène. Les souris atteintes de la sclérose en plaque (démyélinisationdémyélinisation du système nerveux centralsystème nerveux central) ou de l'asthmeasthme (inflammationinflammation des voies aériennes par un antigène) sont moins atteints, indiquant que la vaccination n'est spécifique ni de l'antigène ni du tissu.
Même si les effets sont parfois légers, pour les auteurs, il n'y a pas de doute quant aux perspectives qu'ouvrent ces résultats. « Compte tenu du haut degré de conservation des cellules NKT parmi les espècesespèces, l'immunisation thérapeutique à l'aide d'un peptide activant les NKT pourrait tenir des promesses pour le bénéfice clinique dans le cas de maladies inflammatoires humaines », expliquent-ils. Toutefois, « sachant que les cellules NKT peuvent supprimer ou activer l'immunitéimmunité, leur utilisation thérapeutique nécessite une compréhension approfondie de leur biologie intrinsèque ».