au sommaire
L'immunothérapie avec les cellules CAR Tcellules CAR T fait naître de nombreux espoirs dans le traitement des leucémies. Généralement, dans ce type de thérapie encore expérimentale, les médecins prélèvent des cellules sur le patient, les manipulent génétiquement et les réinjectent au malade. Les lymphocytes T du patient sont modifiés afin d'exprimer un récepteur (CAR19) dirigé contre un antigène des lymphocytes B (CD19). Testé dans des essais cliniquesessais cliniques, ce traitement n'est pas disponible pour tous.
Cette technique a déjà montré des résultats encourageants, avec des rémissionsrémissions chez des patients leucémiques, ainsi que dans un cas de cancer du cerveau. Mais la méthode est difficile à mettre en œuvre chez des nourrissons ou des patients déjà lourdement traités. C'est pourquoi des chercheurs ont mis en place un protocoleprotocole utilisant des cellules provenant du sang d'un donneur et non des malades.
Des médecins de l'hôpital Great Ormond Street à Londres pensent avoir ainsi guéri d'une leucémie deux petites filles âgées de 11 et 16 mois. Leurs résultats paraissent dans la revue Science Translational Medicine.
Ici, les scientifiques ont utilisé les outils TALEN pour modifier le génome des cellules. © Mopic, Fotolia
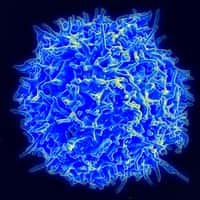
Des lymphocytes T manipulés pour tuer les cellules cancéreuses
Pour y arriver, ils ont généré des lymphocytes T CAR19 « universels » (UCART19) à partir de cellules d'un donneur. Plusieurs modifications génétiquesgénétiques ont été réalisées : l'une d'entre elles devait éviter que le système immunitairesystème immunitaire reconnaisse les cellules du donneur comme étrangères, une autre a permis aux cellules de s'attaquer aux celles qui sont cancéreuses, et une dernière visait à éviter la réponse du patient contre le greffongreffon. Les modifications génétiques ont été réalisées avec le système TalenTalen.
Les deux fillettes souffraient toutes les deux d'une leucémie aiguë lymphoblastiqueleucémie aiguë lymphoblastique. La rémission a été observée au bout de 28 jours de traitement. Mais il est difficile de confirmer que la thérapie cellulairethérapie cellulaire est la seule responsable de la guérisonguérison, car les deux petites patientes ont aussi eu une chimiothérapiechimiothérapie en plus de ce traitement expérimental.
L'utilisation de cellules d'un donneur présente plusieurs avantages. Tout d'abord, le patient peut être traité plus rapidement, puisqu'il n'a pas besoin d'attendre que les siennes soient préparées. De plus, le sang d'un seul donneur peut servir à fabriquer des centaines de doses pour traiter des patients, ce qui réduit énormément le coût du traitement. D'après Julianne Smith, de l'entreprise Cellectis, spécialisée dans le développement des cellules CAR T, le coût de fabrication d'une dose serait d'environ 4.000 dollars, soit plus de dix fois moins que le traitement qui utilise les cellules du patient (environ 50.000 dollars).
Contre la leucémie, un nouveau traitement affiche 93 % de réussite
Article de Marie-Céline Jacquier, paru le 30/04/2016
C'est le résultat obtenu chez 29 patients leucémiques dont 27 étaient en phase de rémission après un nouveau traitement expérimental. Cette immunothérapie utilise des lymphocytes du patient, modifiés au laboratoire pour réagir contre les cellules cancéreuses.
93 % de rémission : voici le résultat très prometteur d'un nouveau traitement encore expérimental testé sur une trentaine de patients leucémiques et présenté dans la revue Journal of Clinical Investigation. Il s'agit d'un véritable espoir pour ceux qui ont épuisé d'autres options thérapeutiques, sans être un traitement miracle non plus. Explications.
En théorie, notre système immunitaire est capable d'éliminer des cellules cancéreuses, grâce aux lymphocytes T. Mais parfois les lymphocytes T ne peuvent pas détecter les cellules cancéreuses ; une fois que les tumeurs se forment, les cellules cancéreuses échappent au système immunitaire. D'où l'idée de ce nouveau traitement : utiliser le système immunitaire du patient pour qu'il s'attaque lui-même aux cellules cancéreuses.
Pour ce faire, les chercheurs extraient des lymphocytes T des patients à partir de leur sang. Ensuite, ils les modifient génétiquement pour qu'ils portent un récepteur CAR (Chimeric Antigene Receptor) qui reconnaît CD19, un marqueur de cellules de leucémie. Le récepteur CAR permet donc une activité anti-tumorale vis-à-vis des leucémies. Puis les chercheurs multiplient ces lymphocytes T améliorés et les injectent au patient.
Au départ de cette étude, 32 patients âgés de 20 à 73 ans (âge médian : 40 ans) devaient participer, mais deux ont eu des complications avant la thérapie et sont sortis de l'essai clinique. Les 30 patients leucémiques restants ont tous reçu des lymphocytes T modifiés mais l'un d'entre eux est décédé rapidement et n'a pas pu être évalué. Deux à quatre semaines après le traitement, les chercheurs ont évalué la rémission des patients par cytométrie de flux. 27 patients, soit 93 %, n'avaient pas de leucémie détectable.
Les lymphocytes T peuvent s’attaquer aux cellules cancéreuses. Des cellules clés pour combattre le cancer. © royaltystockphoto.com, Shutterstock
Une étude préliminaire encourageante mais avec des effets secondaires
Cameron Turtle, du Fred Hutchinson CancerCancer Research de Seattle, explique que les patients qui sont entrés dans l'essai clinique avaient peu d'options de traitement. Le fait qu'il y ait un tel pourcentage de rémission leur donne un véritable espoir. David Maloney, l'un de ses collaborateurs, est enthousiaste : « Vous ne vous attendez pas à des résultats comme ceux-ci des essais de phase précoce. Voilà pourquoi ces taux de réponse sont si extraordinaires. »
Cependant, les résultats doivent être interprétés avec prudence. Tout d'abord, le traitement reste expérimental. De plus, tous les patients ne sont pas restés en rémission : certains ont rechuté. Chez certains patients, le cancer a réussi à résister aux lymphocytes T injectés. Pour expliquer les rechutesrechutes et les échecs, les chercheurs émettent comme hypothèse que le système immunitaire a réagi contre les cellules injectées, à cause des épitopesépitopes du transgène.
Si ces résultats montrent la faisabilité de cette nouvelle approche, la technique demande à être améliorée, notamment à cause de sa toxicitétoxicité : des signes de neurotoxicité étaient manifestes (encéphalopathie par exemple), et les effets secondaires étaient importants. Une étude de dosagedosage doit aussi améliorer ce traitement.
Il est encore trop tôt pour savoir quels seront les effets à long terme sur les patients et surtout si leur rémission va durer. L'étude reste limitée en taille. Mais cela reste une première étape intéressante pour des travaux futurs. Ces résultats encourageants devraient donner lieu à des essais cliniques de plus grande envergure, comme l'explique Cameron Turtle : « C'est juste le début. Il paraît fantastique de dire que nous obtenons plus de 90 % de rémissions, mais il y a tellement de travail à faire pour s'assurer que ce sont des rémissions durables, de travailler sur qui va bénéficier le plus, et d'étendre ce travail à d'autres maladies. »