au sommaire
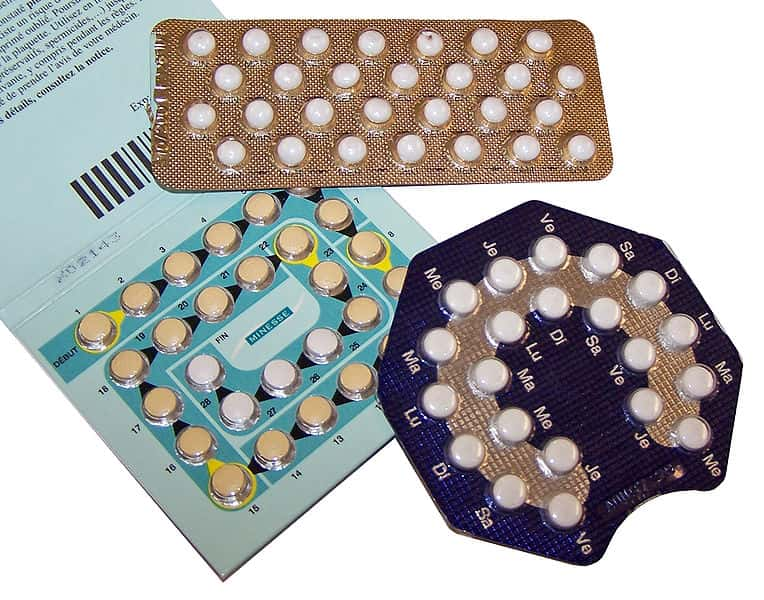
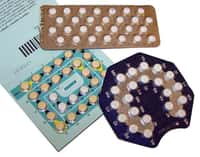
Comme le Diane 35 sera suspendu dans trois mois, des centaines de milliers de femmes qui l'utilisaient comme contraceptif devront se rabattre sur d'autres pilules. Ou pourquoi pas d'autres techniques, comme le stérilet. © Ceridwen, Wikipedia, cc by sa 2.0
L'autorisation de mise sur le marchéautorisation de mise sur le marché (AMM) du médicament anti-acnéique Diane 35 va faire l'objet d'une procédure de suspension en France. La suspension ne sera effective que dans trois mois. Réévalué par l'Agence nationale de sécurité du médicament et des produits de santé (ANSM), son rapport bénéfices/risques s'est avéré défavorable dans le traitement de l'acné. Par la même occasion, l'agence du médicament souhaite interrompre sa prescription (hors AMM) à but contraceptif. Le délai de trois mois a été décidé pour laisser le temps aux patientes de changer de traitement, avec l'aide de leur médecin.
« L'Agence nationale de sécurité du médicament et des produits de santé estime que le rapport bénéfices/risques du Diane 35 et de ses génériques est défavorable dans le traitement de l'acné, au regard notamment du risque thromboembolique veineux et artériel », a indiqué Dominique Maraninchi, directeur général de l'ANSM, au cours d'une conférence de presse (quelque peu précipitée) mercredi 30 janvier. En effet, « de nouvelles données [...] démontrent un risque thromboembolique veineux quatre fois plus élevé que celui des femmes qui ne prennent pas ces traitements ». Depuis 1987, date de sa mise sur le marché en France, au moins quatre femmes sont décédées en raison de la prise de Diane 35.
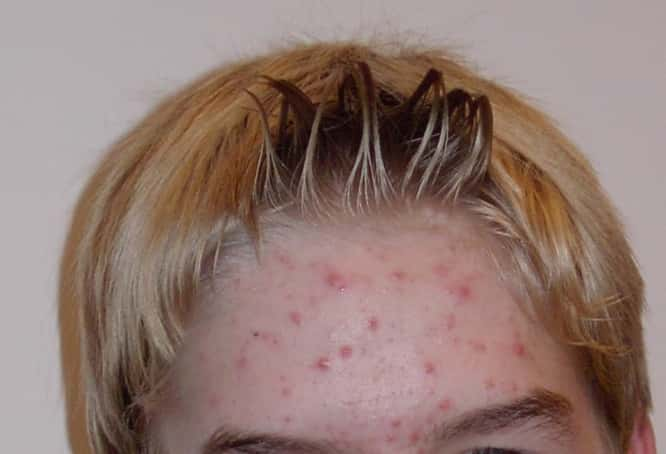
Commercialisé dans le traitement de l'acné, le Diane 35 était connu pour ses propriétés contraceptives et notamment prescrit à des adolescentes pour faire d'une pierre deux coups. Mais son évaluation par l'ANSM semble montrer que même dans son indication originelle, le médicament sera suspendu. © Ellywa, Wikipédia, DP
Le Diane 35 suspendu dans trois mois seulement
« De surcroît, l'usage important de ces médicaments en tant que contraceptifs n'est pas conforme et leur efficacité [...] n'a pas été démontrée par des études cliniquesétudes cliniques appropriées, a rappelé l'ANSM. Dans ce contexte, après information des laboratoires concernés, l'ANSM déclenche une procédure de suspension des AMM des médicaments » en question.
« Afin de permettre aux femmes concernées de consulter leur médecin et de réexaminer avec lui la meilleure option thérapeutique alternative, cette suspension prendra effet dans un délai de l'ordre de trois mois », indique l'ANSM. En attendant, l'agence sanitaire dispense des recommandations de prudence :
- les patientes ne doivent pas interrompre brutalement leur traitement ;
- les médecins ne doivent plus prescrire ces médicaments (ni initiation de traitement ni renouvellement) ;
- les pharmacienspharmaciens pourront délivrer les traitements minimaux nécessaires pour éviter toute rupture brutale de traitement jusqu'à ce que la patiente consulte à nouveau son médecin ou un autre prescripteur (délivrance de boîtes d'un mois de traitement préférentiellement).
À l'issue de cette période de trois mois, « toute prescription et toute délivrance seront interdites et l'ensemble des lots présents sur le marché sera retiré ». Ces médicaments sont autorisés dans la plupart des autres États membres de l'Union européenne. Sur demande de la France, l'Agence européenne des médicaments (Ema) avait déjà entamé une procédure de réévaluation des pilules de troisième et quatrième générations, lundi 28 janvier. L'ANSM annonce qu'elle « initiera une procédure d'arbitrage au niveau communautaire, visant à retirer, suspendre ou modifier l'ensemble des AMM concernées [pour le Diane 35 et ses génériques, NDLRNDLR] en Europe ».