au sommaire
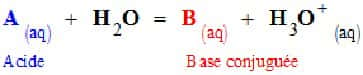
Généralisation d'une réaction entre un acide (A) et l'eau. L'équilibre de la réaction chimique fait intervenir la base conjuguée (B) de l'acide. © DR
Il existe plusieurs définitions d'un acide (Arrhénius, Brönsted...) mais la conception de Lewis est la plus large. Cette dernière précise qu'un acide est un accepteur de doublet d'électrons (donc possédant une orbitaleorbitale vide).
Acide et base conjuguée
À tout acide correspond une base conjuguée et vice versa. Une base est par conséquent un donneur de doublet d'électrons. La force d'un acide et de sa base conjuguée sont liées. Si un acide est fort, sa base conjuguée est faible et réciproquement.
Généralités sur les acides
Un acide colore de rouge le papier tournesoltournesol et possède un pH inférieur à 7.